Электролиз раствора сульфата меди — это процесс, при котором с помощью электрического тока осуществляется разложение раствора сульфата меди на компоненты. Основной целью этого процесса является получение меди, которая является одним из наиболее распространенных и полезных металлов. Однако, помимо меди, этот метод также позволяет получать и другие металлы.
Процесс электролиза основан на использовании двух электродов: положительного (анода) и отрицательного (катода). Раствор сульфата меди помещается в электролитическую ячейку, где анод и катод накапливаются отдельно друг от друга. При пропускании тока через раствор, ионы меди соответственно ионизируются и мигрируют к катоду, где и осаждаются, образуя металлическую медь.
За последние десятилетия, электролиз раствора сульфата меди стал широко применяемым процессом в промышленности. Медь, полученная этим способом, используется для производства проводов, кабелей, труб, медицинского оборудования и многих других изделий.
Кроме получения меди, электролиз раствора сульфата меди также позволяет получить и другие металлы. Например, при использовании железного анода вместо медного, процесс электролиза позволяет получить осадок железа на катоде. Таким образом, данный метод можно применять для извлечения железа из растворов.
Кроме железа, с помощью электролиза раствора сульфата меди можно получать и другие металлы, например, никель, цинк и свинец. Для этого используются соответствующие металлические аноды, которые обеспечивают разложение раствора и осаждение соответствующего металла на катоде.
Электролиз раствора сульфата меди и другие металлы, получаемые этим способом, имеют широкое применение в различных отраслях промышленности. Этот метод является эффективным и экономически выгодным способом получения различных металлов.
Электролиз раствора сульфата меди и другие способы получения металлов
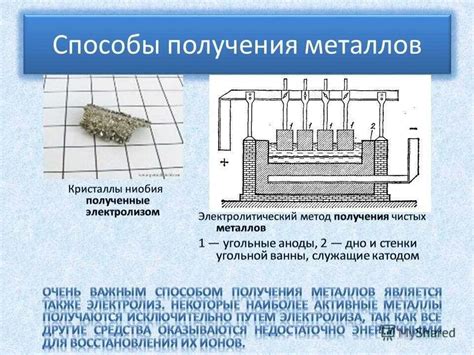
Электролиз растворов сульфата меди является одним из основных способов получения меди. В процессе электролиза раствора сульфата меди на аноде происходит реакция окисления меди, при которой образуется ион меди(II) и электроны. Ионы меди перемещаются в раствор и осаждаются на катоде, образуя медный металл.
Однако медь можно получить и другими способами. Например, медь можно получить методом обжига руды. При этом руда подвергается высокой температуре, что позволяет выделить медь в виде металла.
Другим способом получения меди является использование процесса цементации. При этом раствор медного соединения вступает в реакцию с активным металлом, таким как цинк или железо. Здесь медь осаждается на поверхности металла, а соединение меди с активным металлом превращается в медный металл.
Кроме меди, электролиз растворов также позволяет получать другие металлы. Например, электролизом раствора сульфата свинца можно получить свинец. При этом происходит окисление ионов свинца на аноде, а образовавшийся ион свинца перемещается в раствор и осаждается на катоде.
Таким образом, электролиз растворов сульфатов металлов — это эффективный способ получения различных металлов, включая медь и свинец.
Что такое электролиз и как он применяется для получения металлов?
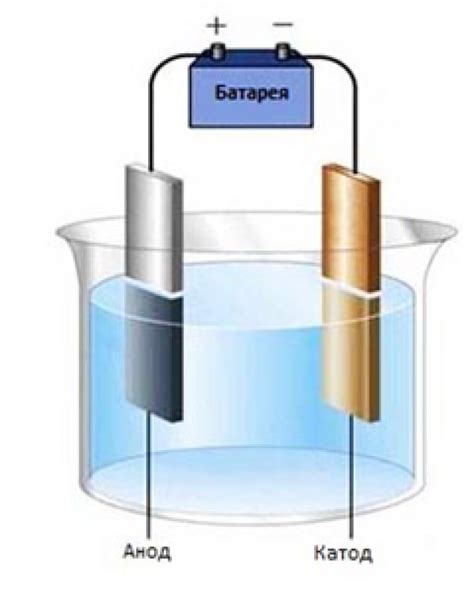
Электролиз – это процесс, при котором распадаются соединения под действием электрического тока. Он применяется для получения металлов из их растворов или расплавов. Электролиз может быть использован для получения различных металлов, включая медь, железо, никель и другие.
В процессе электролиза, вещество, которое содержит металлы, разлагается на положительно заряженные катионы металлов и отрицательно заряженные анионы других элементов. Катионы металлов притягиваются к отрицательному электроду – катоду, где они получают электроны и нейтрализуются, осаждаясь в виде металлического отложения.
Для проведения электролиза в раствор металла добавляют электролит – вещество, которое способствует проводимости тока. В случае получения меди из сульфата меди, в качестве электролита используется серная кислота или соль серной кислоты.
Электролиз применяется в различных отраслях промышленности, таких как производство металлов, химическая промышленность, электротехническая промышленность и другие. Он позволяет получать металлы высокой чистоты и с высокой эффективностью. Важно отметить, что электролиз является энергоемким процессом, требующим подведения электрического тока, поэтому его проведение требует значительных энергетических затрат.
Медь и ее процесс получения в растворе сульфата

Медь — это блестящий, красновато-желтый металл, который широко используется в различных отраслях промышленности, включая электротехнику, строительство и производство ювелирных изделий. Одним из способов получения меди является электролиз раствора сульфата меди.
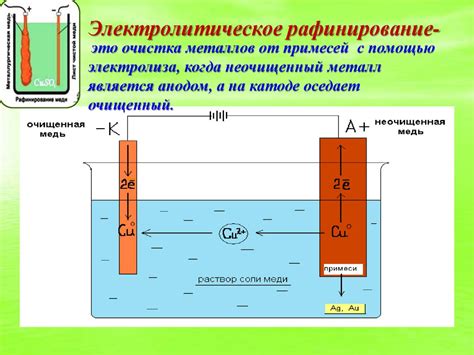
Процесс получения меди посредством электролиза раствора сульфата меди основан на использовании электролитической ячейки, состоящей из анода и катода, погруженных в раствор сульфата меди. Анодом служит положительно заряженная медная пластина, а катодом - отрицательно заряженная пластина из меди или другого металла. При подаче постоянного электрического тока через ячейку, ионы меди, Cу2+, перемещаются к катоду, где они получают электроны и восстанавливаются в нейтральную медь, которая осаждается на поверхности катода.
Процесс электролиза раствора сульфата меди обычно протекает в специальных электролизных ваннах, называемых электролизерами или сотами. Они имеют ряд особенностей, таких как наличие специальных агитаторов для перемешивания раствора, регулировка тока и напряжения, и системы для отдаления осажденной меди от катода.
Полученная медь в растворе сульфата может быть дальше декоративно оформлена или использована в качестве сырья для производства других металлических изделий. Электролиз раствора сульфата меди является одним из наиболее эффективных способов получения чистой меди с высокой степенью чистоты и качества.
Какие другие металлы можно получить методом электролиза?
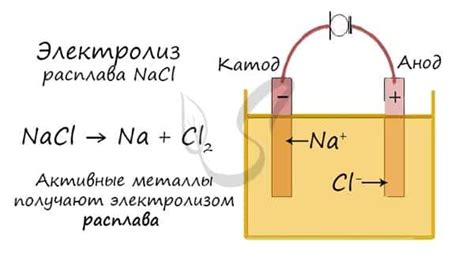
Помимо меди, электролизом раствора сульфата меди можно получить и другие металлы. Однако их список ограничен, так как не все металлы могут быть получены данным способом.
Наиболее распространенными металлами, получаемыми методом электролиза, являются цинк, никель и свинец. Они также могут быть получены из соответствующих растворов и реагентов.
Однако электролизом невозможно получить некоторые металлы, такие как золото, серебро и платина. Для получения этих драгоценных металлов применяют другие методы, например, химическое осаждение или плавление с использованием специальной технологии.
Также стоит отметить, что электролиз может быть использован для получения металлов из руд или рудных концентратов. Например, железо может быть получено электролизом раствора сульфата железа, алюминий - электролизом раствора алюминия.
В целом, электролиз - это эффективный и широко применяемый способ получения различных металлов, но ограниченный некоторыми физическими и химическими свойствами всех металлов.
Электролиз алюминиевых руд в производстве алюминия
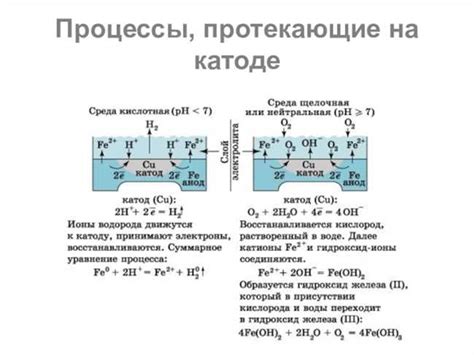
Алюминий является одним из самых важных металлов в современной промышленности. Для его производства широко используется метод электролиза алюминиевых руд.
Процесс начинается с получения алюминия из его основного источника – боксита. Боксит содержит оксиды алюминия, которые проходят обработку, чтобы получить чистый металл.
Для электролиза руды используют электролизные ванны, в которых анодом является анодное кислородное место, а катодом – расплавленный алюминий. Катодные пластины обычно изготавливают из углеродного материала.
Процесс электролиза основан на проведении постоянного электрического тока через ванну с растворенными рудами. При этом алюминий на катоде окисляется и превращается в ионы, которые перемещаются к аноду.
На аноде происходит обратная реакция – ионы алюминия восстанавливаются и осаждается кислород. Алюминий, полученный на катоде, затем сливают и перерабатывают в требуемую форму для дальнейшего использования.
Благодаря процессу электролиза алюминиевых руд, возможно массовое производство алюминия с высокой чистотой и эффективностью. Этот метод является ключевым для производства широкого спектра алюминиевых изделий, от компонентов авиации до упаковочной продукции.
Процесс электролиза для получения кобальта и никеля
Электролиз является одним из методов получения кобальта и никеля из соответствующих солей. Этот процесс основан на использовании электрического тока для разложения раствора электролита и получения металлического отложения на электродах.
Для процесса электролиза кобальтовых и никелевых солей используют электролитические ячейки, состоящие из анода и катода, которые являются проводящими электрическим током и позволяют осуществить электролиз. Анодом обычно служит металлическая пластина, покрытая оксидом кобальта или никеля, а катодом – металлическая пластина, на которую происходит осаждение кобальта или никеля.
Во время электролиза происходит разложение кобальтовых или никелевых солей на ионы кобальта или никеля и отрицательно заряженные ионы из соответствующего аниона. Под действием электрического тока ионы кобальта или никеля перемещаются к катоду, где происходит их осаждение в виде металла.
Электролиз позволяет получить чистые образцы кобальта и никеля, так как металл осаждается на катоде, а примеси остаются в растворе. Это делает электролиз одним из самых эффективных методов получения чистых металлов из их солей.
Полученные кобальт и никель могут быть использованы в различных областях промышленности, включая производство сталей, магнитов, катализаторов и других материалов.
Электролиз в качестве эффективного способа получения редких металлов

Электролиз – физический процесс, основанный на разложении веществ путем применения электрического тока. Этот метод широко применяется в производстве редких металлов, таких как титан, галлий, индий, вольфрам и др.
Для получения редких металлов при электролизе используют растворы, содержащие соединения данных металлов. Например, для получения титана используется раствор титанатана калия. При применении электролиза раствора с титановым ионом образуется титановое металлическое осаждение.
Процесс электролиза растворов редких металлов осуществляется в электролизере, в котором размещены электроды. Один из электродов (анод) служит для распада раствора металла, в то время как другой электрод (катод) используется для осаждения получаемого металла. При подаче постоянного электрического тока на электроды, ионы редких металлов перемещаются в растворе и осаждается на катоде.
Электролиз – эффективный метод получения редких металлов, так как позволяет получить их в высокой степени чистоты. Кроме того, этот метод имеет высокий уровень энергоэффективности. Электролиз также обладает высокой степенью контролируемости, что позволяет получить металлы требуемого качества.
Итак, электролиз является эффективным и широко используемым способом получения редких металлов, позволяя получить их высокой степени чистоты и контролируемости.
Вопрос-ответ

Что такое электролиз?
Электролиз - это процесс разложения вещества под воздействием электрического тока.
Какие металлы можно получить методом электролиза?
Методом электролиза можно получить различные металлы, включая медь, цинк, никель и другие.
Как происходит электролиз раствора сульфата меди?
При электролизе раствора сульфата меди на аноде происходит окисление меди и ее переход в ионы меди, а на катоде происходит восстановление ионов меди и их осаждение на поверхности катода.
Какие свойства имеет медь, получаемая методом электролиза?
Медь, получаемая методом электролиза раствора сульфата меди, обладает высокой степенью чистоты и является мягким и деформируемым металлом с хорошей электропроводностью.
В каких областях применяется медь, получаемая методом электролиза?
Медь, полученная методом электролиза, широко используется в электротехнике, электронике, строительстве, производстве монет и украшений, а также в других отраслях промышленности.
