Периодическая система химических элементов разделена на несколько групп и подгрупп, которые объединяют элементы схожих свойств. Одной из важных подгрупп являются побочные подгруппы металлов, которые находятся справа от главной группы металлов. В этих подгруппах находятся элементы, обладающие различными химическими и физическими свойствами, которые делают их полезными и необходимыми в различных областях науки и техники.
Первая побочная подгруппа металлов включает элементы атомными номерами от 21 до 30. Она включает такие металлы, как скандий, титан, ванадий, хром, марганец, железо, кобальт, никель и медь. Эти металлы широко используются в различных отраслях промышленности, таких как машиностроение, энергетика, химическая промышленность и другие.
Вторая побочная подгруппа металлов состоит из элементов с атомными номерами от 39 до 48. Она включает ихтимий, ренгений, кадмий, индий, олово, свинец и другие. Эти металлы обладают уникальными антикоррозионными и каталитическими свойствами, что делает их незаменимыми материалами для производства различных изделий и оборудования.
Третья побочная подгруппа металлов включает элементы с атомными номерами от 72 до 80. Она включает такие металлы, как гафний, тантал, вольфрам, рений и платина. Эти металлы отличаются высокой электропроводностью, прочностью и теплостойкостью, что делает их незаменимыми в производстве электроники, авиации, медицинского оборудования и других отраслях промышленности.
Металлы с побочными подгруппами в периодической системе химических элементов
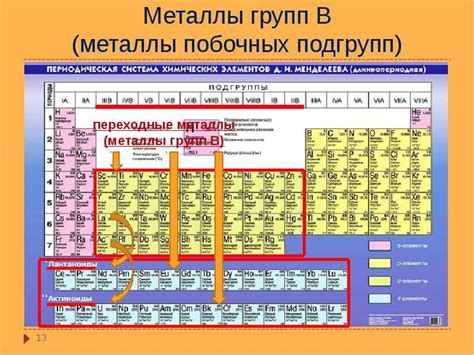
В периодической системе химических элементов есть несколько металлов, которые относятся к побочным подгруппам. Побочные подгруппы включают элементы, расположенные между основными группами 1 и 2, а также 13 и 18. Они представляют собой переходные элементы и имеют своеобразные свойства.
Одним из элементов с побочными подгруппами является медь (Cu). Она находится в побочной подгруппе 11, так называемых "монетных металлов". Медь имеет красивый блеск и отличается высокой проводимостью электрического тока. Она также используется в производстве различных материалов, включая электрические провода и монеты.
Еще одним металлом с побочной подгруппой является железо (Fe). Оно относится к побочной подгруппе 8, которая также называется "железом, марганцем и кобальтом". Железо является одним из самых распространенных элементов на Земле и используется в производстве стали и других металлических сплавов. Оно также играет важную роль в организме человека, участвуя в образовании красных кровяных клеток.
Алюминий (Al) - еще один металл с побочной подгруппой. Он находится в побочной подгруппе 13 и отличается легкостью и прочностью. Алюминий широко используется в производстве конструкций и упаковочных материалов, таких как алюминиевая фольга и пластиковые бутылки. Он также используется в авиационной и автомобильной промышленности.
Были описаны только несколько металлов с побочными подгруппами в периодической системе химических элементов. Каждый из них имеет свои уникальные свойства и находит широкое применение в различных отраслях промышленности и науки.
Щелочноземельные металлы
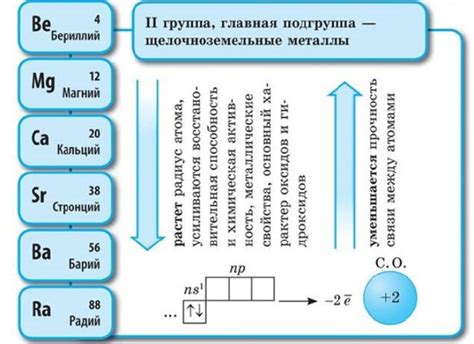
Щелочноземельные металлы – это группа элементов в периодической системе химических элементов, включающая бериллий, магний, кальций, стронций, барий и радий. Они расположены во второй группе и обладают общими химическими свойствами, связанными с их валентностью +2. Название "щелочноземельные" они получили из-за своей схожести с элементами из первой группы - щелочными металлами.
Щелочноземельные металлы являются легкими металлами с низкой плотностью. У них высокая температура плавления и кипения, а также низкое значение электроотрицательности. Они химически активны и реагируют с водой, кислородом и некоторыми другими веществами. Например, при контакте с водой они образуют щелочные гидроксиды и высвобождаются водород.
Эти металлы играют важную роль в различных областях. Бериллий используется в производстве сплавов для создания прочных и легких материалов. Магний является неотъемлемым компонентом алюминиевых сплавов, а также применяется в фармацевтической и строительной промышленности. Кальций широко используется в производстве стекла, цемента и многих других материалов.
Щелочноземельные металлы также имеют важное значение для организмов живого мира. Например, кальций играет ключевую роль в строительстве костей и зубов у животных и людей, а магний является необходимым элементом для работы нервной системы и множества ферментных реакций. Барий используется в медицине для создания рентгеноконтрастных веществ.
Постпереходные металлы

Постпереходные металлы – это группа элементов в периодической системе химических элементов, расположенная между переходными металлами и полупроводниками. Они обладают свойствами, связанными как с переходными металлами, так и с полупроводниками, и имеют разнообразные применения в промышленности и научных исследованиях.
К постпереходным металлам относятся элементы такие, как галлий, индий, олово и свинец. Они обладают различными химическими свойствами и являются хорошими проводниками тепла и электричества. Вследствие этого они широко используются в производстве электроники, солнечных батарей, специальных сплавов и покрытий.
Важным свойством постпереходных металлов является их низкая температура плавления, что делает их пригодными для использования в процессах пайки и легирования других материалов. Например, свинец, который является одним из постпереходных металлов, широко применяется при производстве паяльных припоев и аккумуляторов.
Постпереходные металлы также обладают интересными атомными и электронными свойствами. Некоторые из них образуют комплексы с органическими соединениями, что находит применение в катализе реакций и синтезе органических соединений. Кроме того, постпереходные металлы могут образовывать оксиды и соли, которые используются в производстве стекла и керамики.
Побочные металлы блока f
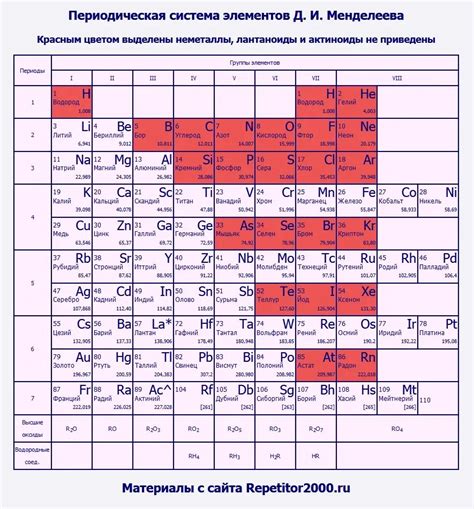
Побочные металлы блока f - это группа химических элементов, которые находятся между лантаноидами и актиноидами в периодической системе химических элементов. Они также известны как переходные металлы второго периода. В этой группе находятся такие элементы как скандий (Sc), иттрий (Y), лантан (La) и актиний (Ac).
Скандий - элемент с атомным номером 21. Он имеет серебристо-белый цвет и проявляет химические свойства типичные для переходных металлов. Скандий используется в производстве сплавов, а также в производстве ядерных реакторов и в биомедицинской отрасли.
Иттрий - элемент с атомным номером 39. Он является серебристо-белым металлом и обладает химической активностью, схожей с активностью алюминия. Иттрий используется в производстве сплавов, катализаторов, лазеров и в некоторых видовых стеклах.
Лантан - элемент с атомным номером 57. Он является серебристо-белым металлом и обладает химической активностью, схожей с активностью циркония. Лантан используется в производстве специальных стекол, а также в качестве катализатора в химической промышленности.
Актиний - элемент с атомным номером 89. Он является серебристо-белым металлом и обладает химической активностью, схожей с активностью тория. Актиний имеет несколько изотопов, некоторые из которых являются радиоактивными. Он используется в исследованиях в области нуклидной физики и радиационной терапии для лечения рака.
Активные супертяжелые металлы

Активные супертяжелые металлы – это группа элементов в периодической системе химических элементов, которые отличаются особыми свойствами и принадлежат к самым тяжелым элементам в природе. Они имеют атомные номера выше 104 и являются элементами с очень высокой атомной массой.
Одно из главных свойств активных супертяжелых металлов – это их нестабильность. Эти элементы обладают очень короткими временем полураспада, что делает их изучение и применение в экспериментах сложным и опасным. Однако, их нестабильность также вносит вклад в их активность и способность образовывать реакции с другими веществами.
Активные супертяжелые металлы имеют широкий спектр применений. Они используются в медицине для создания радиоактивных препаратов, а также в ядерной энергетике для производства плутония и других радиоактивных изотопов. Кроме того, они могут быть использованы в материалах для защиты от радиации и термоядерных реакций, а также в процессе синтеза новых элементов и соединений в лабораторных условиях.
Несмотря на свою крайнюю нестабильность и краткое время существования, активные супертяжелые металлы продолжают привлекать внимание исследователей и ученых. Их свойства и возможности все еще изучаются, и они могут играть важную роль в различных областях науки и технологий в будущем.
Ксенофорное металлорганическое соединение
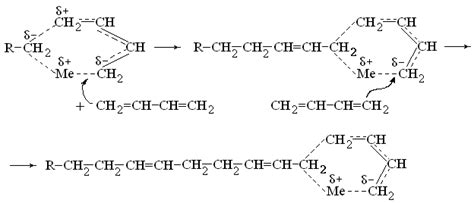
Ксенофорные металлорганические соединения представляют собой класс химических соединений, в которых присутствуют как минимум два металла, связанных с органическими лигандами. Данная подгруппа металлорганических соединений получила свое название из-за необычности и редкости встречаемости таких соединений в природе.
Металлорганические соединения, содержащие ксенофорные комплексы, обладают уникальными свойствами, такими как высокая устойчивость к окружающей среде и эффективность в катализе различных химических реакций. Они могут использоваться в различных областях, включая фармацевтику, электронику, сенсорику и солнечные элементы.
Ксенофорные металлорганические соединения являются объектом активных исследований в современной науке. Ученые исследуют их структуру и свойства с помощью различных методов анализа, включая рентгеноструктурный анализ, спектроскопические методы и компьютерное моделирование. Благодаря этому ученым удается получать новые данные о данном классе соединений и разрабатывать новые варианты их использования.
Ксенофорные металлорганические соединения имеют потенциал для применения в различных технологиях, таких как катализ, аккумуляторы, светодиоды и твердотельные лазеры. Благодаря своим уникальным свойствам, эти соединения могут стать основой для разработки новых материалов с улучшенными характеристиками и новых технологий, способных изменить многие сферы человеческой деятельности.
Вопрос-ответ

Какие металлы входят в побочные подгруппы в периодической системе химических элементов?
Побочные подгруппы металлов включают элементы, находящиеся вблизи переходной линии между блоками s и p в периодической системе химических элементов. К ним относятся металлы из групп 3-12 (включая лантаноиды и актиноиды).
Какие примеры можно привести побочных подгрупп металлов?
Примеры побочных подгрупп металлов включают такие элементы, как железо, никель, медь, цинк, алюминий, свинец, магний и другие. Они находятся в центральной части периодической системы химических элементов.
Чем побочные подгруппы металлов отличаются от других элементов?
Побочные подгруппы металлов отличаются своими химическими свойствами, включая способность образовывать ионы различного заряда и разнообразные соединения. Они также обладают хорошей термической и электрической проводимостью, высокой пластичностью и прочностью.
Какое значение имеют побочные подгруппы металлов в промышленности?
Побочные подгруппы металлов играют важную роль в промышленности. Например, железо и его сплавы широко используются в производстве стали, которая является основным строительным материалом. Медь применяется в электротехнике и электронике. Алюминий используется в автомобильной и авиационной промышленности и т.д.
