Металлы и неметаллы представляют собой две основные группы химических элементов, которые обладают существенными отличиями в своих физических и химических свойствах. Одним из ключевых отличий между ними является их молекулярное строение. Металлы характеризуются наличием свободно движущихся электронов в своей структуре, что придает им способность проводить электрический ток. Неметаллы, напротив, обладают строением, в котором электроны не могут свободно перемещаться, что делает их плохими проводниками тока.
Кроме молекулярного строения, ковкость является еще одним существенным отличием между металлами и неметаллами. Металлы, благодаря своей специфической структуре, обладают высокой степенью ковкости. Они могут подвергаться деформации без разрушения и обладают способностью формироваться в различные металлические изделия. Напротив, неметаллы характеризуются низкой ковкостью. Они обычно ломкими и не могут подвергаться деформации так же эластично, как металлы.
Понимание особенностей молекулярного строения и ковкости металлов и неметаллов играет важную роль в различных областях науки и технологии. Эти знания не только помогают в разработке новых материалов с улучшенными свойствами, но и полезны при изучении электрических и тепловых свойств веществ, а также в проектировании и производстве различных изделий.
Металлы и неметаллы

Металлы - это элементы химического периодического стола, обладающие высокой электропроводностью, блеском, жаростойкостью и свойством ковкости. Металлическое строение характеризуется регулярной кристаллической решеткой, в которой положительно заряженные ионы располагаются в межатомных промежутках свободно двигающимися электронами. Это обеспечивает электропроводность и способность металлов сформировать множество различных сплавов.
Примеры металлов: железо, алюминий, медь, олово и т. д. Они широко применяются в различных областях промышленности, таких как машиностроение, электротехника и строительство. Металлы обладают высокой термической и электрической проводимостью, что делает их незаменимыми в производстве проводников и электроники.
Неметаллы - это элементы, обладающие плохой электропроводностью, хрупкостью и различным строением. Неметаллические элементы могут образовывать молекулы, в которых атомы связаны ковалентными связями. Они могут быть газообразными, жидкими или твердыми при комнатной температуре и обладают разнообразными свойствами, такими как прозрачность, непроницаемость для электрического тока и высокая химическая активность.
Примеры неметаллов: кислород, углерод, сера, фосфор и др. Неметаллы широко используются в химической промышленности для производства различных соединений и материалов. Они также играют важную роль в биологических процессах и являются неотъемлемой частью органических соединений.
Различия в молекулярном строении
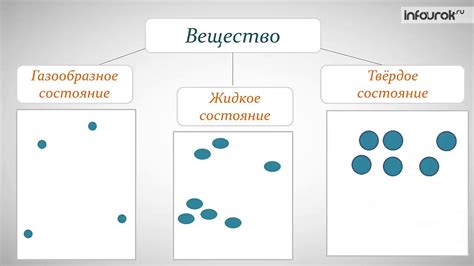
Металлы и неметаллы - две основные категории элементов, которые отличаются в своем молекулярном строении и химических свойствах. Металлы характеризуются наличием свободных электронов, что способствует их высокой проводимости электричества и тепла. Неметаллы, напротив, не обладают такой способностью и имеют высокую электроотрицательность.
Молекулярное строение металлов отличается от молекулярного строения неметаллов. У металлов атомы соединяются между собой особым образом - благодаря металлическим связям. В таких связях между атомами нет строгой упорядоченности, они образуют общие электронные облака, которые могут двигаться свободно по кристаллической решетке. Это делает металлы гибкими и формоизменяемыми.
Молекулярное строение неметаллов обычно представлено простыми или сложными молекулами, состоящими из нескольких атомов, связанных между собой ковалентными связями. В отличие от металлов, неметаллы имеют низкую электропроводность и являются хорошими изоляторами электричества и тепла.
Ковкость металлов определяется особым строением и упорядоченностью их атомов в кристаллической решетке. Это позволяет металлам быть деформированными без разрушения связей между атомами. Например, при давлении или ударе металлы могут быть легко изгибаемыми и принимать различные формы.
Неметаллы, в свою очередь, обычно обладают хрупкостью. Они имеют сложную кристаллическую решетку, в которой связи между атомами более крепкие и не позволяют легко деформироваться. Поэтому неметаллы обычно ломаются при малейшем воздействии силы.
Особенности ковкости металлов

Металлы обладают высокой ковкостью, что делает их идеальными материалами для различных инженерных конструкций. Ковкость определяет способность материала противостоять деформации без разрушения. В металлах это связано с их особенной структурой и способностью образовывать кристаллическую решетку.
Кристаллическая решетка металлов образуется за счет взаимодействия между атомами, образующими так называемые металлические связи. Эти связи характеризуются высокой механической прочностью и позволяют материалу выдерживать большие нагрузки без разрушения.
Ковкость металлов также связана с их способностью к пластической деформации. Под воздействием внешней силы металлы могут изменять свою форму, не теряя при этом своих свойств. Благодаря этому свойству металлы могут быть легко раскатаны, прокатаны, вытянуты и прочно сварены.
При обработке металлы подвергаются термической и механической обработке, что повышает их ковкость. Также важным фактором, влияющим на ковкость, является степень чистоты материала. Чистые металлы, не содержащие примесей и посторонних элементов, обладают более высокой ковкостью.
Таким образом, особенности ковкости металлов связаны с их кристаллической структурой, способностью к пластической деформации и механической прочностью металлических связей. Эти свойства позволяют металлам быть надежными и прочными материалами для использования в различных сферах промышленности и строительства.
Особенности ковкости неметаллов
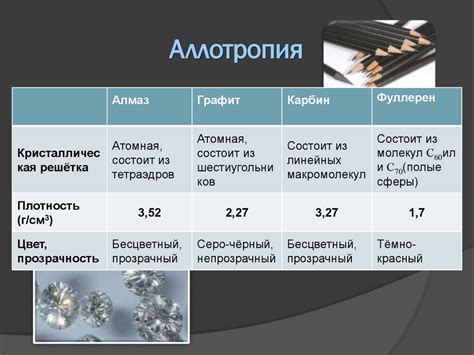
Ковкость – это способность материала оставаться прочным и изменять форму под воздействием внешних сил. В отличие от металлов, неметаллы обладают совершенно другими свойствами ковкости.
Одной из особенностей ковкости неметаллов является их хрупкость. Неметаллы обладают слабой прочностью и склонны к разрушению при механическом воздействии. Например, стекло легко разбивается при попадании в него сильного удара. Причина такой хрупкости заключается в строении молекул неметаллов, которые слабо связаны друг с другом.
Второй особенностью ковкости неметаллов является их неспособность образовывать деформацию под воздействием силы, как это делают металлы. Например, дерево не может быть вытянуто или спрессовано, так как его молекулы не могут сдвигаться друг относительно друга.
Также следует отметить, что неметаллы часто обладают более низкой температурой плавления, чем металлы. Поэтому при нагревании неметаллов они могут изменять свою форму или разрушаться.
Взаимодействия металлов с неметаллами

Металлы и неметаллы являются двумя основными классами элементов в периодической системе химических элементов. Взаимодействие между ними играет важную роль в различных процессах, включая образование соединений и реакции.
Металлы характеризуются высокой проводимостью электрического тока и тепла, а также обычно обладают блестящей поверхностью. Они образуют ионы положительного заряда, известные как катионы. Неметаллы, напротив, образуют ионы отрицательного заряда, называемые анионами. Они обычно обладают плохой проводимостью электрического тока и тепла.
- Одной из наиболее распространенных форм взаимодействия металлов с неметаллами является образование ионных соединений. В этом случае металл отдает электроны неметаллу, что приводит к образованию катионов и анионов.
- Другой формой взаимодействия является ковалентная связь, которая возникает, когда два атома, один из которых металл, делят пару электронов для образования молекулы. Это взаимодействие обычно происходит между неметаллами, но также может наблюдаться и в некоторых случаях с участием металлов.
- Кроме того, некоторые металлы могут вступать в химические реакции с неметаллами, образуя координационные соединения. В этих соединениях металл образует координационную связь с неметаллом через один или несколько его электронных пар.
Взаимодействия металлов с неметаллами имеют важное значение для понимания и применения в областях, таких как химия, материаловедение и электрохимия. Знание этих взаимодействий позволяет улучшить производство и использование различных материалов, а также разработать новые соединения и технологии.
Применение металлов

Металлы являются неотъемлемой частью нашей жизни и находят широкое применение во многих отраслях промышленности и производства.
Металлические материалы используются в строительстве для создания прочных конструкций. Благодаря своей высокой прочности, металлы позволяют строить здания, мосты и другие инфраструктурные объекты, которые выдерживают большие нагрузки и противостоят различным внешним воздействиям.
Металлы также широко применяются в автомобильной и авиационной промышленности. Они используются для создания двигателей, кузовов и других компонентов транспортных средств. Благодаря своим механическим и термическим свойствам, металлы обеспечивают надежность и безопасность в экстремальных условиях эксплуатации.
Металлы играют важную роль в энергетике. Они применяются в производстве электростанций, турбин, генераторов и других энергетических устройств. Металлы обладают хорошей проводимостью электричества и тепла, что делает их идеальными материалами для электрических и термических установок.
Металлы находят применение в медицине и фармацевтической промышленности. Они используются для создания медицинских инструментов, протезов, имплантатов и других медицинских изделий. Металлы обычно безопасны для организма, а их механические свойства позволяют им справляться с высокими нагрузками и длительным использованием.
В искусстве металлы применяются для создания скульптур, украшений и других художественных предметов. Их блеск, прочность и возможность обрабатывать их в различные формы делают металлы популярными материалами для реализации художественных задумок.
В космической отрасли металлы используются для создания спутников, ракет и других космических аппаратов. Они обладают необходимыми свойствами, чтобы выдержать высокие температуры и вакуум космического пространства, а также обеспечивают надежность и безопасность при запусках и полетах.
Кроме того, металлы применяются во множестве других отраслей промышленности, таких как производство электроники, здравоохранение, пищевая промышленность, химическая промышленность и т.д. Без металлов современная промышленность была бы немыслима, их уникальные свойства и многообразие способствуют развитию и прогрессу во многих отраслях.
Применение неметаллов

Углерод является одним из наиболее распространенных элементов в природе и имеет широкое применение. Он используется в производстве стали, применяется при производстве графитовых электродов, карбида кремния, а также для создания материалов с высокой прочностью, например, углеродного волокна и композитов на его основе. Углерод также применяется в электронной промышленности для создания полупроводниковых приборов.
Кислород играет важную роль в дыхании живых организмов и в процессах горения. Он применяется в медицине в качестве лекарственного газа для восполнения дефицита кислорода в организме. Кислород также используется в промышленности при сварке и резке металлов, а также в процессах окисления при производстве химических веществ и материалов.
Азот в основном применяется в удобрениях для повышения урожайности посевов. Кроме того, азот используется в производстве аммиака, который используется для производства удобрений и пластмасс. За счет своих инертных свойств, азот также применяется в промышленности для создания инертной атмосферы при хранении и транспортировке продуктов питания и легковоспламеняющихся веществ.
Фосфор применяется в производстве удобрений, так как является неотъемлемым компонентом многих растений. Также фосфор используется в производстве смазочных материалов, ядерного топлива и огнестойких материалов. Фосфорные соединения применяются в фармацевтической промышленности для создания медицинских препаратов и взрывчатых веществ.
Сера широко применяется в производстве резины, текстиля, бумаги и пластмасс. Ее соединения используются в производстве удобрений, вспомогательных химических веществ и в медицинских целях. Также сера используется в производстве огнетушителей и в косметической и парфюмерной промышленности.
Вопрос-ответ

Какое молекулярное строение характерно для металлов?
Металлы обладают кристаллической решеткой, состоящей из положительно заряженных ионов, окруженных облаком электронов, которые не принадлежат конкретному атому, а перемещаются свободно по решетке.
Какое молекулярное строение характерно для неметаллов?
Неметаллы образуют молекулы, состоящие из двух или более атомов, связанных ковалентной (электронной) связью. Эти связи создаются за счет обмена электронами.
Почему металлы обладают высокой ковкостью?
Металлическая ковкость обусловлена особенностями молекулярного строения металлов. Ионы и молекулы металлов свободно перемещаются по решетке, что делает металлы пластичными и способными к деформации без разрушения.
Почему неметаллы обладают низкой ковкостью?
Неметаллическая ковкость обусловлена ковалентной связью между атомами в молекулах неметаллов. Эта связь очень прочная и требует большого количества энергии для ее разрыва, что делает неметаллы хрупкими и неспособными к пластической деформации.
