Металлы - это вещества, которые обладают высокой электропроводностью, благодаря своей способности образовывать движущиеся заряженные частицы, такие как электроны. Однако, вопрос о том, образуют ли металлы двухатомные молекулы, остается открытым и является предметом научных исследований.
В отличие от неметаллов, которые образуют двухатомные молекулы, металлы имеют особую структуру, в которой ионы положительно заряженных металлов окружены морем свободных электронов. Именно эти свободные электроны отвечают за электропроводность металлов и их способность образовывать движущиеся заряды.
Однако, существуют исключения. Некоторые металлы, такие как молекулярные металлы, могут образовывать двухатомные молекулы. Например, водород может формировать молекулу H2, а молекулы металлов особого типа, такие как медь, серебро и золото, могут образовывать молекулы с атомами этих металлов.
Однако, большинство металлов имеют металлическую связь, в которой электроны можно считать общими для всех атомов металла. Такой подход позволяет объяснить такие свойства металлов, как высокая теплопроводность и электропроводность.
Таким образом, большинство металлов не образуют двухатомные молекулы в обычных условиях. Однако, молекулярные металлы и некоторые особые типы металлов могут образовывать двухатомные молекулы, благодаря наличию особой структуры и свойств.
Металлы и их молекулы

Металлы - это элементы, которые характеризуются блестящей поверхностью, хорошей электропроводностью и высокой пластичностью. Но могут ли металлы образовывать двухатомные молекулы? Давайте разберемся.
Обычно металлы не образуют молекулы, как это делают неметаллы, так как их атомы обладают свободными электронами, которые легко перемещаются между атомами. Вместо этого, металлы формируют кристаллическую решетку, где атомы упорядочены и образуют гигантские структуры.
Однако некоторые молекулярные металлы, такие как ртуть, имеют двухатомную структуру. В молекуле ртути один атом связан с другим через ковалентную связь. Такие металлы, которые образуют двухатомные молекулы, называются диатомными металлами.
Диатомные молекулы металлов обладают некоторыми уникальными свойствами. Например, ртуть является единственным металлом, который находится в жидком состоянии при комнатной температуре. Кроме того, диатомные металлы обычно имеют низкую температуру кипения и высокую парообразность.
Значительная часть металлов образует гигантские кристаллические решетки или аморфные структуры. Эти металлы имеют высокую плотность и твердые свойства. В кристаллической решетке каждый атом металла окружен соседними атомами и удерживается в плотной структуре.
В заключение, металлы обычно не образуют двухатомные молекулы, но некоторые из них, такие как ртуть, могут образовывать диатомные молекулы. Большинство металлов формируют гигантские кристаллические решетки или аморфные структуры, благодаря которым они обладают своими специфическими свойствами.
Новые открытия в химии

Современная наука постоянно привносит новые открытия в химическую область, расширяя наши знания о молекулярной структуре и взаимодействии веществ. Одним из таких открытий является возможность образования двухатомных молекул металлами.
Металлы обычно считаются ионными соединениями, где отрицательные ионы образуют решетку вокруг положительных металлических ионов. Однако последние исследования показали, что некоторые металлы могут образовывать двухатомные молекулы, подобно неметаллам.
Это открытие имеет огромное значение для дальнейшего развития химии и позволяет расширить нашу понятия о молекулярных связях. Оно также открывает новые возможности для использования металлов в различных областях, таких как катализ и электрохимия.
Для подтверждения возможности образования двухатомных молекул металлами проведены многочисленные эксперименты и теоретические исследования. Эти исследования доказали, что металлы, такие как медь, железо и палладий, способны образовывать двухатомные молекулы с другими элементами, создавая новые соединения и структуры.
Такие открытия в химии открывают новые перспективы в разработке новых материалов и технологий, которые могут быть использованы в различных областях науки и промышленности. Благодаря постоянным исследованиям и открытиям, мы можем лучше понять и контролировать свойства веществ, что помогает нам совершенствовать их применение в различных областях нашей жизни.
Образование молекул металлами
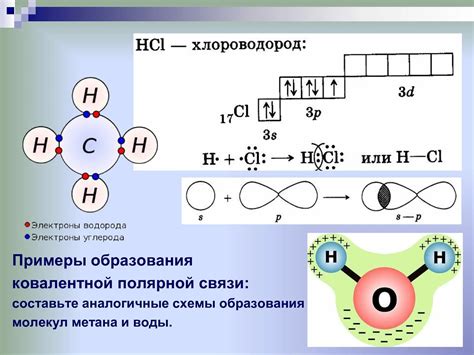
Металлы – это элементы, обладающие хорошей электропроводностью и блестящей поверхностью. Обычно металлы формируют кристаллическую решетку, в которой атомы располагаются регулярно. Однако, образуют ли металлы двухатомные молекулы?
В отличие от неметаллов, которые образуют молекулы, состоящие из двух или более атомов, металлы редко образуют двухатомные молекулы. Вместо этого, металлы образуют кристаллические структуры, где атомы металла равноудалены друг от друга и тесно упакованы.
Однако, существует небольшое количество металлов, таких как ртуть и цезий, которые образуют двухатомные молекулы в определенных условиях. Например, в жидком состоянии ртуть образует молекулы Hg2, состоящие из двух атомов ртути, связанных между собой.
В целом, металлы склонны образовывать металлические связи, при которых электроны общуются как свободные электроны и перемещаются вдоль кристаллической решетки металла. Это делает металлы отличными электропроводниками, однако не способствует образованию двухатомных молекул.
Структура двухатомных молекул

Двухатомные молекулы состоят из двух атомов, которые образуют химическую связь между собой. Структура таких молекул может быть различной в зависимости от типа атомов и типа химической связи между ними.
В большинстве случаев двухатомные молекулы образуются из атомов одного химического элемента. Например, молекула кислорода (O2) состоит из двух атомов кислорода. Также существуют двухатомные молекулы, образованные из атомов разных элементов, например, молекула воды (H2O) состоит из атома кислорода и двух атомов водорода.
Структура двухатомной молекулы определяется типом химической связи между атомами. В некоторых случаях атомы могут образовывать сильную и устойчивую ковалентную связь, при которой электроны общие для обоих атомов. В других случаях могут образоваться слабые связи, такие как водородные связи или ионные связи.
Молекулы, образованные из двух атомов, обычно имеют простую и симметричную структуру. Например, молекула кислорода (O2) имеет линейную структуру, где два атома кислорода находятся на одной линии. Молекула воды (H2O), в свою очередь, имеет угловую структуру, где атомы кислорода и водорода расположены под углом друг к другу.
Выводя итог, структура двухатомных молекул может быть различной в зависимости от типа атомов и химической связи, но в большинстве случаев она проста и симметрична.
Химические связи и металлы

Металлы являются основным классом элементов в периодической таблице. Они обладают особыми химическими свойствами, в том числе способностью образовывать ионные и металлические связи.
Металлическая связь является основной формой химической связи в металлах. Она основывается на обмене свободными электронами между атомами металла. Эти электроны, которые называются "электронами проводимости", образуют облако вокруг положительно заряженных ионов металла.
Металлическая связь обеспечивает высокую электропроводность и теплопроводность металлов. Она также позволяет металлам быть пластичными и прочными, так как электроны проводимости обеспечивают их подвижность и способность к деформации без разрыва связей.
В отличие от других элементов, металлы обычно не образуют двухатомных молекул, так как их атомы сливаются в трехмерные кристаллические решетки. В этих решетках атомы металла расположены в регулярном порядке и образуют бесконечные структуры.
Тем не менее, некоторые металлы могут образовывать комплексные соединения, в которых металл связан с другими молекулами или ионами. Эти соединения имеют сложные структуры и не являются двухатомными молекулами.
Свойства и реактивность металлических молекул
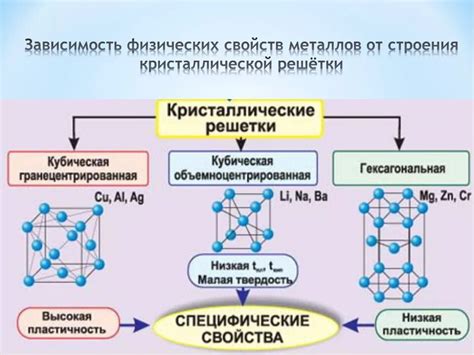
Металлы обычно не образуют двухатомные молекулы, так как их атомы, обладающие малым электроотрицательностью, обычно образуют макрокристаллическую структуру. Однако некоторые металлы, такие как медь и серебро, могут образовывать димеры или парные молекулы в испаренном состоянии или в некоторых соединениях.
Металлические молекулы обычно обладают высоким теплопроводимостью и электропроводностью, так как свободные электроны могут свободно двигаться в структуре металла. Более того, металлы обычно имеют высокую плотность, тугоплавкость и хорошую прочность, что делает их полезными для использования в различных промышленных и строительных процессах.
Реактивность металлических молекул зависит от их реакции с окружающей средой. Некоторые металлы, такие как железо, склонны к окислительным реакциям, где они теряют электроны и образуют окислительные соединения. Другие металлы, такие как никель и медь, могут проявлять свою реактивность в качестве катализаторов в различных химических реакциях.
Металлические молекулы также могут образовывать соединения с неметаллами, такими как кислород, сера или азот. Эти соединения, называемые металлическими оксидами, сульфидами или нитридами, имеют различные свойства и используются в различных областях промышленности, включая производство стекла, керамики, электроники и многих других.
Роль металлов в биологических системах

Металлы играют важную роль в биологических системах, выполняя различные функции и принимая участие во многих жизненно важных процессах.
Одной из самых важных функций металлов в биологии является их участие в структуре и активности белков. Металлы, такие как железо, цинк, медь и магний, могут быть неотъемлемой частью активных центров белков, обеспечивая их каталитическую активность. Например, гемоглобин, содержащий железо, является основной молекулой, отвечающей за транспорт кислорода в организме.
Металлы также играют роль в поддержании структурной целостности клеток. Например, кальций участвует в формировании костей и зубов, а натрий и калий контролируют баланс воды в клетках и помогают поддерживать нормальное давление внутриклеточного пространства.
Еще одной важной ролью металлов является их участие в сигнальных путях и регуляции генной экспрессии. Металлы могут взаимодействовать с белками-рецепторами, активируя или инактивируя определенные сигнальные пути. Также они могут влиять на активность генов, контролируя их экспрессию.
Кроме того, межклеточные сигналы и нейротрансмиттеры также могут быть связаны с металлами. Например, цинк и магний участвуют в регуляции нервных импульсов и передаче сигналов между нервными клетками.
Таким образом, металлы играют значительную роль в биологических системах и необходимы для поддержания нормальной функции организма. Их участие в структуре и активности белков, регуляции генной экспрессии и поддержании структурной целостности клеток делает их неотъемлемой частью живых организмов.
Вопрос-ответ

Могут ли металлы образовывать двухатомные молекулы?
Нет, металлы обычно не образуют двухатомные молекулы. Они образуют металлическую структуру, состоящую из положительных ионов, окруженных электронным облаком.
Почему металлы не могут образовывать двухатомные молекулы?
Металлы обладают свободными донорными электронами, которые способны образовывать металлические связи с другими атомами металла. Это делает невозможным образование двухатомных молекул, так как межатомные связи образуются только между неметаллическими элементами.
Могут ли металлы образовывать молекулы?
Нет, металлы обычно не образуют молекулы, так как металлические связи возникают между атомами металла и не требуют образования отдельных молекул. Вместо этого, металлы образуют кристаллическую решетку, состоящую из положительных ионов, окруженных общим электронным облаком.
Есть ли исключения, когда металлы могут образовывать двухатомные молекулы?
Возможны некоторые исключения, когда металлы могут образовывать двухатомные молекулы. Например, некоторые комплексные соединения металлов, такие как диоксид кислорода (О2) и диазот молекула (N2), образуются между атомами металлов и неметаллами. Однако это относится к особым случаям и не является типичным для большинства металлов.
Как объясняется невозможность образования двухатомных молекул у металлов?
Образование двухатомных молекул требует наличия ковалентной связи, которая возникает между неметаллическими элементами. Металлы, в свою очередь, обладают особой структурой, в которой атомы металла образуют кристаллическую решетку и не образуют отдельных молекул. Это связано с наличием свободных донорных электронов, которые образуют металлические связи между атомами металла.
