Металлы и неметаллы – это две основные категории химических элементов, которые в значительной степени определяют их физические и химические свойства. Металлы обладают рядом характеристик, которые отличают их от неметаллов, и наоборот. Различия между ними связаны с их строением атомов, межатомными связями и их влиянием на электронную структуру вещества.
В основном, металлы отличаются от неметаллов своей способностью проводить электричество и тепло, высокой пластичностью и степенью блеска. У них часто высокие температуры плавления и кипения, и они обычно имеют множество положительных окислительных состояний. Металлы также обычно формируют ионные соединения, где они выступают в качестве катионов.
Неметаллы, в свою очередь, имеют другой набор свойств. Они обычно хорошо изолируют электричество и тепло, являются хрупкими и не обладают блеском. Неметаллы имеют низкие температуры плавления и кипения, обычно образуют отрицательные окислительные состояния и часто выступают в качестве анионов в ионных соединениях.
Различия между металлами и неметаллами

Металлы и неметаллы - две основные категории химических элементов, которые имеют существенные различия в своих физических и химических свойствах.
Во-первых, металлы обладают хорошей теплопроводностью и электропроводностью, в то время как неметаллы обычно являются плохими проводниками и не обладают такими свойствами. Это связано с различиями в электронной структуре атомов: металлы имеют малое количество валентных электронов, что облегчает передачу тепла и электричества, в то время как у неметаллов количество валентных электронов больше, и они образуют ковалентные связи.
Во-вторых, металлы обычно обладают металлическим блеском, а неметаллы - матовой поверхностью. Это связано с различиями в рассеянии света атомами: у металлов свет рассеивается электронами свободного энергетического уровня, что создает блеск, в то время как у неметаллов свет рассеивается сложной структурой атома, что создает матовую поверхность.
Кроме того, металлы обычно обладают высокой пластичностью и эластичностью, то есть они легко поддаются деформации и могут вернуться к своей исходной форме без разрушения. Неметаллы, напротив, обычно хрупкие и ломк
Физическое состояние

Металлы и неметаллы отличаются физическим состоянием при комнатной температуре. В основном, металлы представлены в твердом состоянии, хотя есть и исключения, например, ртуть, которая находится в жидком состоянии при комнатной температуре. Неметаллы, в свою очередь, могут находиться в разных агрегатных состояниях. Некоторые неметаллы, такие как кислород и азот, представлены в газообразном состоянии. Однако, большинство неметаллов находятся в твердом состоянии, например, уголь и сера.
Также, стоит отметить, что металлы обладают высокой плавкостью и кипения, в отличие от неметаллов, у которых эти значения обычно ниже. Например, железо имеет высокую плавкость и кипение при 1535 градусах Цельсия и 2750 градусах Цельсия соответственно. В то же время, сера имеет плавкость при 115 градусах Цельсия и кипение при 444 градуса Цельсия.
Прочность и твердость также являются характеристиками, которые разделяют металлы и неметаллы. Металлы, как правило, обладают высокой прочностью и твердостью, что позволяет использовать их в различных областях, включая строительство и производство машин. Неметаллы, в свою очередь, обычно менее прочны и менее тверды. Например, аллюминий, который является металлом, имеет высокую прочность и твердость, в то время как сера, являющаяся неметаллом, имеет низкую прочность и твердость.
Различия в физическом состоянии металлов и неметаллов влияют на их свойства и применение в различных отраслях науки и техники. Знание о физических характеристиках металлов и неметаллов позволяет ученым и инженерам использовать их оптимально и максимально эффективно в различных областях деятельности.
Электропроводность

Электропроводность - это способность материала проводить электрический ток. Данный параметр является одним из ключевых при разделении веществ на металлы и неметаллы.
Металлы обладают высокой электропроводностью благодаря своей уникальной структуре. Электроны в металлах образуют свободные электроны, которые могут свободно передвигаться по всей структуре материала. Это позволяет металлам эффективно проводить электрический ток и является причиной их хорошей проводимости.
Неметаллы, в отличие от металлов, обладают низкой электропроводностью или даже являются изоляторами. Это связано с их строением - неметаллы образуют ковалентные связи, в которых электроны плотно связаны с атомами и не могут свободно перемещаться. В результате неметаллы не могут проводить электрический ток так эффективно, как металлы.
Важно отметить, что существуют также полупроводники, которые обладают промежуточной электропроводностью. Полупроводники имеют структуру, в которой частично есть свободные электроны, но их количество недостаточно для полноценной проводимости. Однако при наличии дополнительной энергии (например, при изменении температуры или добавления примесей) полупроводники могут стать лучшими проводниками.
Теплопроводность
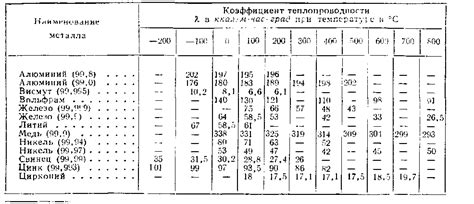
Теплопроводность — это свойство материалов передавать тепло. Она определяет способность вещества проводить тепловую энергию от области с более высокой температурой к области с более низкой температурой.
Металлы обладают высокой теплопроводностью благодаря свободным электронам, которые могут свободно перемещаться внутри кристаллической решетки. Это позволяет быстро и эффективно передавать тепло по всему объему материала. Так, например, алюминий и медь являются отличными теплопроводными материалами и широко используются в промышленности.
Неметаллы, в свою очередь, обычно обладают низкой теплопроводностью. У них отсутствуют свободные электроны, и тепловая энергия передается через колебания атомов или молекул. Это замедляет процесс передачи тепла и делает неметаллы менее эффективными в этом отношении. Например, дерево или пластик обычно являются плохими теплопроводниками.
Однако, есть и неметаллы, такие как алмаз, которые обладают высокой теплопроводностью благодаря своей кристаллической структуре. В случае алмаза, его высокая теплопроводность связана с тем, что энергия в нем передается через кристаллическую решетку, а не через свободные электроны, как в металлах.
Химическая активность
Химическая активность является одной из основных характеристик, разделяющих металлы и неметаллы. Металлы обладают большей химической активностью по сравнению с неметаллами. Они способны образовывать соединения с кислородом, образовывать ионы и подвергаться реакциям с другими веществами.
Неметаллы, напротив, имеют меньшую химическую активность и обычно образуют ковалентные соединения. Они могут образовывать связи с другими неметаллами или с металлами, но не реагируют с кислородом так же интенсивно, как металлы.
Химическая активность металлов обусловлена их способностью отдавать электроны во время химических реакций. Электроны играют важную роль в стабильности соединений, поэтому металлы с легкостью образуют ионы положительной валентности, что позволяет им вступать в различные химические реакции.
В то время как неметаллы имеют большую аффинность к электронам и кислороду. Это позволяет им образовывать отрицательные ионы и вступать в реакции с металлами и другими неметаллами.
Способность к образованию ионов

Металлы обладают способностью образовывать положительно заряженные ионы (катионы).
В металлах, внешний электронный слой состоит из слабо связанных электронов, которые легко отдаются другим элементам. Когда металл реагирует с другим веществом, электроны из внешнего слоя передаются другому элементу, образуя положительно заряженный ион металла.
Например, натрий (Na) в реакции с хлором (Cl) образует ион натрия Na+ и ион хлора Cl-. В этом случае натрий отдаёт свой один электрон, что приводит к образованию положительно заряженного иона Na+.
Неметаллы, напротив, образуют отрицательно заряженные ионы (анионы).
В неметаллах, внешний электронный слой обычно содержит пространство для приема электронов, что позволяет им образовывать отрицательно заряженные ионы. Когда неметалл реагирует с другим веществом, он принимает электроны от другого элемента, образуя отрицательно заряженный ион неметалла.
Например, кислород (O) в реакции с водородом (H) образует ион кислорода O2- и ион водорода H+. В этом случае кислород принимает два электрона от водорода, что приводит к образованию отрицательно заряженного иона O2-.
Свойства соединений

Свойства соединений зависят от их состава и структуры. Одним из основных химических свойств соединений является их реакционная способность. Соединения могут проявлять активность при взаимодействии с другими веществами, образуя новые соединения.
Соединения также могут обладать специфическими физическими свойствами, такими как плотность, температура плавления и кипения, электропроводность и т.д. Эти свойства зависят от типа соединения, его состава атомов и образующих его химических связей.
Одна из важнейших характеристик соединений - их растворимость. Растворимость определяет, насколько соединение может раствориться в данном растворителе при определенных условиях. Растворимость может зависеть от ряда факторов, включая температуру, давление и концентрацию раствора.
Кроме того, многие соединения обладают специфическими химическими свойствами, например, кислотность или щелочность. Кислоты обладают способностью отдавать протоны, а щелочи - принимать их. Эти свойства определяются наличием определенных химических групп в структуре соединений.
Свойства соединений могут быть использованы для их идентификации и классификации. По типу химических связей и химическим свойствам соединений выделяют различные классы веществ, такие как соли, кислоты, основания и т.д. Это позволяет более точно описывать их химические свойства и применение в различных отраслях науки и технологий.
Вопрос-ответ

В чем отличие металлов от неметаллов?
Металлы и неметаллы отличаются по ряду химических свойств. Металлы обладают хорошей электропроводностью, металлическим блеском, малой твердостью, и могут быть деформированы без разрушения. Неметаллы, напротив, не проводят электричество, обладают различными цветами и текстурами, и обычно твёрды.
Какие еще свойства разделяют металлы и неметаллы?
Кроме указанных ранее свойств, металлы обладают высокой тепло- и электропроводностью, высокой пластичностью и термостабильностью. Металлы также имеют металлический блеск. Неметаллы, наоборот, имеют низкую плотность, плохую тепло- и электропроводность, и не имеют металлического блеска.
Какие элементы являются металлами, а какие неметаллами?
К неметаллам относятся водород, гелий, углерод, кислород, азот, фосфор, сера, селен, йод и другие элементы. К металлам относятся железо, медь, золото, калий, натрий, магний, свинец и другие элементы.
Какие соединения характерны для металлов и неметаллов?
Металлы образуют ионы положительного заряда, обычно окислители, такие как оксиды, гидроксиды и соли. Неметаллы обычно образуют ионы отрицательного заряда, обычно вещества, имеющие эффект восстановления, такие как галогениды, сульфиды и оксиды.
