Взаимодействие металлов с хлором является одной из важнейших химических реакций, которая имеет широкое применение в различных отраслях промышленности и науки. Хлор – это химический элемент с атомным номером 17, принадлежащий к галогенам. Он обладает сильным окислительным действием и может вступать в реакцию с различными металлами.
При взаимодействии металлов с хлором происходит образование металлического хлорида. Это ионное соединение, состоящее из положительно заряженного иона металла и отрицательно заряженного иона хлора. В зависимости от конкретных условий реакции и свойств металла, металлический хлорид может образовываться в различных структурах и фазовых состояниях.
Взаимодействие металлов с хлором может протекать при различных температурах и давлениях. Некоторые металлы мгновенно реагируют с хлором при комнатной температуре, образуя интенсивно горящие ярко-желтые пламя и облака дыма. Другие металлы могут взаимодействовать с хлором только при нагревании до высоких температур.
Что такое хлор?

Хлор — это химический элемент с атомным номером 17 и символом Cl в периодической таблице. Он относится к группе галогенов и является недоразделенным, ядовитым газом в нормальных условиях.
Хлор имеет ярко-желтый цвет и неприятный запах, похожий на запах противогаза. Он обладает сильным окислительным действием и легко реагирует с многими другими элементами, образуя соединения. Хлор обычно выпускается в виде газа, но может также быть представлен в виде жидкости или твердого вещества в зависимости от условий.
Хлор широко используется в промышленности и быту. Он используется для очистки воды, создания пестицидов и удобрений, производства резины, пластика, красителей и многих других продуктов. Хорошо известными соединениями хлора являются хлорид натрия (поваренная соль) и хлор известной зеленой жидкости, называемой хлороформом.
Металлы и хлор: что нужно знать?

Процесс взаимодействия металлов с хлором
Взаимодействие металлов с хлором является одним из основных химических процессов, которые можно встретить в ежедневной жизни. При взаимодействии хлора с металлами происходит образование соединений, называемых хлоридами.
Химические свойства хлора
Хлор - это химический элемент, который имеет высокую реакционную способность. Он обладает сильным окислительным свойством и способен взаимодействовать с большинством металлов. Хлор обычно проявляется в виде газа желто-зеленого цвета.
Главные виды хлоридов
Существует множество различных хлоридов, образующихся при взаимодействии хлора с металлами. Некоторые из них имеют важное значение для промышленности и научных исследований. Например, хлорид натрия (NaCl) - это обычная соль, которая используется в пищевой промышленности и в быту. Хлорид цинка (ZnCl2) используется в гальванической отрасли и производстве лаков и красок.
Применение хлоридов
Хлориды имеют широкое применение. Они используются в различных отраслях промышленности, включая производство пищевых продуктов, фармацевтическую промышленность, металлургию и др. Они также используются в химических лабораториях и научных исследованиях для проведения различных экспериментов.
Особенности взаимодействия некоторых металлов и хлора
Взаимодействие хлора с некоторыми металлами может быть высокоэнергетичным процессом. Например, при взаимодействии алюминия с хлором возникает интенсивное разрушение металла и выделение большого количества энергии в виде тепла и света. Это явление может использоваться в промышленности в виде реактивов, а также в пиротехнике для создания огней и взрывов.
Реакции металлов с хлором

Взаимодействие металлов с хлором является одной из самых распространенных и изучаемых химических реакций. Хлор полагается к галогенам и обладает сильной окислительной способностью, что позволяет ему реагировать с многими металлами. Эти реакции могут быть разнообразными и включать образование солей или хлоридов.
Ряд металлов реагируют с хлором при нагревании до образования хлоридов. Например, натрий сильно реагирует с хлором, образуя хлорид натрия (NaCl). Процесс сопровождается выделением большого количества тепла и является экзотермическим. Такие реакции обычно протекают очень быстро и с большими объемами поглощаемого хлора.
- Магний также активно реагирует с хлором, образуя хлорид магния (MgCl2). Реакция происходит по аналогии с натрием, но требует большего количества энергии.
- Алюминий, быть металлом главной подгруппы III, реагирует с хлором при нагревании, образуя хлорид алюминия (AlCl3). Этот продукт обычно образует кристаллы благородно-белого цвета.
- Железо также способно реагировать с хлором, формируя несколько хлоридов, таких как хлорид железа (FeCl2) и хлорид железа (FeCl3). Реакционная способность железа с хлором зависит от степени окисления элемента.
Некоторые реакции металлов с хлором можно использовать в промышленности для получения важных химических соединений, таких как соли и хлориды, которые могут использоваться в различных отраслях, включая производство лекарств, пластиков и других химических веществ.
Как образуются хлориды металлов?

Хлориды металлов образуются в результате реакции металла с хлором. В химическом реагировании атомы металла отдают свои электроны хлору, который становится отрицательно заряженным и образует ионы хлорида. Металл, в свою очередь, становится положительно заряженным и образует ионы металла.
Формирующиеся ионы металла и хлорида образуют кристаллическую решетку, в которой ионы металла и ионы хлорида располагаются в определенном порядке. В результате этого образуется кристаллический хлорид металла.
Химические свойства хлорида металла определяются свойствами металла и степенью его взаимодействия с хлором. Некоторые хлориды металлов обладают специфическими свойствами, такими как высокая степень растворимости в воде или способность образовывать комплексные соединения с другими веществами.
Оксидация металлов при контакте с хлором
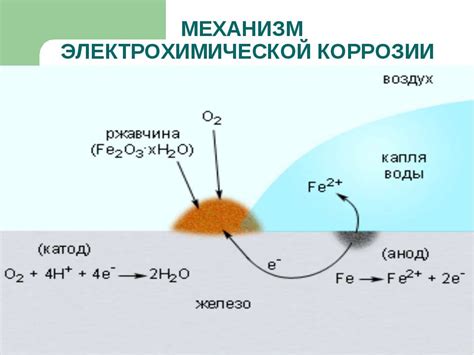
Оксидация металлов – это процесс, при котором металлы вступают в химическую реакцию с кислородом или другими окислителями. Контакт с хлором, являющимся сильным окислителем, может привести к оксидации различных металлов.
Оксидация металлов с хлором происходит по реакции, в результате которой образуются хлориды металлов. Реакция может происходить как при нормальных условиях, так и при высокой температуре. Важно отметить, что разные металлы могут иметь различную скорость оксидации и образования хлоридов.
Одной из характерных реакций оксидации металлов при контакте с хлором является образование хлорида кальция (CaCl₂). Эта реакция происходит при нагревании металла кальция в присутствии хлора. В результате образуется белый кристаллический порошок, который представляет собой хлорид кальция.
Другим примером реакции оксидации металлов с хлором является образование хлорида железа (FeCl₃). Эта реакция происходит при нагревании железа в присутствии хлора. В результате образуется темно-коричневый порошок, представляющий собой хлорид железа.
Таким образом, оксидация металлов при контакте с хлором является важным процессом, который может приводить к образованию различных хлоридов металлов. Эти реакции имеют широкое применение в промышленности и научных исследованиях.
Хлор в промышленности
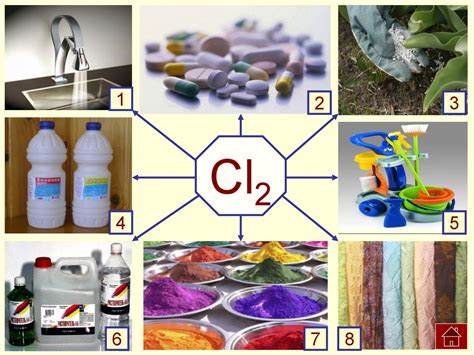
Хлор (Cl2) играет важную роль в промышленных процессах и имеет широкое применение. Он является одним из основных химических веществ, используемых во многих отраслях промышленности.
Одним из главных применений хлора является производство хлорированных органических соединений. Хлор используется для синтеза многих важных промышленных химических веществ, таких как пластмассы, резины, хлорэтил, хлороформ и др. Также хлор используется в процессе производства противогазов, антисептиков и дезинфицирующих средств.
Еще одной важной областью применения хлора в промышленности является производство хлора-щелочных продуктов. Хлор используется в процессе электролиза солей для получения щелочи, соды и хлора. Щелочные продукты, такие как гидроксид натрия (щелочь) и гидроксид калия, широко используются в химической, стекольной, пищевой, фармацевтической и других отраслях промышленности.
Хлор также применяется в очистке воды. Хлорированная вода используется для уничтожения бактерий и вирусов, обеззараживания питьевой воды, бассейнов и водоемов. Хлорирование является одним из наиболее эффективных методов дезинфекции воды и помогает предотвратить распространение инфекционных заболеваний.
В итоге, хлор является одним из важнейших веществ в промышленности, играющим ключевую роль в производстве химических соединений, щелочей и очистке воды. Его широкое применение делает его неотъемлемым компонентом многих отраслей промышленности.
Металлы в процессе хлорирования
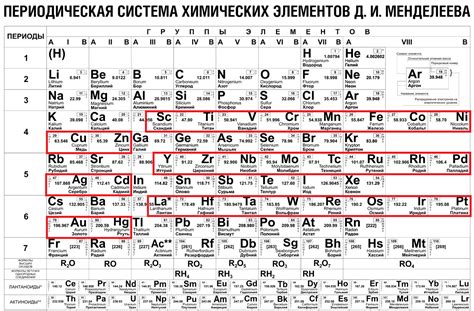
Хлорирование – это химическая реакция, при которой хлор добавляется к различным веществам для осуществления различных процессов. В контексте металлургии хлор может вступать во взаимодействие с различными металлами. В результате этой реакции образуются металлические хлориды, которые имеют важное промышленное применение.
Металлы в процессе хлорирования проявляют разную степень реакционной активности. Некоторые металлы, такие как натрий, калий и магний, реагируют с хлором довольно интенсивно и быстро. При этом образуются хлориды этих металлов, которые являются солью хлористой кислоты.
Другие металлы, например, алюминий и железо, могут реагировать с хлором только при нагревании до высоких температур. При этом происходит образование соответствующих металлических хлоридов. Такой процесс является важным при использовании хлорирования в промышленности.
Хлорирование металлов используется для получения металлических соединений с определенными химическими свойствами. Такие соединения могут применяться в различных отраслях промышленности, например, в производстве лакокрасочных материалов, полупроводниковой электроники, катализаторов и др.
Применение хлора и металлов в производстве
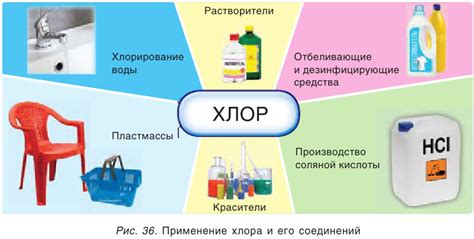
Хлор - один из наиболее распространенных химических элементов, который широко используется в различных отраслях промышленности. Он является основным компонентом для производства огромного количества химических соединений, а также используется в процессах очистки воды и дезинфекции.
Одним из важных применений хлора является его взаимодействие с металлами. В результате этого взаимодействия образуются различные хлориды металлов. Эти соединения широко применяются в различных отраслях промышленности, включая производство стали, алюминия, цинка и других металлических изделий.
Металлы, в свою очередь, также активно применяются в производстве. Они используются для создания различных изделий, начиная от мелких деталей и заканчивая крупной промышленной техникой. Металлические изделия обладают высокой прочностью и устойчивостью к внешним воздействиям, что делает их востребованными во многих отраслях промышленности.
В процессе взаимодействия металлов с хлором образуются хлориды металлов, которые находят широкое применение. Например, хлорид железа используется в производстве красителей, пигментов и других химических веществ. Хлорид натрия, или обычная кухонная соль, широко применяется в пищевой промышленности и домашнем хозяйстве. Хлорид кальция применяется для упрочнения бетона и в процессе консервации пищевых продуктов.
Таким образом, взаимодействие хлора с металлами играет важную роль в производстве различных продуктов и изделий. Оно позволяет получать разнообразные химические соединения, которые необходимы во многих отраслях промышленности.
Результаты взаимодействий металлов с хлором

Взаимодействие металлов с хлором является одним из важных процессов в химии. При этом образуются различные химические соединения, которые могут иметь различные свойства и применения.
Одним из наиболее известных результатов взаимодействия металлов с хлором является образование хлоридов металлов. Хлориды металлов представляют собой соли, состоящие из металлического и анионного компонентов. Они обладают характерными физическими и химическими свойствами и широко используются в различных отраслях промышленности.
При взаимодействии металлов с хлором может происходить образование хлоридов различной степени окисления. Например, у железа можно образовать хлориды FeCl2 и FeCl3. В зависимости от условий реакции, также могут возникать другие соединения, такие как комплексные хлориды или хлорид-оксиды.
Взаимодействие металлов с хлором может проводиться различными способами, например, путем прямого нагревания, восстановления хлорида металла или реакции с хлоридами других металлов. Также важным фактором является концентрация и температура среды, в которой происходит реакция.
Результаты взаимодействий металлов с хлором находят широкое применение в различных отраслях промышленности. Например, хлориды металлов могут использоваться в процессах электролиза, при производстве лекарственных препаратов, а также в качестве катализаторов в различных химических реакциях.
Вопрос-ответ

Зачем металлы взаимодействуют с хлором?
Металлы взаимодействуют с хлором, чтобы образовать хлориды металлов. Это происходит при нагревании металла в присутствии хлора или путем растворения металла в хлоридной кислоте. Взаимодействие металлов с хлором позволяет получать различные соединения, которые имеют широкое применение в различных отраслях промышленности.
Отличается ли взаимодействие металлов с хлором в зависимости от их химических свойств?
Да, взаимодействие металлов с хлором может различаться в зависимости от химических свойств металла. Некоторые металлы, такие как натрий или калий, реагируют с хлором с выделением большого количества энергии и образованием яркого пламени. Другие металлы, такие как железо или алюминий, взаимодействуют с хлором при нагревании, но не с такой яркостью и интенсивностью. Это связано с различием в реакционной способности и энергии взаимодействия различных металлов с хлором.
Какие соединения образуются при взаимодействии металлов с хлором?
При взаимодействии металлов с хлором образуются хлориды металлов. Например, при взаимодействии натрия с хлором образуется хлорид натрия (NaCl). При взаимодействии алюминия с хлором образуется хлорид алюминия (AlCl3). Реакция зависит от химических свойств конкретного металла, но в целом при взаимодействии металлов с хлором образуются стабильные хлориды, которые имеют различные применения в промышленности, медицине и других сферах.
