Металлы представляют собой особый класс веществ, обладающих рядом уникальных свойств. В основном они отличаются хорошей теплопроводностью и электропроводностью, а также высокой пластичностью и прочностью. Благодаря этим свойствам металлы широко используются в различных отраслях промышленности.
Оксиды, с другой стороны, являются химическими соединениями, в состав которых входит кислород и один или несколько элементов. Они могут образовываться как в результате воздействия кислорода на металлы, так и в процессе окисления неорганических веществ. Оксиды имеют разнообразные свойства, включая электропроводность, магнитные и каталитические свойства, а также способность быть кислотами или основаниями.
Существует несколько способов получения металлов и оксидов. Один из наиболее распространенных методов – это методы пирометаллургии, включающие восстановление металлов из их руд с использованием высоких температур и химических реакций. Еще один способ получения – это методы гидрометаллургии, основанные на использовании химических растворителей для разложения руды и выделения металлов.
Металлы: общие свойства и классификация

Металлы - это класс веществ, обладающих рядом характерных свойств. Они являются самыми распространенными материалами в нашей жизни и играют важную роль в различных областях техники, строительства и промышленности. Основные свойства металлов - высокая электропроводность, теплопроводность, пластичность и хорошая механическая прочность.
Металлы классифицируются по различным признакам. Одним из них является их химическая активность. Таким образом, металлы могут быть активными (например, натрий, калий) или пассивными (например, золото, платина). Активные металлы легко реагируют с окислителями, образуя оксиды, в то время как пассивные металлы обладают высокой устойчивостью к окислению.
Еще одним признаком классификации металлов является их плотность. Металлы могут быть легкими (алюминий, магний), средней плотности (железо, медь) или тяжелыми (свинец, золото). Плотность металла определяется его атомной структурой и массой единичного атома.
Также металлы могут быть классифицированы по своей химической структуре. Некоторые металлы образуют простые вещества, состоящие только из атомов данного металла (например, железо, алюминий). Другие металлы могут образовывать сплавы, состоящие из атомов двух или более различных металлов (например, бронза, нержавеющая сталь).
Все эти признаки помогают нам более полно и точно описывать различные металлы и их свойства, что в свою очередь позволяет использовать их в различных сферах нашей жизни.
Металлы: физические свойства и химическая активность

Металлы являются одной из основных групп веществ, имеющих высокую электропроводность, теплопроводность и металлический блеск. Они отличаются высокой пластичностью и стойкостью к деформациям. Металлы обладают различными физическими свойствами, такими как высокая плотность, твердость и точка плавления.
Химическая активность металлов обусловлена их электронной структурой. Металлы легко отдают электроны, образуя положительно заряженные ионы, которые обладают способностью образовывать ионы в различных степенях окисления. Это позволяет металлам участвовать в реакциях окисления и восстановления, образовывать соли и соединения с другими элементами.
Металлы также могут обладать способностью реагировать с кислородом воздуха, образуя оксиды. Оксиды металлов обычно являются основаниями и обладают щелочными свойствами. Однако, среди металлов найдутся и такие, оксиды которых проявляют кислотные свойства и способны взаимодействовать с щелочами.
Металлы могут быть получены различными способами, включая выделение из природных руд, электролиз, проведение химических реакций или сплавление. Полученные металлы имеют важное применение в различных отраслях промышленности, строительстве и технике благодаря своим уникальным физическим свойствам и химической активности.
Оксиды металлов: типы и основные свойства
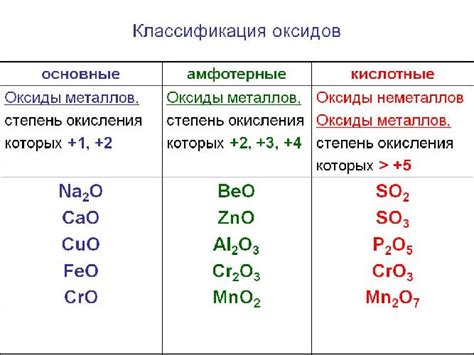
Оксиды металлов – это соединения, которые образуются в результате реакции металлов с кислородом. Они широко распространены в природе и имеют важное значение как промышленные и химические соединения. Оксиды металлов обладают различными свойствами, которые определяют их применение в различных отраслях промышленности.
Существует множество разновидностей оксидов металлов, каждый из которых имеет свои уникальные характеристики. Например, оксид железа (II) – FeO, оксид железа (III) – Fe2O3, оксид алюминия – Al2O3 и т.д. В зависимости от состава и структуры, оксиды могут быть кислыми, основными или амфотерными. Кислотные оксиды растворяются в воде с образованием кислотных растворов, основные оксиды растворяются с образованием щелочных растворов, а амфотерные оксиды способны проявлять свойства как кислотных, так и основных соединений.
Одним из наиболее известных оксидов металлов является оксид железа (III) или ржавчина (Fe2O3). Он обладает ярко выраженным красным цветом и широко используется в производстве красок, пигментов и стекла. Другим примером оксида металла является оксид алюминия (Al2O3) или алюминий, который используется в производстве керамики, стекла и катализаторов. Оксид меди (II) – CuO, оксид цинка – ZnO и другие тоже имеют свои отличительные свойства и применение в различных отраслях промышленности.
Оксиды металлов демонстрируют различные физические и химические свойства. Некоторые оксиды обладают высокой проводимостью электричества и используются в производстве электроники и полупроводников. Другие обладают высокой термической стабильностью и применяются в производстве огнеупорных материалов. Оксиды металлов также проявляют различную реакцию с кислородом, солями, кислотами и щелочами, что позволяет использовать их в химической промышленности для получения разнообразных химических соединений.
Оксиды металлов: участие в химических реакциях
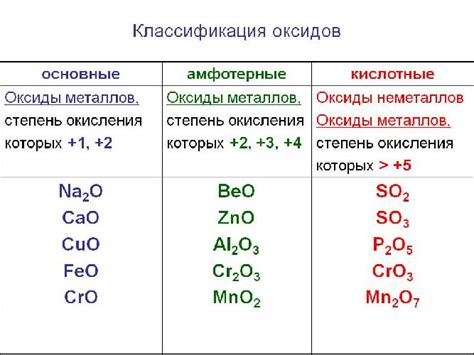
Оксиды металлов - это химические соединения, состоящие из атомов металла и кислорода. Они обладают различными свойствами и способны участвовать во многих химических реакциях.
Оксиды металлов могут проявлять кислотные или основные свойства. Некоторые оксиды металлов, например, оксид железа (Fe2O3) или оксид алюминия (Al2O3), проявляют кислотные свойства и могут реагировать с основаниями, образуя соли. Например, реакция между оксидом железа и гидроксидом натрия может привести к образованию соли - гидроксида железа.
Оксиды металлов также могут реагировать с кислотами, образуя соли или воду. Например, оксид цинка (ZnO) реагирует с соляной кислотой (HCl), образуя хлорид цинка (ZnCl2) и воду (H2O).
Некоторые оксиды металлов могут также реагировать с водой. Например, кальций ооксид (CaO), известный также как негашеная известь, разлагается взаимодействием с водой, образуя гидроксид кальция (Ca(OH)2) и выделяя теплоту.
Оксиды металлов играют важную роль во многих процессах и применяются в различных отраслях промышленности. Они используются в производстве стекла, керамики, катализаторов, а также в процессах образования и обработки металлов.
В целом, оксиды металлов обладают широким спектром свойств и способны участвовать во многих химических реакциях, определяя их характер и результаты.
Способы получения металлов
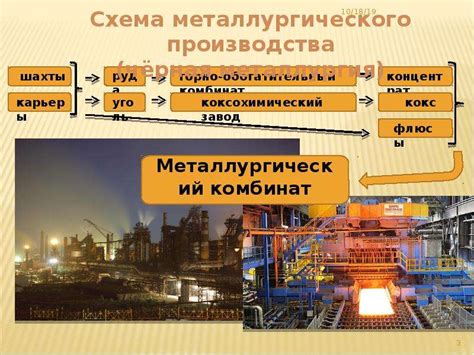
Существует несколько способов получения металлов, которые зависят от их химических свойств и физических характеристик. Один из наиболее распространенных способов - это процесс плавки и выделения металла из его руды. В этом случае руда с содержанием целевого металла подвергается высокой температуре, что позволяет извлечь металл в жидком состоянии.
Еще одним способом получения металлов является электролиз, основанный на использовании электрической энергии. В этом процессе металлы извлекаются из их растворов или расплавов с помощью электрохимического разложения. Электролиз позволяет получать чистые металлы высокой степени чистоты.
Еще одним способом получения металлов является гидрометаллургический метод, который основан на использовании химических растворителей. В этом процессе руда подвергается обработке определенными химическими соединениями, что позволяет растворить металлы и затем выделить их из раствора.
Также металлы могут быть получены методом восстановления из оксидов. Этот процесс основан на соединении металлических оксидов с веществом-восстановителем. При воздействии высоких температур оксиды восстанавливаются и образуются металлы.
Некоторые металлы могут также получаться путем газофазных реакций, при которых металл восстанавливается из парового состояния. Этот метод особенно важен для получения металлов с низкими температурами плавления или высокой химической активностью.
Способы получения оксидов металлов

1. Путем нагревания металла в кислородных условиях.
Одним из самых распространенных способов получения оксидов металлов является их нагревание в присутствии кислорода. Этот процесс называется окислением. При нагревании металла в кислороде происходит реакция, в результате которой образуется соответствующий оксид. Например, при нагревании железа в кислороде образуется оксид железа (III):
4 Fe + 3 O2 → 2 Fe2O3
2. Взаимодействием металла с кислотами.
Другим способом получения оксидов металлов является их взаимодействие с кислотами. Кислоты являются источниками кислорода, поэтому при взаимодействии металла и кислоты происходит окисление металла и образование соответствующего оксида. Например, при реакции цинка с серной кислотой образуется оксид цинка:
Zn + H2SO4 → ZnO + H2SO4
3. Прямым взаимодействием металла с кислородом.
Некоторые металлы способны прямо реагировать с кислородом воздуха и образовывать соответствующий оксид. Например, медь при нагревании на воздухе покрывается тонким слоем черного оксида меди:
2 Cu + O2 → 2 CuO
Эти три способа получения оксидов металлов являются основными и широко используются в химической промышленности и научных исследованиях.
Применение металлов и оксидов в различных отраслях промышленности

Металлы и оксиды играют важную роль в различных отраслях промышленности, благодаря своим уникальным свойствам и способностям. Они являются неотъемлемой частью процессов производства и используются в различных областях, таких как строительство, энергетика и электроника.
В строительстве металлы широко применяются для создания прочных и надежных конструкций. Сталь, алюминий и медь используются для создания фундаментов, каркасов зданий, мостов и других сооружений. Они обладают высокой прочностью, устойчивостью к воздействию окружающей среды и способностью выдерживать большие нагрузки.
В энергетике металлы широко используются для производства и передачи электроэнергии. Алюминиевые провода и кабели применяются для электрической проводки в зданиях и на улицах. Медные провода обладают высокой электропроводностью и применяются в электроэнергетических системах для эффективного передачи энергии на большие расстояния. Оксиды, такие как диоксид титана или оксид цинка, используются в производстве солнечных батарей и других альтернативных источников энергии.
В электронике металлы и оксиды применяются для создания полупроводниковых материалов и компонентов. Оксиды металлов, такие как оксид кремния, используются для изготовления субстратов и чипов в микроэлектронике. Металлы, такие как золото и серебро, применяются для создания контактных площадок и проводников в электрических схемах.
В сельском хозяйстве металлы и оксиды используются для создания сельскохозяйственной техники и оборудования. Стальные орудия и машины применяются для обработки почвы, уборки урожая и других сельскохозяйственных операций. Оксиды, такие как оксид железа или оксид алюминия, используются в процессе создания удобрений и пестицидов.
В итоге, металлы и оксиды играют важную роль в различных отраслях промышленности и являются неотъемлемой частью современного производства. Их свойства и способности делают их незаменимыми материалами для создания прочных конструкций, передачи электроэнергии, изготовления полупроводников и применения в сельском хозяйстве.
Вопрос-ответ

Какие металлы являются самыми распространенными в природе?
Самыми распространенными в природе металлами являются железо, алюминий, кальций и магний. Они встречаются в различных минералах и часто используются в промышленности.
Какие свойства оксидов делают их важными в различных областях жизни?
Оксиды обладают различными полезными свойствами в различных областях жизни. Например, оксид железа используется для производства стали, оксид цинка используется в качестве пигмента в косметической промышленности, оксид алюминия используется в строительстве и т.д. Также многие оксиды обладают свойством проводить электричество и применяются в электротехнике и электронике.
Какими способами можно получить металлы из их руды?
Существует несколько способов получения металлов из их руды. Одним из самых распространенных является метод плавления и выплавки руды с применением высоких температур. Этот способ используется для получения металлов, таких как железо, алюминий и медь. Еще одним способом является электролиз - разложение ионосодержащих соединений металлов при помощи электрического тока. Этот метод применяется, например, для получения алюминия и калия.
