Металлы - это химические элементы, обладающие особыми свойствами, которые делают их незаменимыми в различных отраслях промышленности и жизни человека. Одной из ключевых особенностей металлов является их способность образовывать идеально регулярную кристаллическую решетку. Данная тенденция атомов металлов к образованию структуры с четко определенным порядком позволяет им обладать высокой прочностью и пластичностью.
Чтобы понять, почему металлы имеют такую атомную структуру, необходимо обратиться к особенностям их электронной оболочки. В отличие от не металлов, у металлов электроны заполняют не только внутренние энергетические уровни, но и занимают внешний уровень - уровень свободных электронов. Это делает металлы отличными проводниками электричества и тепла, а также позволяет им образовывать структуру с мощной внутренней связью между атомами.
Основной принцип образования кристаллической структуры металлов - это расположение атомов в узлах решетки. Атомы металлов образуют регулярные, плотные массивы, которые называются элементарными ячейками. Каждый атом металла имеет несколько свободных электронов, которые отдаются другим атомам в процессе образования такой структуры. Это позволяет устанавливать мощные связи между атомами и создавать прочные материалы.
Металлы: структура атомов и их связей
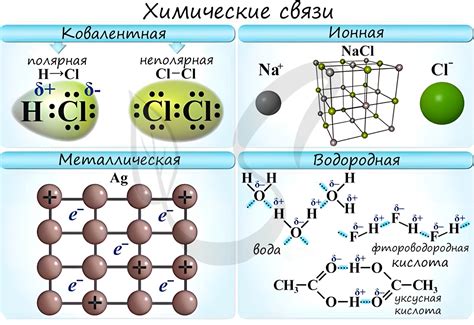
Металлы - это особый класс химических элементов, известных своей высокой электропроводностью и блеском. Структура атомов металлов играет ключевую роль в их свойствах и характеристиках.
Атом металла обычно состоит из ядра, в котором находятся протоны и нейтроны, а также облака электронов, вращающихся вокруг ядра в электронных оболочках. Самая внешняя оболочка, называемая валентной оболочкой, определяет химические свойства металла.
У атомов металлов имеется особая тенденция к образованию металлической связи, что позволяет им образовывать металлическую структуру. Это происходит благодаря наличию свободных или слабо привязанных электронов в валентной оболочке, которые создают электронное облако с общими электронами для всех атомов металла.
Такая структура атомов и их связей в металлах обуславливает их основные свойства, такие как высокая теплопроводность, электропроводность и пластичность. Это также обуславливает специфическое металлическое блеск и способность металлов отражать свет.
Металлическая структура: образование атомов и их взаимодействие

Металлы обладают особой структурой, которая обусловлена особенными свойствами их атомов. В металлической структуре атомы металла образуют кристаллическую решетку, в которой они упорядочены и тесно связаны между собой.
Образование атомов металла происходит за счет перемещения электронов. В металлической связи электроны, находящиеся на внешнем энергетическом уровне атомов металла, свободно перемещаются по кристаллической решетке. В результате образуется облако электронов, окружающее положительно заряженные ядра атомов. Это облако электронов дает металлам такие свойства, как отличная электропроводность и теплопроводность.
Взаимодействие атомов в металле обусловлено наличием облака электронов, которое создает силы, привлекающие положительно заряженные ядра друг друга. Это обеспечивает кристаллическую структуру металла и дает ему прочность. Взаимодействие атомов также определяет температуру плавления и кипения металла, так как при нагревании атомы начинают более активно колебаться, что приводит к разрушению кристаллической решетки и переходу металла из твердого состояния в жидкое.
Таким образом, металлическая структура обусловлена образованием и взаимодействием атомов металла, а особенности этой структуры придают металлам их характеристические свойства.
Вопрос-ответ

Почему атомы металлов стремятся к образованию?
Атомы металлов стремятся к образованию, потому что это позволяет им достичь более стабильного состояния. В своей ионной форме, металлы могут передавать электроны другим атомам, что позволяет им образовывать кристаллическую решетку и иметь более низкую энергию. Таким образом, образование металлической структуры является энергетически выгодным процессом для атомов металлов.
Как образуются металлические связи?
Металлические связи образуются благодаря способности атомов металлов передавать электроны друг другу. Обычно атомы металлов имеют несколько валентных электронов, которые могут легко двигаться внутри металлической структуры. Когда атомы металлов сближаются, свободные электроны создают электростатическое притяжение между положительно заряженными ядрами и свободными электронами, образуя так называемый "электронный облак". Это и создает металлическую связь.
Какие свойства имеют металлы благодаря образованию?
Образование металлической структуры придает металлам ряд характерных свойств. Одно из них - высокая теплопроводность. Благодаря возможности свободного движения электронов, тепловая энергия передается эффективно через металл. Еще одно свойство - хорошая электропроводность. Свободные электроны могут легко перемещаться под влиянием электрического поля. Также, металлы обладают высокой пластичностью и прочностью, что связано с их кристаллической структурой и способностью атомов двигаться внутри нее.
