Металлы главных подгрупп щелочные металлы — это группа химических элементов периодической системы, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они относятся к категории активных металлов и имеют свойства, которые делают их уникальными и широко используемыми в различных сферах науки и промышленности.
Вопросы связанные с щелочными металлами часто возникают в контексте их химических свойств и применения. Например, какие свойства делают их настолько реактивными? Можно ли использовать щелочные металлы в батареях или солнечных панелях? Как щелочные металлы воздействуют на человеческий организм?
Ответы на эти и другие вопросы о щелочных металлах дают возможность более полного понимания их роли и значимости. В данной статье будут рассмотрены основные аспекты химических свойств и применения щелочных металлов, а также освещены некоторые интересные факты, связанные с этой группой элементов.
Что такое металлы главных подгрупп щелочные металлы?
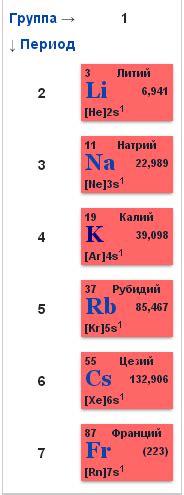
Металлы главных подгрупп щелочные металлы – это элементы, фигурирующие в первой группе периодической системы химических элементов. Главные подгруппы щелочные металлы включают элементы литий, натрий, калий, рубидий, цезий и франций.
Металлы главных подгрупп щелочные металлы отличаются от других элементов периодической системы своими химическими и физическими свойствами. Они имеют низкую плотность, низкую температуру плавления и плохую проводимость тепла и электричества.
Металлы главных подгрупп щелочные металлы являются очень реактивными элементами и легко реагируют с водой и кислородом. Они также образуют химические соединения с другими элементами, такими как хлор, бром и йод.
Металлы главных подгрупп щелочные металлы часто используются в различных отраслях промышленности. Например, калий используется в производстве удобрений, литий – в батарейках, натрий – в производстве стекла и мыла. Они также применяются в лабораториях для проведения химических экспериментов и исследований.
Основные свойства металлов главных подгрупп щелочные металлы

Металлы главных подгрупп щелочные металлы являются химическими элементами, относящимися к первой и второй группам периодической таблицы. Они обладают рядом основных свойств, которые определяют их уникальные химические и физические характеристики.
Первое основное свойство щелочных металлов - это высокая реактивность. Они являются самыми реактивными металлами и легко вступают в химические реакции с другими веществами. Особенно активны они в контакте с водой, образуя щелочные растворы с выделением водорода и образованием соответствующих гидроксидов.
Второе свойство щелочных металлов - это низкое плавление и кипение. Они имеют очень низкие температуры плавления и кипения, что делает их жидкими при комнатной температуре. Это свойство обусловлено наличием слабых межатомных сил в их кристаллической структуре.
Третье свойство щелочных металлов - это мягкость и деформируемость. Они являются самыми мягкими металлами и могут быть легко деформированы или раскатаны в листы или проволоку. Это связано с большой деформированностью и слабостью их межатомных связей.
Четвертое свойство щелочных металлов - это способность образовывать ионы с положительным зарядом. Они легко отдают свои внешние электроны, образуя положительно заряженные ионы. Эта способность позволяет им вступать в реакции с отрицательно заряженными ионами или молекулами, образуя стабильные соединения.
Таким образом, основные свойства металлов главных подгрупп щелочные металлы определяют их химическую активность, низкие температуры плавления и кипения, мягкость и деформируемость, а также способность образовывать положительно заряженные ионы.
Каким образом металлы главных подгрупп щелочные металлы используются в промышленности?
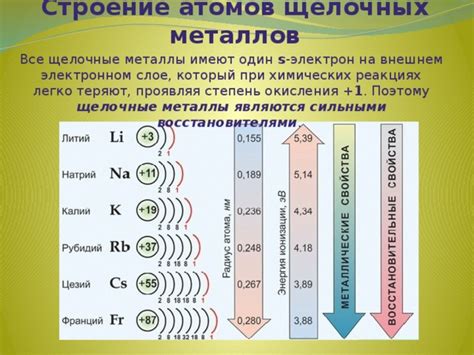
Металлы главных подгрупп щелочные металлы – литий, натрий, калий, рубидий и цезий – находят широкое применение в различных отраслях промышленности благодаря своим уникальным свойствам и химической активности.
Литий широко используется в производстве легких и прочных литиевых батарей, которые применяются в электронике, автомобильной промышленности и медицине. Также литий используется в производстве стекла и керамики, в процессе получения различных сплавов и катализаторов.
Натрий является одним из основных компонентов в производстве щелочей, соды, хлора, гидроксида натрия и других оснований. Натрий используется в производстве стекла, мыла, отбеливающих средств, а также в пищевой промышленности в качестве консерванта и регулятора кислотности.
Калий применяется в качестве удобрения в сельском хозяйстве, обеспечивая рост и развитие растений. Калийные соединения используются в производстве стекла, мыла, моющих средств и полимеров. Также калий широко применяется в производстве взрывчатых веществ и удобрений.
Рубидий и цезий находят применение в научных исследованиях, в технике и в производстве электронных приборов. Они используются в фоточувствительных элементах, в приборах сверхвысоких частот и в лазерной технике.
В чем состоит роль металлов главных подгрупп щелочные металлы в нашей жизни?
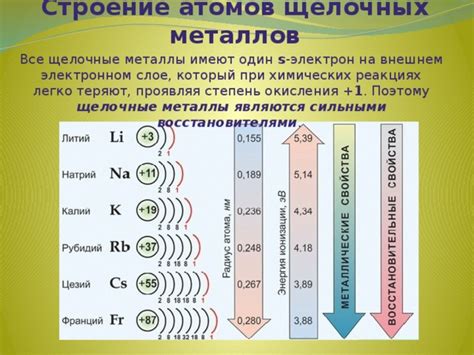
Металлы главных подгрупп щелочные металлы играют важную роль во многих сферах нашей жизни. Например, натрий широко используется в пищевой промышленности для приготовления пищевых добавок, регулирования кислотности продуктов и увеличения сроков их хранения. Калий, в свою очередь, является необходимым макроэлементом для растений и используется в сельском хозяйстве в качестве удобрения.
Металлы главных подгрупп щелочные металлы также применяются в качестве катализаторов в различных процессах. Например, литий и цезий используются в производстве нефтепродуктов, а рубидий применяется в процессе хлорирования органических соединений.
Кроме того, металлы главных подгрупп щелочные металлы имеют широкое применение в производстве электронных устройств и батарей. Литий-ионные аккумуляторы, состоящие в основном из лития, представляют собой одну из наиболее распространенных и эффективных батарей для мобильных устройств, электромобилей и других портативных приборов.
Важно отметить, что металлы главных подгрупп щелочные металлы обладают высокой химической реактивностью и реакционной способностью, что делает их незаменимыми во многих отраслях промышленности. Они широко используются в процессах синтеза различных соединений и материалов, а также в производстве стекла, керамики и лаков.
Преимущества и недостатки металлов главных подгрупп щелочные металлы

Преимущества:
- Щелочные металлы, такие как литий, натрий, калий и другие, обладают высокой химической активностью. Они легко вступают в реакцию с кислотами и водой, что делает их полезными в различных промышленных процессах.
- Эти металлы хорошо проводят электричество и тепло. Из-за этого они широко используются в производстве аккумуляторов, проводов и других электронных устройств.
- Щелочные металлы обладают низкой плотностью и низкой температурой плавления, что делает их легкими в обработке и применении в различных отраслях промышленности.
Недостатки:
- Одним из главных недостатков щелочных металлов является их высокая химическая реактивность. Они очень реактивны в контакте с водой и кислородом, что может привести к возгоранию или взрыву.
- Щелочные металлы имеют низкую механическую прочность и довольно мягкие, что ограничивает их использование в конструкционных материалах.
- Некоторые щелочные металлы, такие как литий, имеют высокую стоимость из-за их редкого нахождения в природе и сложности процесса добычи.
Интересные факты о металлах главных подгрупп щелочные металлы

1. Они относятся к самым химически активным металлам.
Щелочные металлы – это элементы, расположенные в первой группе периодической таблицы, а именно: литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они получили свое название "щелочные" из-за способности образовывать щелочные растворы при контакте с водой.
2. Вещества с щелочными металлами обладают яркой окраской.
Многие соединения щелочных металлов обладают яркой окраской, что делает их популярными в качестве пигментов для красок и красителей. Например, хлорид цезия даёт ярко-синюю окраску, а хромат калия – ярко-желтую.
3. Эти металлы широко используются в быту и промышленности.
Щелочные металлы имеют широкое применение в различных областях. Например, литий используется в производстве литий-ионных аккумуляторов, калий используется в удобрениях, а натрий – в производстве стекла и мыла.
4. Щелочные металлы обладают низкой плотностью.
Одной из особенностей этих металлов является низкая плотность. Например, литий является самым легким металлом, его плотность составляет всего около 0,53 г/см³. Это делает их очень легкими и удобными в использовании.
5. Они реагируют с водой, образуя гидроксиды и высвобождая водород.
Одной из характерных реакций щелочных металлов является реакция с водой. При этом образуются гидроксиды металлов и высвобождается водород. Например, реакция натрия с водой выражается следующим уравнением: 2Na + 2H₂О → 2NaOH + H₂.
Вопрос-ответ

Какие элементы относят к группе щелочные металлы?
К группе щелочные металлы относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Какую роль играют щелочные металлы в природе?
Щелочные металлы играют важную роль в природе. Они являются основными компонентами земной коры и морской воды. Кроме того, эти металлы являются необходимыми элементами для живых организмов. Например, калий необходим для многих биологических процессов в организме человека.
