Металлы главной подгруппы второй группы - это элементы, которые включают в себя металлы, такие как цинк (Zn), кадмий (Cd) и ртуть (Hg). Они находятся во второй горизонтальной периоде периодической системы элементов и имеют общую электронную конфигурацию ns2.
Цинк является блестящим серебристо-белым металлом, который легко поддаётся обрабатыванию и способный образовывать различные соединения. Кадмий также имеет серебристо-белый цвет и является очень реактивным металлом. Он обладает низкой температурой плавления и испарения. Ртуть - это единственный металл, который находится в жидком состоянии при комнатной температуре.
Металлы главной подгруппы второй группы обладают рядом уникальных физических и химических свойств. Они отличаются высокой электропроводностью и теплопроводностью, и являются хорошими катализаторами химических реакций. Они также обладают высокой пластичностью и мягкостью, что делает их легко поддающимися формованию и обработке.
Кроме того, металлы главной подгруппы второй группы обладают различными важными применениями в промышленности и науке. Например, цинк широко используется в гальванических покрытиях, в производстве батареек и литейных сплавов, а также в качестве добавки в различных материалах. Кадмий используется в резисторах, аккумуляторах и компьютерных чипах. Ртуть применяется в термометрах, барометрах и детекторах уровня.
Родственные связи и химическая природа

Металлы главной подгруппы второй группы – это группа химических элементов, которые имеют сходные химические свойства и образуют родственные связи друг с другом. Они входят во второй период ПТ, следующий за первым периодом, где находятся металлы главной подгруппы первой группы.
Металлы главной подгруппы второй группы включают бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Все эти элементы относятся к щелочно-земельным металлам и отличаются высокой электропроводностью и металлическим блеском.
Химическая природа металлов главной подгруппы второй группы основана на наличии двух валентностей: +2 и +1. Большинство элементов этой группы, за исключением бериллия, образуют двухвалентные соединения, что связано с наличием у них двух электронов во внешней электронной оболочке. При этом, при одновременном наличии двух валентностей возможно образование сложных соединений, содержащих положительно заряженные ионы.
Электронная структура и магнитные свойства
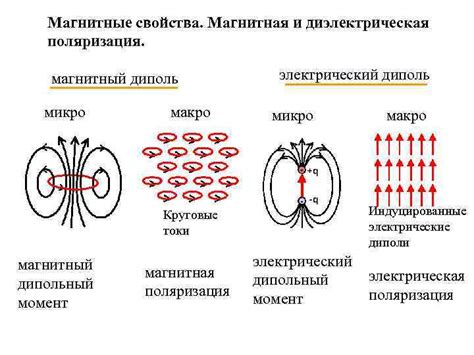
Электронная структура металлов главной подгруппы второй группы представляет особый интерес из-за их уникальных свойств и химической активности. Внешней электронной конфигурацией данных металлов является с2p3, что означает наличие двух внешних электронов s-подуровня и трех электронов p-подуровня. Это говорит о том, что данные металлы входят во вторую группу по периодической системе Менделеева и имеют 2 валентные электрона.
Магнитные свойства металлов главной подгруппы второй группы весьма разнообразны и зависят от их электронной структуры. Некоторые из этих металлов обладают ферромагнитными свойствами, то есть являются постоянными магнитами и обладают способностью притягивать другие металлы. Это связано с наличием неспаренных электронов в орбитали п-подуровня и гибридизацией s- и p-орбиталей. Однако не все металлы этой группы обладают магнитными свойствами, так как их магнитное поведение может сильно варьировать в зависимости от других факторов, включая специфическую структуру исследуемого металла.
Кроме того, металлы главной подгруппы второй группы обладают интересными свойствами с точки зрения применения в магнитных материалах. Некоторые из них, такие как железо, кобальт и никель, широко используются в производстве магнитных сплавов и магнитов благодаря своим магнитным свойствам. Они обеспечивают высокую магнитную индукцию, стабильность и долговечность магнитных материалов.
Физические свойства и состояние

Металлы главной подгруппы второй группы характеризуются определенными физическими свойствами и состоянием.
Точка плавления: Одной из основных характеристик металлов является их высокая точка плавления. Большинство металлов главной подгруппы второй группы имеют достаточно высокую температуру плавления, что позволяет им существовать в твердом состоянии при комнатной температуре или выше.
Плотность: Металлы главной подгруппы второй группы обладают высокой плотностью. Это связано с компактной укладкой атомов в кристаллическую решетку. Плотность металлов может быть разной, но в целом они отличаются от других элементов по своей плотности.
Проводимость: Все металлы главной подгруппы второй группы обладают высокой электропроводностью. Это связано с наличием свободных электронов в их валентной оболочке, которые легко перемещаются под воздействием электрического поля.
Изготовление и применение: Из-за своих физических свойств, металлы главной подгруппы второй группы имеют широкое применение в различных отраслях. Они используются в строительстве, машиностроении, электронике и многих других областях. Они отличаются высокой прочностью, устойчивостью к коррозии и механическому воздействию.
Применение и альтернативные методы использования
Металлы главной подгруппы второй группы обладают разнообразными свойствами, что позволяет им использоваться во многих отраслях промышленности и науки. Одним из основных применений этих металлов является их использование в производстве различных видов стали. Сталь, благодаря присутствию главной подгруппы второй группы металлов, обладает высокой прочностью, твердостью, устойчивостью к коррозии и другим полезным свойствам.
Однако металлы главной подгруппы второй группы также находят применение и в других областях. Например, они широко используются в электротехнике для производства контактных элементов, электрических проводов и кабелей, а также различных электронных компонентов. Благодаря своей низкой сопротивляемости электрическому току, эти металлы значительно улучшают эффективность работы электронных устройств.
Кроме того, металлы главной подгруппы второй группы активно применяются и в медицине. Благодаря своей биосовместимости, они используются в производстве медицинских инструментов, имплантатов и протезов. Эти металлы обладают высокой степенью устойчивости к коррозии и неприхотливости в эксплуатации, что делает их идеальными материалами для использования в организме человека.
В настоящее время появились и альтернативные методы использования металлов главной подгруппы второй группы. Например, вместо использования этих металлов в их чистом виде, их можно использовать в соединении с другими материалами, например, полимерами, чтобы получить материалы с новыми свойствами и улучшенными характеристиками. Также исследователи работают над разработкой новых способов получения и использования данных металлов с использованием новейших технологий, таких как нанотехнологии и инженерия поверхности.
В целом, металлы главной подгруппы второй группы являются универсальными и незаменимыми материалами, которые нашли применение во многих отраслях промышленности и науки. Благодаря их уникальным свойствам и постоянному развитию новых методов использования, эти металлы остаются актуальными и востребованными в современном мире.
Вопрос-ответ

Какие металлы относятся к главной подгруппе второй группы?
К главной подгруппе второй группы относятся металлы цинк (Zn), кадмий (Cd) и ртуть (Hg).
Какие основные характеристики металлов главной подгруппы второй группы?
Металлы главной подгруппы второй группы обладают следующими характеристиками: они являются отличными проводниками электропроводности, имеют блестящую поверхность, формируют оксиды, которые растворяются в воде, и обладают низким плавлениям и кипением.
Какие свойства имеют металлы главной подгруппы второй группы?
Металлы главной подгруппы второй группы обладают несколькими свойствами. Например, они довольно хорошо взаимодействуют с кислородом, образуя оксиды, которые обладают щелочными свойствами. Кроме того, эти металлы образуют комплексы с различными лигандами и имеют способность образовывать сплавы с другими металлами.
Какие применения имеют металлы главной подгруппы второй группы?
Металлы главной подгруппы второй группы имеют различные применения в нашей повседневной жизни. Например, цинк используется для оцинковки стали, что помогает предотвратить ее коррозию. Кадмий находит применение в производстве аккумуляторов и в электронике. Ртуть используется в термометрах и в некоторых электрических приборах.
