Металлы главной подгруппы II группы периодической системы элементов характеризуются своими уникальными свойствами. Один из наиболее распространенных и широко используемых металлов этой группы - кальций.
Кальций - срежний металл блестящего серого цвета, который с легкостью реагирует с водой и воздухом. Одной из его основных особенностей является его высокая реактивность. Кальций обладает способностью вступать в химические реакции с большим количеством веществ, включая кислород, нитроген и сероводород.
Особая важность кальция в природе заключается в том, что он является существенным компонентом для поддержания основных процессов в организмах живых существ. Кальций играет ключевую роль в формировании и поддержании костной ткани, функционировании мышц и нервной системы, а также в свертываемости крови.
Благодаря своим уникальным свойствам, кальций находит широкое применение в различных отраслях промышленности. Он используется в производстве стали, алюминия, керамики, стекла, пластика и других материалов. Кроме того, кальций применяется в фармакологии, сельском хозяйстве, в процессе очистки воды и во многих других сферах деятельности человека.
Химические свойства кальция

Реакция с водой: Кальций является очень активным металлом и реагирует с водой с образованием водорода. При этой реакции образуется гидроксид кальция, который растворяется в воде, образуя щелочную среду.
Реакция с кислородом: Кальций является реактивным металлом и сильно окисляется на воздухе под воздействием кислорода. На поверхности кальция образуется пленка оксида, которая защищает металл от дальнейшего окисления.
Взаимодействие с неметаллами: Кальций реагирует с многими неметаллами, образуя соответствующие химические соединения. Например, при взаимодействии с серой образуется сульфид кальция.
Окислительные свойства: Кальций обладает выраженными окислительными свойствами и может окислять другие вещества. Например, он может окислять металлы облегченной группы I, такие как литий и натрий.
Реакция с кислотами: Кальций реагирует с кислотами, образуя соответствующие соли и выделяя водород. Например, при реакции с соляной кислотой образуется хлорид кальция и выделяется водородный газ.
Физические свойства кальция

Кальций является мягким и химически активным металлом.
Он обладает серебристо-белым цветом и блестящей поверхностью.
Температура плавления кальция составляет около 842 градусов по Цельсию, а его температура кипения - около 1484 градусов по Цельсию.
Одной из особенностей кальция является его активность воздухе.
При контакте с кислородом из воздуха, кальций окисляется и покрывается оксидной пленкой.
Эта пленка способна защищать металл от дальнейшей окислительной реакции.
Однако, влажность воздуха способствует образованию водорастворимого гидроксида кальция, что может приводить к быстрому разрушению металла.
Кальций обладает хорошей электропроводностью и теплопроводностью.
Он также является довольно пластичным металлом, что позволяет его легко прокатывать и раскатывать в тонкую проволоку или пластины.
Кальций относительно легко растворяется в воде, образуя гидроксид кальция.
Этот гидроксид обладает щелочными свойствами и широко используется в различных отраслях промышленности.
Реакции кальция с водой и кислотами
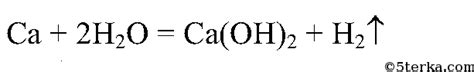
Реакция кальция с водой: Кальций активно взаимодействует с водой, выделяя при этом водородный газ и образуя гидроксид кальция. Эта реакция имеет химическое уравнение: Ca + 2H2O → Ca(OH)2 + H2. При контакте с водой образуется белая нерастворимая осадок гидроксида кальция, который может быть заметен невооруженным глазом.
Реакция кальция с кислотами: Кальций реагирует с различными кислотами, образуя соли и выделяя при этом водородный газ. Например, реакция кальция с соляной кислотой имеет химическое уравнение: Ca + 2HCl → CaCl2 + H2. Эта реакция является типичным представителем реакций металлов с кислотами.
Взаимодействие кальция с карбидом кальция: Кальций может взаимодействовать с карбидом кальция, образуя ацетилен. Эта реакция имеет химическое уравнение: CaC2 + 2H2O → C2H2 + Ca(OH)2. Ацетилен, образующийся при этой реакции, является важным промышленным сырьем и используется, например, в газовых светильниках и сварочных аппаратах.
Окисление кальция воздухом: Кальций реагирует с кислородом воздуха при помещении на воздух, образуя оксид кальция. Эта реакция имеет химическое уравнение: 2Ca + O2 → 2CaO. Оксид кальция является основным продуктом окисления кальция воздухом и является активным кислотным окислителем.
Применение кальция в промышленности

Кальций – это металл главной подгруппы II группы периодической системы, который широко используется в промышленности благодаря своим уникальным свойствам и химической активности.
Одним из основных областей применения кальция является производство стали. Кальций используется в виде сплавов с другими металлами, такими как алюминий и сера, чтобы улучшить свойства стали. Эти сплавы способствуют улучшению прочности, коррозионной стойкости и способности к деформации стали.
Кальций также широко применяется в производстве алюминия. Он используется для очистки расплавленного алюминия от примесей и вредных элементов, таких как кремний и железо. Кальций также способствует улучшению сплавляемости алюминия и повышению его прочности и коррозионной стойкости.
Другой важной областью применения кальция является производство очистных средств. Кальций используется в качестве активного компонента многих моющих средств и отбеливателей. Он способствует эффективному удалению загрязнений, обезжириванию и отбеливанию поверхностей.
- Кальций применяется также в производстве стекла и керамики. Он улучшает термическую и механическую стабильность материалов, а также позволяет им иметь прозрачность и блеск.
- Кальций используется в производстве некоторых видов бетона и строительных материалов. В результате реакции кальция с водой образуется кальцийгидроксид, который является одним из основных компонентов цемента.
- В металлургии кальций используется для десульфурации железной руды. Он реагирует с серой в руде, образуя кальцийсульфид, который можно легко удалить.
Таким образом, кальций играет важную роль в промышленности и находит широкое применение в различных отраслях, включая производство стали, алюминия, очистных средств, стекла, керамики, бетона и металлургию.
Биологическая роль кальция

Кальций является одним из самых важных макроэлементов, необходимых организму человека и животных. Он выполняет множество биологических функций и присутствует во многих тканях и клетках.
В первую очередь, кальций играет важную роль в формировании и укреплении костей и зубов. Около 99% общего количества кальция в организме находится именно в костях и зубах. Он является строительным материалом для костей и придает им прочность. Также кальций участвует в процессах реакций, контролирующих образование, перестройку и разрушение костной ткани.
Кроме того, кальций играет роль в сократительной функции мышц. Он необходим для передачи нервных импульсов и участвует в процессе сокращения мышц. Благодаря кальцию мы способны двигаться и выполнять различные двигательные действия.
Кальций также участвует в процессах свертываемости крови. Вместе с фосфатами кальций образует основной компонент тромба, благодаря которому происходит остановка кровотечения при повреждении сосудов.
Кроме того, кальций участвует в регуляции работы множества ферментов, гормонов и нейромедиаторов, что позволяет ему контролировать множество биологических процессов в организме. Он также участвует в передаче нервного импульса и в работе многих гормонов, включая инсулин.
Важно отметить, что кальций необходим для нормальной функции клеток и обменных процессов в организме. Он участвует в многих реакциях, связанных с обменом энергии, и является неотъемлемой частью множества ферментов и белков, необходимых для выполнения различных клеточных функций.
Опасность и меры предосторожности при работе с кальцием
Кальций — это металлический элемент, который обладает определенной опасностью при работе с ним. При контакте с кальцием возможно возникновение пожара или взрыва. Поэтому необходимо соблюдать определенные меры предосторожности.
Во-первых, важно обеспечить хорошую вентиляцию при работе с кальцием. При его нагревании или реакции с другими веществами могут выделяться вредные газы. Поэтому рекомендуется работать с кальцием в специально оборудованных помещениях или под вытяжной вентиляцией.
Во-вторых, при работе с кальцием необходимо использовать защитные средства. Рекомендуется надевать защитные очки, респиратор или маску, а также резиновые перчатки. Это позволит предотвратить попадание кальция на кожу или в глаза и защитит дыхательные пути от вредных газов.
В-третьих, необходимо избегать контакта кальция с водой или влажными веществами. При взаимодействии с водой кальций выделяет водород, что может привести к возгоранию или взрыву. Поэтому следует осторожно обращаться с кальцием и хранить его в сухом месте.
Наконец, при работе с кальцием необходимо ознакомиться с инструкциями производителя и соблюдать все указанные противопоказания и предупреждения. Следование этим рекомендациям поможет избежать опасных ситуаций и обеспечить безопасность при работе с кальцием.
Вопрос-ответ

Зачем нужен кальций для организма человека?
Кальций является одним из самых важных макроэлементов для организма человека. Он играет ключевую роль в формировании и укреплении костей и зубов, а также участвует в работе мышц, нервной системы и сердечно-сосудистой системы. Кроме того, кальций необходим для правильного сокращения мышц, передачи нервных импульсов и синтеза гормонов.
В каких продуктах содержится кальций?
Кальций можно получить из различных продуктов питания. Самые богатые источники кальция - это молочные продукты, включая молоко, йогурт, творог и сыр. Также кальций содержится в зеленых овощах, таких как брокколи и шпинат, в тунце и сардине, а также в некоторых видов орехов, включая миндаль и бразильский орех.
Какой является оптимальная доза кальция для взрослого человека?
Оптимальная доза кальция для взрослого человека составляет около 1000-1300 мг в день. Важно отметить, что уровень кальция, необходимый для каждого конкретного человека, может варьироваться в зависимости от пола, возраста, физической активности и других факторов. Поэтому перед увеличением дневного потребления кальция рекомендуется проконсультироваться с врачом или диетологом.
