Коррозия — это процесс разрушения металлов под воздействием окружающей среды. Железо и его сплавы, такие как сталь, подвержены коррозии особенно сильно. Коррозия может быть вызвана различными факторами, включая влагу, кислород, химические реакции и другие агенты. Однако, существует несколько методов защиты железных изделий от коррозии, одним из которых является использование других металлов в качестве защитного покрытия.
Один из самых популярных металлов, используемых для защиты железа от коррозии, это цинк. Цинк создает на поверхности железных изделий тонкую защитную пленку, которая предотвращает контакт металла с влагой и кислородом. Цинковое покрытие может быть нанесено на поверхность железа различными способами, включая оцинковку и горячее цинкование.
Еще одним эффективным методом защиты от коррозии является использование алюминия. Алюминий обладает самоустанавливающимися свойствами, что означает, что при повреждении покрытия на поверхности алюминия образуется окисный слой, который действует как барьер для дальнейшей коррозии. Алюминиевые покрытия можно наносить с помощью анодной окиси или алюминизации.
Также для защиты железных изделий от коррозии могут быть использованы другие металлы, такие как хром, никель, олово и медь. Каждый из этих металлов имеет свои особенности и преимущества, поэтому выбор зависит от конкретного случая и требований.
Основные причины коррозии железных изделий

Коррозия железных изделий представляет собой процесс разрушения металла под воздействием окружающей среды. Она вызывает значительные повреждения не только наружных поверхностей, но и внутренних структур материала. Представляем вам основные причины этого нежелательного процесса.
- Воздействие влаги и воды. Наличие влаги и воды является главным фактором, способствующим возникновению коррозии железных изделий. Влага содержит растворенные соли, которые ускоряют химические реакции на поверхности металла, приводящие к образованию окислов и потере прочности материала.
- Контакт с кислотами. Кислотные растворы, такие как серная или соляная кислота, могут также вызвать коррозию железных изделий. Кислоты реагируют с металлом, образуют коррозионные реакции и разрушают его структуру.
- Контакт со средами с высоким содержанием солей. Соли, содержащиеся в атмосфере или других окружающих средах, могут также вызвать коррозию железных изделий. Соли реагируют с поверхностью металла, ускоряя процесс коррозии.
Для защиты железных изделий от коррозии рекомендуется использовать специальные металлы или защитные покрытия, которые могут предотвратить контакт металла с окружающей средой. Также важно регулярно проводить проверку и обслуживание изделий, чтобы своевременно выявить и устранить возможные признаки коррозии.
Воздействие атмосферных условий

Одной из основных причин коррозии железных изделий является их воздействие атмосферными условиями. При наличии кислорода в воздухе, железо начинает окисляться, что приводит к образованию ржавчины. Этот процесс ускоряется в наличии влаги и солей, так как они являются катализаторами окисления металла.
Климатические особенности места эксплуатации также оказывают влияние на скорость коррозии железных изделий. В зонах с высокой влажностью воздуха, например, близ морского побережья, коррозия происходит быстрее, поскольку влага способствует увеличению активности окислительных процессов.
Кроме влаги и кислорода, на железо могут воздействовать и другие атмосферные загрязнители, такие как сернистый газ, диоксид серы и другие химические соединения. Они могут ускорить процесс коррозии и привести к более быстрому разрушению металлической поверхности.
Для защиты железных изделий от коррозии воздействию атмосферных условий необходимо применять различные методы и материалы. Например, нанесение покрытий из антикоррозионных материалов или использование специальных покрытий, которые предотвращают доступ влаги и кислорода к поверхности металла. Также можно использовать сплавы с высокой стойкостью к коррозии или применять методы электрохимической защиты, такие как катодная защита.
Химические процессы
Одним из способов защиты железных изделий от коррозии является использование химических процессов. При этом происходит взаимодействие различных веществ с поверхностью металла, что позволяет предотвратить образование коррозии.
Один из наиболее распространенных методов химической защиты - нанесение на поверхность металла покрытия с использованием специальных химических соединений. Эти соединения образуют защитный слой, который препятствует проникновению влаги и кислорода, основных факторов, вызывающих коррозию. Такие покрытия могут быть невидимыми или иметь определенный цвет в зависимости от выбранного химического соединения.
Другим методом химической защиты является использование водородного пероксида или кислоты для удаления окисленного слоя с поверхности металла. Это помогает восстановить его и предотвратить дальнейшую коррозию. Важно использовать правильную концентрацию и применять эти вещества с осторожностью, чтобы избежать повреждений металлической поверхности.
Также существуют специальные составы на основе органических или неорганических кислот, которые наносят на поверхность металла. Они вызывают химические реакции с окисленными слоями и образуют защитный слой. Эти составы могут быть прозрачными или иметь определенный оттенок, что позволяет выбрать наиболее подходящий вариант для конкретного изделия.
Необходимо отметить, что в процессе химической защиты металлической поверхности важно обеспечить правильные условия, такие как температура, время взаимодействия и применяемые вещества. Только соблюдение всех требований позволит достичь эффективной защиты от коррозии и обеспечить продолжительность эксплуатации железных изделий.
Воздействие воды и влаги
Вода и влага являются одними из основных причин коррозии металлических изделий. При контакте с водой, металл может начать окисляться, что приводит к появлению ржавчины и разрушению изделий. Даже небольшие количества влаги могут проникать в малейшие трещины и микропоры металла, вызывая необратимые процессы коррозии.
Эффект воды и влаги на металлические изделия может быть значительно усилен при наличии дополнительных факторов. Например, при повышенной температуре вода может проникать глубже в структуру металла и ускорять процессы коррозии. Также, наличие солей или кислот в воде может усилить коррозивное воздействие, так как они обладают высокой агрессивностью по отношению к металлам.
Для предотвращения воздействия воды и влаги на металлические изделия можно применять различные подходы и материалы. Например, использование ржавеющей стали с высоким содержанием хрома и никеля может снизить риск коррозии. Также, можно нанести на поверхность металла защитные покрытия, такие как краска или гальваническое покрытие. Важно учитывать, что эффективность таких мер зависит от условий эксплуатации и свойств металла, поэтому выбор наиболее подходящих методов защиты требует тщательного анализа и расчета.
Механическое повреждение
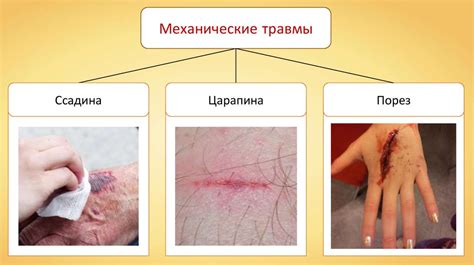
Механическое повреждение является одной из основных причин коррозии металлических изделий. При обработке, транспортировке и эксплуатации изделий, на них может возникать множество механических воздействий, которые могут повредить поверхность металла, открыть микротрещины или удалить защитное покрытие.
Механическое повреждение может быть вызвано такими факторами, как удары, трение, истирание и неправильное использование металлических изделий. Например, удары могут вызвать отслоение защитного покрытия и повреждение поверхности металла. Трение и истирание могут привести к образованию коррозионных желобков и глубоких царапин на поверхности металла.
Другой причиной механического повреждения является неправильное использование металлических изделий. Если металлическое изделие используется не по назначению или неправильно хранится, то это может привести к механическому повреждению и возникновению коррозии.
Для защиты металлических изделий от механического повреждения рекомендуется использовать специальные защитные покрытия или обрабатывать поверхность изделий специальными составами. Также важно правильно использовать и хранить металлические изделия, чтобы минимизировать риск механического повреждения.
Методы защиты от коррозии
Коррозия – это процесс разрушения металла под воздействием окружающей среды. Она вызывает повреждение и деградацию изделий, поэтому методы защиты от коррозии являются важной составной частью промышленности.
1. Покрытие металла
Покрытие металла – это один из наиболее распространенных методов защиты от коррозии. Оно заключается в нанесении защитного слоя на поверхность металла, который создает барьер, препятствующий воздействию окружающих веществ. Для покрытия металла часто используются покрытия на основе цинка, алюминия или эмали.
2. Гальваническая защита
Гальваническая защита основана на создании гальванической пары между металлом, который нужно защитить, и металлом, функционирующим как анод. Анодный металл теряет электроны и становится жертвой коррозии, тогда как металл, который нужно защитить, становится катодом и остается неповрежденным.
3. Использование пассивирующих металлов
Некоторые металлы обладают способностью к пассивации, то есть образованию защитной пленки, которая препятствует дальнейшей коррозии. Например, нержавеющая сталь содержит в составе хром, который образует оксидную пленку на поверхности металла и защищает его от коррозии.
4. Контроль окружающей среды
Очень важным методом защиты от коррозии является контроль окружающей среды, в которой находятся металлические изделия. Одна из основных причин коррозии – влажность и присутствие агрессивных химических веществ в окружающей среде, поэтому поддержание оптимальных параметров окружающей среды помогает предотвратить повреждения.
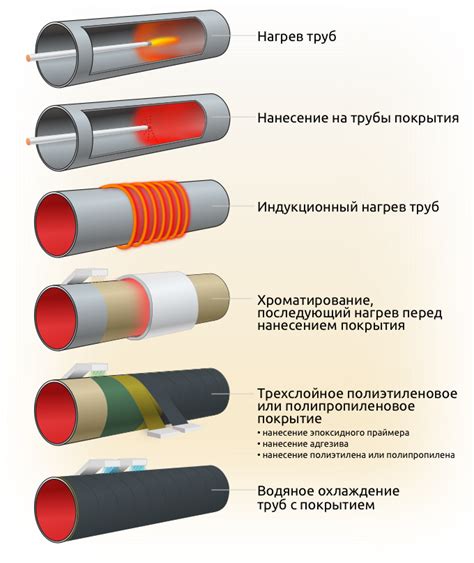
Покрытия

Один из способов защиты железных изделий от коррозии - нанесение различных покрытий на их поверхность. Покрытия могут быть органическими или неорганическими, их выбор зависит от условий эксплуатации и требуемого уровня защиты.
Органические покрытия, такие как краски и лаки, содержат органические полимеры, которые образуют защитный слой на поверхности металла. Они обладают хорошей адгезией к железу и эффективно препятствуют контакту металла с агрессивными средами. Однако органические покрытия могут терять свои свойства со временем и требуют периодической поверхностной обработки.
Неорганические покрытия, такие как цинковые и алюминиевые покрытия, образуются путем нанесения специальных растворов или пленок металла на поверхность изделий. Они обладают высокой степенью защиты и способны создавать электрохимическую барьерную защиту от коррозии. Такие покрытия широко применяются в сфере строительства и машиностроения.
Кроме того, существуют специализированные покрытия, способные обеспечить дополнительную защиту от специфических коррозионных факторов. Например, кадмиевые покрытия обладают высокой устойчивостью к высоким температурам и агрессивным химическим средам. Титановые покрытия обеспечивают защиту от коррозии при воздействии солей и кислот.
В целом, выбор покрытия для защиты железных изделий от коррозии - это вопрос комплексного подхода и зависит от многих факторов, таких как условия эксплуатации, желаемый срок службы и требования к внешнему виду. Правильно выбранное покрытие поможет продлить срок службы металлических объектов и сохранить их эстетический вид на протяжении длительного времени.
Катодная защита

Катодная защита – это эффективный метод предотвращения коррозии железных изделий. Она основана на создании электрического поля, которое разрушает химический процесс окисления металла. В качестве анодов используются специальные металлические элементы, которые при постоянном токе расщепляются и поглощают всю коррозионную энергию.
Преимуществом катодной защиты является ее длительность и надежность. При правильном подборе материалов и эксплуатации система катодной защиты может служить несколько десятилетий, предотвращая появление ржавчины и других повреждений. Этот метод активно используется при защите металлических трубопроводов, резервуаров, судов и других объектов, находящихся в агрессивных условиях коррозионной среды.
Однако внедрение катодной защиты требует определенных затрат и специалистов с опытом работы в этой области. Систему необходимо проектировать с учетом всех факторов, влияющих на коррозию, таких как рН, температура, концентрация агрессивных веществ и др. Кроме того, регулярно следует проводить контроль параметров электрического поля и производить ремонтные работы при необходимости.
Несмотря на некоторые особенности и требования, катодная защита является эффективным и широко используемым методом защиты металлических изделий от коррозии. Она позволяет значительно продлить срок службы металла, снизить затраты на ремонт и обеспечить надежность работы оборудования в условиях агрессивных сред.
Использование металлических сплавов

Для защиты железных изделий от коррозии широко применяются различные металлические сплавы. Они отличаются особыми свойствами и химическим составом, что позволяет создавать материалы, обладающие высокой степенью защиты.
Один из наиболее эффективных сплавов — нержавеющая сталь. Она содержит хром, который образует защитную пленку на поверхности металла, предотвращая его коррозию. Нержавеющая сталь используется в различных отраслях, где требуется высокая устойчивость к агрессивной среде, например, в пищевой промышленности или при производстве химических реактивов.
Еще одним распространенным металлическим сплавом является алюминий. Он обладает хорошей устойчивостью к окислению и образует плотную оксидную пленку на поверхности, защищающую металл от коррозии. Алюминий широко применяется в авиационной и строительной отраслях, где необходима легкость и прочность материала.
Другим интересным сплавом является цинковое покрытие. Цинк наносится на поверхность железа методом гальванического покрытия и образует защитную пленку. Цинковые покрытия используются для защиты стальных изделий от коррозии в различных условиях эксплуатации, включая суровые климатические условия и контакт с агрессивными средами.
Важно отметить, что выбор металлического сплава для защиты железных изделий от коррозии должен основываться на конкретных условиях эксплуатации и требованиях к материалу. Каждый сплав имеет свои преимущества и ограничения, поэтому необходимо учитывать все факторы перед принятием решения о выборе определенного материала.
Вопрос-ответ

Какие металлы подходят для защиты железных изделий от коррозии?
Для защиты железных изделий от коррозии можно использовать такие металлы, как алюминий, цинк и магний. Они обладают высокой электрохимической активностью и способны создать защитную пленку на поверхности железа.
Какие свойства должен иметь металл для эффективной защиты от коррозии?
Металл, используемый для защиты от коррозии, должен обладать следующими свойствами: высокой электрохимической активностью, способностью создавать защитную пленку на поверхности металла, стабильностью в окружающей среде и совместимостью с материалом, который нужно защитить.
Какую роль играет алюминий в защите железных изделий от коррозии?
Алюминий является одним из эффективных металлов для защиты железных изделий от коррозии. Он обладает высокой электрохимической активностью и способен создать защитную пленку на поверхности железа. Эта пленка защищает от контакта с окружающей средой и препятствует коррозии.
Какую пленку создает цинк на поверхности железных изделий?
Цинк создает на поверхности железных изделий защитную пленку из оксида цинка. Эта пленка защищает железо от контакта с воздухом и влагой, что препятствует коррозии. Кроме того, цинк обладает высокой электрохимической активностью и предотвращает образование электрических пар.
Какие металлы могут быть использованы в качестве анодов при использовании катодной защиты для железных изделий?
Для катодной защиты железных изделий от коррозии используют такие металлы, как магний, алюминий и цинк. Они играют роль анодов и создают электрическую связь с железом, приводя к образованию защитной пленки на его поверхности.
