Металлический тип связи является одним из основных типов химической связи в металлах. Он образуется благодаря специфическому расположению электронов в металлической решетке, что придает металлам их уникальные свойства и особенности.
В металлической решетке положительные ионы металла занимают позиции в решетке, образуя кристаллическую структуру. Особенностью металлического типа связи является наличие свободных электронов, которые перемещаются между положительно заряженными ионами. Это свободное движение электронов является основной причиной электрической и тепловой проводимости металлов.
Свободные электроны в металлическом типе связи объединяются в электронные облака, которые взаимодействуют между собой и с положительными ионами. Такое взаимодействие позволяет электронам гибко перемещаться по металлической структуре, создавая специфическую металлическую связь. Это также обеспечивает металлам высокую пластичность и способность к формованию.
Металлический тип связи обладает высокой степенью прочности и устойчивости, что позволяет металлам сохранять свою форму и структуру при различных воздействиях. Он также предоставляет металлам возможность образовывать сплавы и специальные структуры, которые обладают уникальными свойствами, например, магнитными или суперпроводящими. Металлический тип связи является одним из фундаментальных принципов, определяющих свойства и поведение металлов, и играет важную роль во многих областях науки и техники.
Определение металлического типа связи
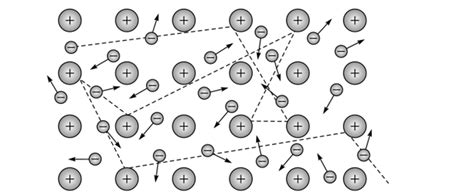
Металлический тип связи - один из основных типов химической связи в металлах. Этот тип связи обусловлен особенностями строения и взаимодействия атомов в металлической решетке.
В основе металлической связи лежит взаимное влияние положительно заряженных ионов и свободных электронов в металле. Ионы положительной заряды, являющиеся атомами металла, образуют кристаллическую решетку, в которой свободно движутся электроны. Это свободное движение электронов обеспечивает металлам их характерные свойства, такие как электропроводность и теплопроводность.
Металлическая связь обладает следующими характерными особенностями:
- Наличие общего электронного газа, состоящего из свободных электронов;
- Наличие перекрытия энергетических уровней свободных электронов с энергетическими уровнями ионов металла;
- Наличие положительного заряда ионов металла и отрицательного заряда свободных электронов, что приводит к образованию ионо-электронных пар;
- Силы металлической связи начинают действовать на межатомные расстояниях порядка 2-3 атомных радиусов, что обеспечивает металлам их механическую прочность.
Интенсивность металлической связи зависит от таких факторов, как наличие свободных электронов, заряд ионов металла и их величина, размер и форма атомов металла. В результате металлы обладают высокой теплопроводностью, электропроводностью, пластичностью и другими специфическими свойствами.
Атомная решетка в металлах
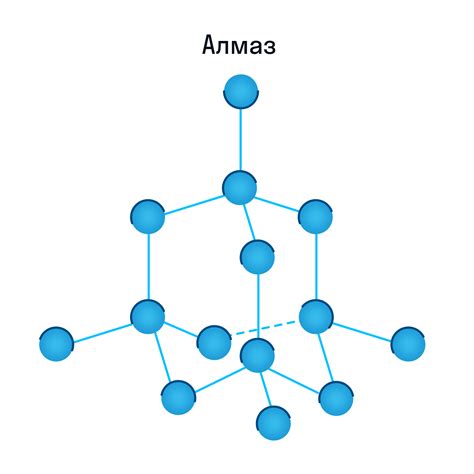
Атомная решетка в металлах является одним из основных элементов, определяющих их структуру и свойства. На микроскопическом уровне металлические материалы представляют собой кристаллическую сетку, состоящую из регулярно расположенных атомов. В отличие от молекулярной решетки, атомы в металлах обладают высокой степенью подвижности и сильной взаимодействуют друг с другом.
Атомы в металлической решетке объединены связями металлического типа, которые характеризуются общими свойствами: электронная проводимость, благодаря свободным электронам, и металлическая связь, обусловленная силой электростатического притяжения между положительно заряженными ядрами и отрицательно заряженными электронами.
Регулярная структура металлической решетки обеспечивает металлам свойства, такие как высокая пластичность и проводимость. Атомы в металле расположены в упорядоченном трехмерном пространстве, при этом каждый атом окружен ближайшими соседями, с которыми он образует кристаллическую решетку. Такая структура обеспечивает металлам высокую механическую прочность и устойчивость к деформациям.
Все металлы имеют свои характерные структуры атомных решеток, которые определяют их свойства и поведение при различных условиях. Например, металлы с кубической решеткой, такие как железо, алюминий и медь, обладают высокой твердостью и прочностью. Другие металлы, например, золото, серебро и платина, имеют кубно-гексагональную структуру, что придает им высокую пластичность и покатность.
Электронная структура металлических связей
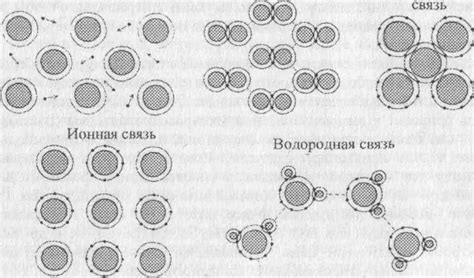
Металлические связи – это особый тип химической связи, который характерен для металлов. Этот тип связи обусловлен особенностями электронной структуры атомов в металлах.
Основной особенностью металлических связей является наличие так называемого "электронного моря". Внешние электроны металла образуют общую облако электронов, которое окружает положительные ионы металла. Такая электронная структура создает специфические свойства металлов и позволяет им обладать высокой проводимостью тепла и электричества, а также формировать ковкую структуру.
Электроны в металлических связях организуются во всевозможные энергетические уровни. Основные энергетические уровни заполняются электронами по принципу возрастания энергетического состояния. Возникновение электронного моря происходит из-за перекрытия энергетических уровней соседних атомов.
Количество электронов в металлических связях определяет химические свойства металлов. Чем выше количество электронов, тем больше энергии имеет электронное облако металла, что способствует возникновению более ковкой и прочной структуры.
Таким образом, электронная структура металлических связей определяется электронным морем, которое образуют внешние электроны металла, и влияет на физические и химические свойства металлов.
Физические свойства металлов, обусловленные металлической связью

Металлическая связь является одной из типичных форм химической связи в металлах. Она обеспечивает уникальные физические свойства, которые отличают металлы от других материалов.
В металлах электроны свободно движутся внутри кристаллической решетки. Это создает высокую электропроводность и теплопроводность металлов. Электроны, свободно перемещаясь, могут эффективно переносить электрический ток и тепловую энергию через металлический материал.
Металлическая связь также отвечает за высокую пластичность и прочность металлов. Свободные электроны слабо связаны с положительно заряженными ионами, что позволяет атомам в кристаллической решетке смещаться без определенной структурной регулярности. Благодаря этому металлы обладают способностью подвергаться деформации без разрушения и позволяют легко формировать различные изделия.
Металлическая связь также ответственна за способность металлов ведущих электропроводностью и теплопроводностью сохранять свои свойства при низких и высоких температурах. Электроны в металлической связи могут свободно перемещаться даже при экстремальных температурах, обеспечивая эффективный транспорт энергии внутри материала.
Благодаря металлической связи металлы обладают также хорошей коррозионной стойкостью. Электроны, свободно перемещаясь в металлической решетке, уравновешивают реакции окисления и восстановления, предотвращая разрушение и разложение материала при взаимодействии с внешней средой.
Химические свойства металлов, обусловленные металлической связью

Металлическая связь является специфическим типом химической связи, который обуславливает особые химические свойства металлов. Металлы обладают рядом характеристик, которые являются результатом их металлической структуры и связей между атомами.
Одним из основных свойств металлов является их высокая электропроводность. Металлическая структура предполагает наличие свободных электронов, которые могут свободно перемещаться по металлической решетке. Это позволяет металлам легко проводить электрический ток, что делает их основными материалами для производства электрических проводов и контактов.
Другое важное химическое свойство металлов - их способность образовывать ионы положительного заряда. Это связано с тем, что металлические связи обеспечивают высокую энергию ионизации - энергию, необходимую для отделения электрона от атома. Благодаря этому металлы легко образуют положительные ионы, что делает их активными в химических реакциях.
Также металлическая связь обеспечивает металлам свойство пластичности и деформируемости. Металлы могут быть легко расплавлены и отформованы, что делает их идеальными материалами для производства различных изделий и конструкций.
Важным химическим свойством металлов, обусловленным металлической связью, является также их высокая теплопроводность. Свободные электроны в металлической структуре способствуют эффективному переносу тепла, что делает металлы хорошими теплоотводящими материалами.
В зависимости от конкретного металла и условий, его химические свойства, обусловленные металлической связью, могут отличаться. Однако, в целом, металлы обладают схожими химическими свойствами, которые делают их основными строительными блоками многих веществ и конструкций в природе и промышленности.
Применение металлов с металлической связью в различных отраслях промышленности

Металлы с металлической связью, такие как железо, алюминий, медь и другие, широко применяются в различных отраслях промышленности. Они обладают высокой прочностью, хорошей проводимостью тепла и электричества, а также способностью быть легко обрабатываемыми и варимыми. В результате, эти металлы находят широкое применение в производстве различных изделий и компонентов.
Одним из основных применений металлов с металлической связью является строительство. Железобетонные конструкции, металлические каркасы зданий и мостов, металлические профили и листы используются для создания прочных и долговечных основ для различных сооружений. Также металлы широко применяются в строительстве металлических и алюминиевых конструкций, воздушных линий электропередачи, специальных металлических конструкций для нефтегазовой отрасли и т.д.
В автомобильной промышленности металлы с металлической связью находят применение в производстве кузовов, двигателей и других компонентов автомобилей. Железо используется для создания каркаса автомобиля, а алюминий обладает преимуществами низкого веса и высокой прочности, что делает его идеальным материалом для создания кузова и деталей подвески. Медь востребована в системах электропроводки и электрических компонентах, таких как провода и разъемы.
Металлы с металлической связью также широко используются в энергетической отрасли. Они являются основными материалами для создания электрических генераторов, турбин, паровых котлов и других устройств, используемых в процессах производства и передачи электроэнергии. Алюминий, благодаря своей низкой плотности и высокой проводимости, используется в производстве проводов и кабелей, а также солнечных батарей и других альтернативных источников энергии.
Наконец, металлы с металлической связью применяются в производстве различных изделий бытового назначения. Ножи из нержавеющей стали, посуда из алюминия, различные металлические инструменты и даже украшения из золота и серебра - всё это можно найти в нашей повседневной жизни благодаря металлической связи, которая придает металлам структуру и уникальные свойства.
Вопрос-ответ

В чем заключается металлический тип связи в металлах?
Металлическая связь в металлах основана на свободном перемещении электронов внутри кристаллической решетки. Это происходит из-за отсутствия тесной связи между атомами.
Какие физические свойства обусловлены металлической связью?
Металлическая связь обуславливает такие физические свойства металлов, как высокая проводимость электричества и тепла, деформируемость и пластичность, а также способность образовывать гладкие поверхности и блеск.
Как происходит образование свободных электронов в металлической связи?
Образование свободных электронов в металлах происходит благодаря отдельным электронам, которые отрываются от своих атомов и свободно передвигаются по всей кристаллической решетке.
Почему металлы хорошие проводники электричества?
Металлы являются хорошими проводниками электричества из-за наличия свободных электронов, которые могут свободно перемещаться по кристаллической решетке и переносить электрический заряд.
Какие еще свойства металлов можно объяснить металлической связью?
Металлическая связь может также объяснить высокую теплопроводность металлов, их способность отражать свет и электромагнитные волны, а также их высокую плотность. Все эти свойства определяются свободными электронами, которые легко передают энергию и взаимодействуют со светом.
