Ионная связь – одна из основных форм химической связи, проявляющаяся в образовании ионов из атомов. Это взаимодействие возникает между атомами металлов и атомами неметаллов. В процессе образования ионной связи, атомы металлов вступают в превращение, изменяя свою электронную структуру.
Атомы металлов обладают низкой электроотрицательностью и имеют малое количество электронов во внешней оболочке. Такие атомы стремятся отдать свои валентные электроны, чтобы достичь более устойчивого электронного состояния. При образовании ионной связи, атомы металлов становятся положительно заряженными ионами – катионами.
Превращение атомов металлов при образовании ионной связи связано с потерей валентных электронов. В результате этого процесса, металлические атомы становятся положительно заряженными. Они отдают свои электроны неметаллам, образуя кристаллическую решетку и образцы сетки кристаллов. В общем случае, число электронов, отданных атомом металла, равно числу электронов в его внешней оболочке. Для атомов, имеющих несколько валентных электронов, превращение может происходить в несколько этапов.
Таким образом, при образовании ионной связи атомы металлов претерпевают превращение, меняя свое электронное состояние. Отдавая свои валентные электроны, атомы металлов приобретают положительный заряд и становятся катионами. Эти катионы затем образуют кристаллическую решетку ионов, которая стабильна и обладает множеством полезных свойств, таких как прочность и электропроводность.
Образование ионной связи: превращение атомов металлов

Образование ионной связи - один из способов, которым атомы металлов могут взаимодействовать друг с другом. При образовании ионной связи, атомы металлов теряют один или несколько электронов и превращаются в положительно заряженные ионы.
Процесс образования ионной связи происходит благодаря разности электроотрицательностей между металлическим и неметаллическим элементами. В результате, электроотрицательный неметалл притягивает электроны от металла, образуя отрицательно заряженный ион. Металлический элемент, в свою очередь, становится положительно заряженным ионом.
Получившиеся ионы с противоположными зарядами притягиваются друг к другу и образуют заряженные агрегаты - ионы. Такие агрегаты обладают высокой структурной устойчивостью и формируют кристаллическую решетку в ионных соединениях.
Ионная связь обладает рядом особенностей, которые определяют ее химические и физические свойства. Ионные соединения обычно обладают высокой температурой плавления и кипения, хорошей электропроводностью в расплавленном или растворенном состоянии, а также хрупкостью и краткосрочностью.
Важно отметить, что образование ионной связи относится к одному из способов взаимодействия металлов с другими элементами. Кроме ионной связи, металлы могут образовывать и другие типы химических связей, такие как ковалентная связь или металлическая связь.
Важность ионной связи
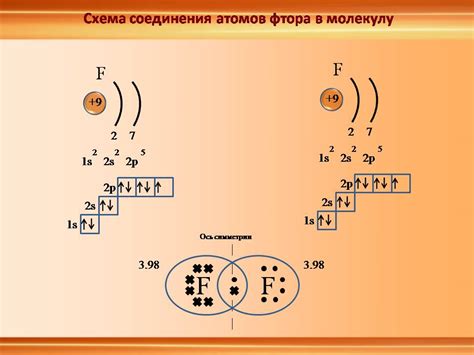
Ионная связь – один из основных видов связи в химии, и ее важность в неорганической и органической химии трудно переоценить. Она играет ключевую роль во множестве процессов и явлений, влияет на физические и химические свойства веществ.
Ионная связь возникает между атомами, когда один атом отдает один или несколько электронов другому атому. В результате образуются положительно и отрицательно заряженные ионы, которые притягиваются друг к другу. Именно эта притяжение ионов и обеспечивает устойчивость соединений и их особые свойства.
Важность ионной связи проявляется во множестве аспектов. Во-первых, именно благодаря ионной связи возможно образование структуры кристаллов, которая определяет многие физические свойства веществ, например, твердотельную проводимость или влияние на оптические свойства. Во-вторых, ионная связь обуславливает растворимость многих соединений, и является основой для реакций растворения. Это важно для процессов, связанных с жизнедеятельностью организмов, так как позволяет растворять ионные вещества в телевой жидкости и использовать частицы, необходимые для различных функций.
Таким образом, ионная связь является неотъемлемой частью химии и играет важную роль в объяснении и понимании различных явлений и свойств веществ. Ее изучение позволяет лучше разобраться в химических взаимодействиях, а также применять полученные знания в практической деятельности, например, в современных технологиях и процессах.
Атомы металлов и их свойства

Атомы металлов являются основными строительными блоками металлических материалов и обладают рядом уникальных свойств. Одно из ключевых свойств атомов металлов - высокая электропроводность. Это связано с наличием свободных электронов, которые легко передают электрический ток.
Другое важное свойство атомов металлов - высокая теплопроводность. Это объясняется высокой подвижностью электронов в кристаллической решетке металла, что позволяет быстро передавать тепловую энергию.
Атомы металлов также обладают высокой пластичностью, то есть способностью претерпевать деформацию без разрушения. Это связано с наличием групп электронов с особыми энергетическими состояниями, которые обеспечивают металлам способность к механической обработке.
Более сложные свойства атомов металлов связаны с их способностью образовывать ионные связи с атомами неметаллов. При образовании ионной связи, электроотрицательные атомы неметаллов захватывают электроны у металлических атомов, образуя отрицательно заряженные анионы, в то время как металлические атомы образуют положительно заряженные катионы.
Процесс образования ионной связи
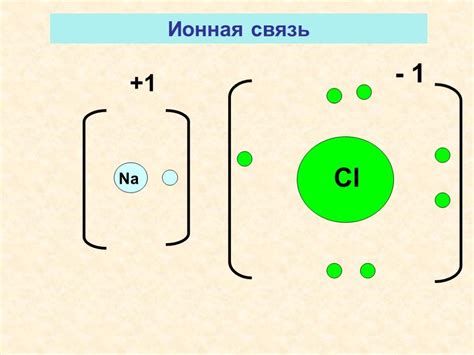
Ионная связь - это тип химической связи, который возникает между атомами металлов и неметаллов. В ходе образования ионной связи происходит передача электронов от металла к неметаллу.
Процесс начинается с образования положительно заряженных ионов на поверхности металла. Это происходит путем отрыва электронов от атомов металла, образуя катионы.
Затем образованные катионы притягивают негативно заряженные атомы неметалла, что приводит к образованию анионов.
Таким образом, образовывается кристаллическая структура, где положительно заряженные ионы расположены в решетке и притягиваются к отрицательно заряженным ионам.
Ионная связь обладает высокой электропроводностью в расплавленном или растворенном состоянии, так как ионы могут свободно перемещаться и создавать электрический ток.
Роль электронов в ионной связи
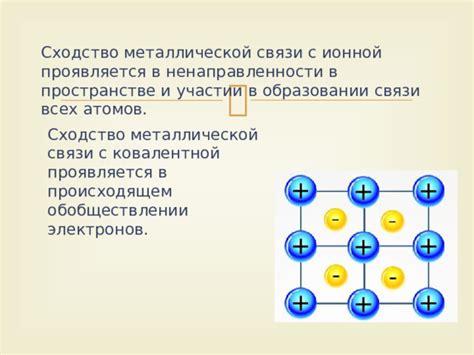
Электроны являются главными участниками образования ионной связи между атомами металлов. Эти небольшие заряженные частицы играют важную роль в структуре и свойствах ионных соединений.
При образовании ионной связи, атомы металлов отдают один или несколько электронов из своей внешней оболочки, образуя положительно заряженные ионы, называемые катионами. Электроны, отданные металлическими атомами, становятся свободными электронами, которые образуют "облако" электронов в общей структуре.
Катионы, образованные металлическими атомами, притягиваются к свободным электронам в облаке, создавая прочную и устойчивую ионную решетку. За счет электронов в своей структуре, ионные соединения обладают характеристиками, такими как высокая температура плавления и кипения, хорошая проводимость электричества и тепла.
Электроны в ионной связи также обладают высокой подвижностью. Они могут перемещаться в облаке электронов, что позволяет ионным соединениям проявлять электронаявную проводимость. Вещества с ионной связью могут быть твердыми, жидкими или газообразными в зависимости от формы и структуры ионной решетки.
Особенности образования ионной связи у металлов
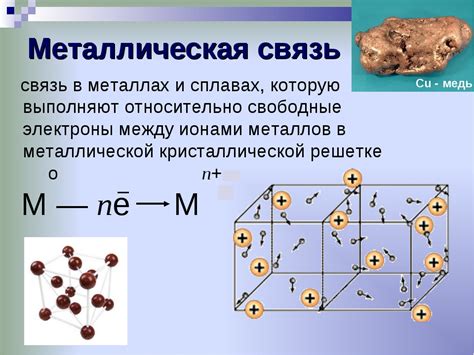
Ионная связь – это один из видов связей между атомами, в котором происходит образование положительно и отрицательно заряженных ионов. В отличие от ковалентной связи, где электроны общие для атомов, при ионной связи электроны полностью передаются с одного атома на другой. У металлов образование ионной связи имеет свои особенности.
Металлы обладают характерной структурой, называемой кристаллической. В ней атомы расположены регулярно в трехмерной решетке, образуя кристаллическую решетку. Большинство атомов в металлах имеют свободные электроны в валентной оболочке. Эти электроны легко участвуют в образовании ионной связи.
Когда металлы вступают в реакцию с неметаллами, их атомы отдают свои электроны, становясь положительно заряженными ионами – катионами. Неметаллы, в свою очередь, принимают эти электроны и образуют отрицательно заряженные ионы – анионы. Положительные и отрицательные ионы притягиваются друг к другу электростатической силой и образуют ионную связь.
Ионная связь у металлов имеет ряд особенностей. Поскольку в металлах есть свободные электроны, кристаллическая решетка становится общей для всех атомов металла. Свободные электроны образуют так называемое «электронное облако», которое окружает положительные ионы. Это электронное облако является проводником электричества и тепла.
Ионная связь у металлов обладает высокой прочностью и пластичностью. Кристаллическая решетка позволяет атомам металлов сдвигаться друг относительно друга без разрушения связей. Именно благодаря этой особенности металлы обладают высокой упругостью и пластичностью, что делает их идеальным материалом для производства различных изделий и конструкций.
Применение ионной связи в технологиях

Ионная связь – это особый тип химической связи, основанный на притяжении противоположно заряженных ионов. В металлургии и химической промышленности ионная связь находит широкое применение.
Одним из примеров применения ионной связи является вопрос обработки руды для получения металлов. Руды часто содержат металлы в виде оксидов или сульфидов, которые нужно превратить в ионы для образования металлического элемента. Для этого применяют различные технологии, включающие растворение руды в кислотах или лугах с последующим осаждением металлических ионов.
Ионная связь также используется в электрохимии. Примером может служить процесс гальванического покрытия, при котором ионы металла откладываются на поверхности предмета под воздействием электрического тока. Это позволяет изменить свойства поверхности, придав ей дополнительную прочность, стойкость к коррозии или декоративность.
Другим примером использования ионной связи может быть процесс синтеза кристаллов. Путем применения высоких температур и давления ионные кристаллы могут быть получены из смесей соответствующих ионов. Это позволяет создавать материалы с определенными оптическими или электронными свойствами, которые находят применение в различных областях науки и техники.
Таким образом, ионная связь является важным инструментом в различных технологиях. Ее применение позволяет получать металлы из руды, проводить электрохимические процессы, создавать новые материалы с уникальными свойствами. Благодаря этому, ионная связь играет важную роль в современной промышленности и научных исследованиях.
Вопрос-ответ

Что происходит с атомами металлов при образовании ионной связи?
При образовании ионной связи атомы металлов теряют электроны и превращаются в положительно заряженные ионы.
Каким образом происходит превращение атомов металлов при образовании ионной связи?
Превращение атомов металлов при образовании ионной связи происходит путем отдачи одного или нескольких электронов, что приводит к образованию положительно заряженных ионов металла.
Почему атомы металлов теряют электроны при образовании ионной связи?
Атомы металлов теряют электроны при образовании ионной связи, потому что у них относительно низкая электроотрицательность. Таким образом, они готовы отдать свои электроны другим атомам с высокой электроотрицательностью, чтобы достичь более стабильной электронной конфигурации.
Какие ионы образуются при превращении атомов металлов при образовании ионной связи?
При превращении атомов металлов при образовании ионной связи образуются положительно заряженные ионы металла. Например, натриевый атом (Na) теряет один электрон и превращается в положительно заряженный натриевый ион (Na+).
