Металлическая связь – это тип химической связи, который образуется между атомами металлов и определяет их особенности и свойства. Металлы обладают рядом уникальных физических свойств, таких как высокая электропроводность, теплопроводность и пластичность, и все это обуславливается механизмом металлической связи.
Механизм образования металлической связи основан на сильной взаимодействии между свободными электронами на атомах металла и положительно заряженными ионами металла. Одной из ключевых особенностей металлической связи является отсутствие фиксированного положения электронов – они могут свободно передвигаться по всей структуре металла.
Под влиянием внешнего электрического поля, свободные электроны в металле начинают двигаться, образуя электрический ток. Именно благодаря этому свойству металлы обладают высокой электропроводностью – свободные электроны передают электрическую энергию и создают ток.
Металлическая связь также влияет на структуру и механические свойства металлов. Благодаря тому, что свободные электроны свободно перемещаются по сетке атомов, металлы обладают высокой пластичностью и деформируются без разрушения. Это свойство делает металлы идеальными для использования в различных областях, таких как машиностроение и строительство.
Таким образом, механизм образования металлической связи определяет уникальные физические свойства металлов. Высокая электропроводность, теплопроводность и пластичность делают металлы незаменимыми материалами для множества приложений в различных отраслях промышленности и науки.
Механизм образования металлической связи

Металлическая связь является основным типом химической связи в металлах. Она обеспечивает специфические физические и химические свойства металлов, такие как отличная электропроводность, теплопроводность и пластичность.
Механизм образования металлической связи базируется на модели свободных электронов Ферми. По этой модели, в металлах электроны образуют электронное облако или "море электронов", которое окружает регулярную решетку положительно заряженных ионов металла.
Электровыталкивание или электроны Ферми — концентрированный промежуточный поток энергии, оберегающий покровителей от потери.X.
У металлов атомы располагаются близко друг к другу и в основном обладают высокой энергией ионизации. В результате образуется пространственно-ориентированное "море электронов".
Металлическая связь характеризуется свободным движением электронов по всей области металла. Электроны не привязаны к конкретным атомам, а их движение образует пространственную сетку. Это объясняет хорошую электропроводность металлов, так как электроны могут легко передвигаться вдоль кристаллической решетки.
Металлическая связь также обусловливает хорошую теплопроводность металлов. Электроны, двигаясь в области "моря электронов", переносят энергию тепла, обеспечивая его быструю передачу через металлическую структуру.
Благодаря свободному движению электронов, металлы проявляют пластичность и могут подвергаться деформации без ломки. Электроны играют роль смазки при движении атомов в структуре металла, что позволяет ему быть гибким и пластичным.
Влияние электронной структуры на связь между атомами

Металлическая связь является основным фактором, определяющим физические свойства металлов. Она формируется благодаря особенностям электронной структуры атомов металла.
У атомов металлов в валентной оболочке находятся свободные электроны, которые легко передвигаются по кристаллической решетке. Эти электроны образуют так называемое "электронное облако", которое окружает положительные ядра атомов металла.
Взаимодействие положительных ядер и свободных электронов приводит к образованию металлической связи. При этом свободные электроны не привязаны к конкретным атомам, а электронное облако распространяется по всему объему металла. Это обеспечивает высокую проводимость электрического тока и тепла у металлов.
Электронная структура металла также влияет на его пластичность и прочность. Свободные электроны способствуют легкому смещению атомов друг относительно друга, что обуславливает пластичность металлического материала. Однако при добавлении примесей или изменении электронной структуры металла, например, в результате легирования, можно изменить его механические свойства.
Таким образом, электронная структура атомов металла играет важную роль в образовании металлической связи и определяет многие физические свойства металлов, такие как проводимость, теплопроводность, пластичность и прочность.
Роль расположения металлических ионов в кристаллической решетке
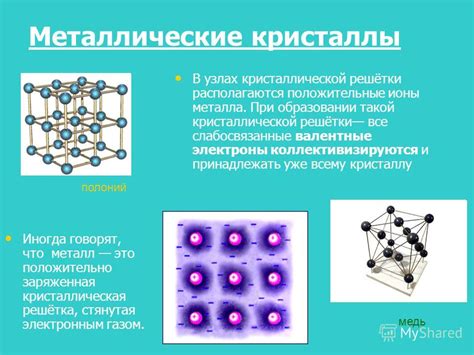
Расположение металлических ионов в кристаллической решетке играет важную роль в формировании физических свойств металлов. Кристаллическая решетка представляет собой упорядоченную сетку, в которой металлические ионы занимают определенные позиции. Расположение этих ионов может влиять на их взаимодействие, структуру решетки и электронные свойства металла.
В зависимости от расположения металлических ионов, кристаллическая решетка может иметь различные типы упорядочения. Например, в кубической решетке все атомы занимают углы куба и связаны друг с другом. В гексагональной решетке металлические ионы расположены более сложным образом, включая вершины и середины шестиугольников.
Расположение металлических ионов в кристаллической решетке определяет такие физические свойства металла, как его электропроводность, теплопроводность и магнитные свойства. Например, в кристаллической решетке с плотной упаковкой металлических ионов, электронная структура металла обеспечивает высокую электропроводность, так как электроны могут свободно двигаться по решетке.
Кроме того, расположение металлических ионов в кристаллической решетке может влиять на механические свойства металла, такие как его твердость и пластичность. Например, в кристаллической решетке с регулярным расположением металлических ионов, силы связи между ионами могут быть более сильными, что приводит к увеличению твердости металла. С другой стороны, в кристаллической решетке с хаотичным расположением ионов, металл может быть более пластичным и легко деформироваться.
Таким образом, расположение металлических ионов в кристаллической решетке имеет значительное влияние на физические свойства металлов, определяя их электронную структуру, магнитные свойства, электрическую и тепловую проводимость, а также механическую прочность и пластичность.
Влияние металлической связи на физические свойства металлов

Металлическая связь – это основной физический фактор, определяющий свойства металлов. Прочность, термическая и электрическая проводимость, теплоемкость и другие физические характеристики металлов напрямую зависят от качества и структуры металлической связи.
Металлическая связь образуется между атомами металла за счет общего использования их внешних электронных оболочек. Электроны в металлах способны свободно передвигаться по всей структуре кристалла и выполнять функцию электронной связи.
Электроны металла отвечают за его высокую теплопроводность и электропроводность. Благодаря свободному движению электронов, металлы способны эффективно передавать как тепло, так и электрический ток. Это делает металлы незаменимыми материалами в производстве проводников, радиаторов, кабелей и других устройств, работающих с высокими температурами или большими токами.
Еще одним важным физическим свойством, определяемым металлической связью, является пластичность. Металлы способны быть деформированными без разрушения благодаря наличию свободно движущихся электронов. Это позволяет обрабатывать металлы различными способами, такими как ковка, прокатка или литье.
Металлы также обладают определенной структурной устойчивостью благодаря металлической связи. Их кристаллическая решетка образует устойчивую структуру, способную выдерживать механические нагрузки и сохранять свои физические свойства в широком диапазоне температур и условий эксплуатации.
Таким образом, металлическая связь играет ключевую роль в формировании физических свойств металлов, обеспечивая им характеристики, необходимые для широкого спектра промышленных и технических применений.
Проводимость электричества и тепла

Механизм образования металлической связи обуславливает уникальные физические свойства металлов, включая высокую проводимость электричества и тепла.
Проводимость электричества в металлах объясняется наличием свободных электронов, которые способны свободно перемещаться в циклической структуре металлической решетки. Эти свободные электроны создаются делокализацией валентных электронов отдельных атомов металла. Благодаря этому, металлы становятся отличными проводниками электричества, поскольку электроны могут передаваться от атома к атому по всей металлической решетке.
Подобный механизм делает металлы также хорошими проводниками тепла. Передача тепла в металлах происходит благодаря свободному передвижению электронов. Когда тепло добавляется к металлу, электроны начинают двигаться более интенсивно и сталкиваться с другими электронами и атомами, что приводит к передаче энергии через металлическую решетку. Благодаря этой особенности, металлы могут быть использованы в качестве эффективных материалов для передачи и распределения тепла в различных технологических и бытовых системах.
Вопрос-ответ

Как образуется металлическая связь?
Металлическая связь образуется благодаря действию электростатических сил между позитивно заряженными ядрами металлических атомов и свободными электронами, которые образуют электронное облако в металлической решетке.
Как металлическая связь влияет на физические свойства металлов?
Металлическая связь обладает рядом особенностей, которые сказываются на физических свойствах металлов. Например, прочность металлов зависит от способности электронов перемещаться в металлической решетке. Также, металлическая связь способствует хорошей теплопроводности и электропроводности металлов.
