Цинк и магний являются двумя химическими элементами, которые активно взаимодействуют с водой при обычных условиях. Эти металлы отличаются своими химическими свойствами, что приводит к различным реакциям при контакте с водой. Оба элемента имеют большое значение в промышленности и научных исследованиях, а также имеют важную роль в живых организмах.
Цинк, химический элемент с атомным номером 30, имеет серебристо-серый цвет и является одним из наиболее распространенных металлов в земной коре. Он обладает химической активностью и взаимодействует с водой, образуя гидроксид цинка и выделяяся в виде ионов Zn2+. Эта реакция не происходит самопроизвольно, но может быть существенно ускорена при наличии кислорода или кислоты.
Магний, химический элемент с атомным номером 12, имеет серебристый цвет и является легким металлом. Вода реагирует с магнием, образуя гидроксид магния и выделяя водород. Эта реакция происходит быстро и является спонтанной, особенно при повышенной температуре или взаимодействии с кислотами. Магний играет важную роль в живых системах, являясь одним из важнейших элементов в составе хлорофилла в растениях и в металлохелатозах в организмах животных.
Отношения цинка с водой

Цинк является химическим элементом переходной группы, который обладает высокой химической активностью. При взаимодействии с водой цинк может проявлять различные реакции в зависимости от условий среды.
При обычных условиях цинк реагирует с водой с образованием щелочных гидроксидов: Zn + 2H2O -> Zn(OH)2 + H2. Эта реакция протекает достаточно медленно, особенно на поверхности цинка, так как образующийся гидроксид образует защитную пленку на металлической поверхности.
В некоторых случаях, при наличии кислорода и определенных примесей, цинк может реагировать с водой более активно. Например, при наличии ионов кислорода и хлора образуется гидроксоксихлорид цинка: Zn + 2H2O + Cl2 -> Zn(OH)Cl + H2.
Также цинк может реагировать с водой при повышенных температурах или в присутствии кислот. Например, при взаимодействии с сильными кислотами, такими как серная или азотная, образуются соответствующие соли и высвобождается водород: Zn + H2SO4 -> ZnSO4 + H2.
В целом, отношения цинка с водой являются комплексными и зависят от множества факторов, таких как состояние поверхности металла, наличие примесей и условия окружающей среды.
Взаимодействие металла цинк с водой в обычных условиях
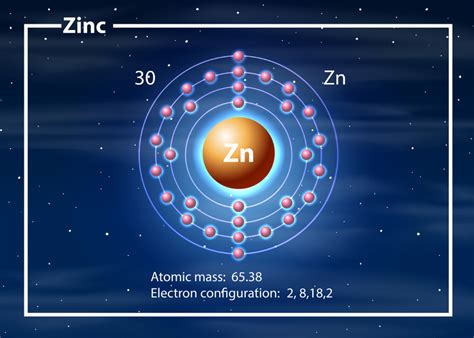
Цинк – химический элемент, который можно обнаружить в различных компонентах нашей повседневной жизни, будь то строительные материалы, электроды или покрытия. Вода также является средой, с которой цинк может взаимодействовать.
При обычных условиях цинк нереактивен с водой, то есть не растворяется в ней и не отдает электроны для образования ионов. Благодаря своей стабильности он образует на поверхности металла защитную пленку, называемую оксидом цинка, которая препятствует дальнейшему контакту с водой.
Однако, при высоких температурах или в присутствии кислорода, реакция между цинком и водой все же может происходить. В результате такой реакции вода может диссоциироваться, то есть разложиться на водород и кислород. Возникающий водород может образовывать пузырьки, которые видны на поверхности металла. Эта реакция помогает очищать металл от оксида цинка и предотвращает его коррозию.
Интересно, что взаимодействие цинка с водой является основой работы некоторых батарей, которые используются в нашей повседневной жизни, например, в батарейках. Там цинк служит в качестве отрицательного электрода, а вода – в качестве электролита. Таким образом, взаимодействие цинка с водой имеет не только химическую, но и практическую пользу.
Реакции цинка и воды при стандартных условиях
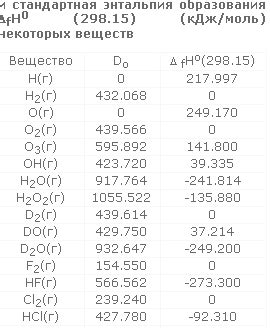
Цинк является активным металлом и реагирует с водой при стандартных условиях. В результате взаимодействия цинка с водой образуется оксид цинка (ZnO) и водород.
Уравнение реакции выглядит следующим образом:
Zn + 2H2O → ZnO + H2
Реакция происходит со значительной выделением водорода, поэтому цинк при контакте с водой активно выделяет пузырьки газа и быстро растворяется.
Реакция цинка с водой является экзотермической, т.е. сопровождается выделением тепла. Образование оксида цинка является причиной белого осадка на поверхности металла.
Эта реакция является химически активной и быстро протекает при комнатной температуре. Однако, погружение цинка в воду может происходить медленно и без видимого заметного эффекта, если на поверхности металла присутствует пассивная пленка оксида или других примесей. В таком случае, необходимо активировать металл, например, обрабатывая его поверхность разбавленной кислотой для удаления пассивной пленки.
Существенные особенности при взаимодействии цинка и воды

Цинк является химическим элементом из группы переходных металлов, который обладает несколькими особенностями при взаимодействии с водой.
Во-первых, цинк реагирует с водой, но реакция протекает медленно при обычных условиях. При взаимодействии с водой цинк образует гидроксид цинка (Zn(OH)2), который не очень растворим в воде. Это обусловливает медленность реакции и незначительность образования гидроксида цинка.
Во-вторых, взаимодействие цинка с водой происходит с выделением водорода. Цинк при этом выступает в качестве активного металла, который обладает способностью вытеснять водород из воды. Это иллюстрирует химическое уравнение реакции: Zn + 2H2O → Zn(OH)2 + H2.
В-третьих, реакция цинка с водой происходит с образованием щелочной среды. Гидроксид цинка, образующийся в результате взаимодействия цинка с водой, является основанием и обладает щелочными свойствами. Это объясняет повышение pH воды при добавлении цинка.
Таким образом, взаимодействие цинка и воды происходит медленно, с выделением водорода и образованием щелочной среды. Эти особенности играют важную роль в различных приложениях, таких как производство водорода и использование цинка в щелочных элементах.
Воздействие магния на воду

Магний является активным химическим элементом, который может взаимодействовать с водой при обычных условиях. При контакте с водой, магний начинает проявлять свои реакционные свойства.
Одной из характеристик взаимодействия магния с водой является его способность реагировать прямо с водой, образуя гидроксид магния (Mg(OH)2). Гидроксид магния обладает щелочными свойствами и может быть использован в качестве антацидов, что помогает снизить кислотность в желудке.
Вода также способствует окислению магния, образуя оксид (MgO) и гидроксид (Mg(OH)2). Эти соединения магния могут иметь различные применения в химической промышленности, в производстве керамики и в других отраслях.
Важно отметить, что вода может ускорить процесс коррозии магния, особенно в присутствии растворенных солей и кислот. Это связано с электрохимическими свойствами магния и его склонностью к окислению.
Таким образом, взаимодействие магния с водой обладает как отрицательными (коррозия), так и положительными (образование гидроксида) сторонами и может быть используется в различных сферах науки и промышленности.
Вопрос-ответ

Какие особенности есть во взаимодействии цинка с водой?
Цинк при обычных условиях не реагирует с водой. Однако, при нагревании цинк начинает образовывать водородный газ и оксид цинка.
Что происходит при взаимодействии магния с водой?
Магний при обычных условиях также не реагирует с водой. Однако, при нагревании магний может образовывать водородный газ и оксид магния.
Какие реакции могут происходить при взаимодействии цинка и магния с водой?
Нагревание цинка и магния с водой может привести к образованию водородного газа и соответствующих оксидов металлов. Например, при нагревании цинка с водой образуется гидроксид цинка (Zn(OH)2) и водород (H2), а при нагревании магния с водой образуется гидроксид магния (Mg(OH)2) и водород (H2).
