Металлы являются одними из наиболее распространенных элементов в природе и часто используются в различных областях жизни человека. Однако, несмотря на их широкое применение, металлы имеют свойство подвергаться окислению - реакции с кислородом воздуха, которая приводит к их порче и разрушению. Но металлы также могут проявлять восстановительное действие - способность передавать электроны и протекать в реакциях окисления-восстановления.
Уникальное свойство металлов - их способность к восстановлению - обусловлено специфической структурой и атомной структурой. Металлическая структура, состоящая из слоев атомов, обеспечивает легкое движение электронов, что является основой их восстановительной активности. При этом, разные металлы имеют различную склонность к окислению и восстановлению, что связано с их электрохимическим потенциалом.
Окислительное и восстановительное действие металлов играют важную роль во множестве процессов, включая химические реакции, электрохимические процессы, коррозию и защиту металлов от коррозии. Знание этих свойств металлов позволяет эффективно использовать их в различных сферах деятельности, включая промышленность, медицину, энергетику и многое другое.
Металл: вечный окислитель или непреодолимый восстановитель?
Металлы, будучи активными элементами, могут проявлять как окислительные, так и восстановительные свойства в химических реакциях. Окислительные свойства проявляются, когда металлы активно вступают в реакцию с другими веществами, отдавая электроны. Восстановительные свойства, напротив, демонстрируются, когда металлы поглощают электроны и тем самым восстанавливают другие вещества.
Металлы, такие как алюминий и железо, обладают сильными окислительными свойствами. Они реагируют с кислородом из воздуха, образуя оксиды, которые являются стойкими и прочными соединениями. Например, алюминий вступает в реакцию с кислородом, образуя оксид алюминия, который образует защитную пленку на поверхности металла и предотвращает дальнейшюю окислительную реакцию.
С другой стороны, металлы такие как медь и серебро, обладают сильными восстановительными свойствами. Они способны отдавать электроны химическим соединениям, восстанавливая их. Например, медь может восстанавливать двухвалентное железо в трехвалентное, что делает ее полезной в промышленности и медицине.
Значит, металлы могут быть как окислителями, так и восстановителями в зависимости от условий, в которых они находятся. Окружающая среда, температура, концентрация веществ и другие факторы могут влиять на их химические свойства и способность вступать в реакции. Поэтому, выбирая металл для определенного применения, необходимо учитывать его окислительные или восстановительные свойства.
Металл и окисление: вечная борьба
Металлы - это не только прочные и долговечные материалы, но и вечные борцы с окислением. Окисление - это процесс, когда металл взаимодействует с кислородом из окружающей среды и образует оксидную пленку на своей поверхности. Эта пленка является причиной коррозии, что ведет к разрушению металла.
Большинство металлов имеют свойство быть окислительными или восстановительными в зависимости от условий окружающей среды. Например, железо и алюминий легко окисляются на воздухе и покрываются слоем ржавчины или оксида. Однако, некоторые металлы, такие как золото и платина, не подвержены окислению и сохраняют свой блеск и качества на протяжении длительного времени.
Окисление металлов является неизбежным процессом, который может быть замедлен или предотвращен с помощью различных методов защиты. Как правило, металлы, покрытые защитным слоем, будь то краска или покрытие из другого металла, менее подвержены окислению. Отсюда следует, что правильное использование защитных покрытий помогает сохранить металл в хорошем состоянии на протяжении длительного времени.
Окисление - процесс, который может привести к серьезным проблемам и повреждениям металлов, особенно в условиях высокой влажности или агрессивной среды. Поэтому необходимо принимать меры по защите металлов для предотвращения окисления и обеспечения их долговечности. Удачная борьба с окислением - это вечная задача для металлургии и промышленности, и только при использовании правильных методов и технологий можно достичь устойчивого развития и сохранения металлических материалов.
Реакция металла с кислородом и образование оксидов

Кислород является одним из наиболее активных химических элементов, и его реакция с металлами приводит к образованию соединений, называемых оксидами. Оксиды - это понятие, обозначающее химические соединения, в состав которых входит кислород.
В результате реакции металла с кислородом, окисление металла происходит за счет передачи электронов от металла к кислороду. Естественно, при этом процессе металл выступает в качестве восстановителя, а кислород - в качестве окислителя.
Процесс образования оксидов может протекать в различных условиях. Например, металлы могут реагировать с атмосферным кислородом при обычной температуре и давлении. Возможна также реакция металла с кислородом в составе оксидной пленки, образующейся на поверхности металла при взаимодействии с влажностью и кислородом.
Реакция металла с кислородом и образование оксидов играют важную роль в промышленности и в повседневной жизни. Некоторые оксиды имеют полезные свойства и широко используются в различных отраслях, например в производстве стекла или в качестве катализаторов. Другие оксиды металлов являются коррозионно-стойкими и применяются для защиты металлических конструкций от воздействия окружающей среды.
Металл и восстановительные свойства

Восстановительные свойства являются одной из важных характеристик металлов. Металлы, благодаря своей структуре и особенностям атома, как правило, имеют возможность передавать электроны и выполнять функцию восстановителя в химических реакциях.
Восстановление - это химическая реакция, в результате которой происходит передача электронов от вещества, называемого восстанавливающим агентом, к веществу, называемому окислителем. Восстановительные свойства металлов обусловлены наличием свободных электронов в их внешней электронной оболочке.
Когда металл вступает в реакцию восстановления, он теряет один или несколько электронов, превращаясь в положительно заряженный ион. Это явление в химии называется окислением. В то же время, окислитель - вещество, с которым металл реагирует, приобретает эти электроны и становится отрицательно заряженным - это восстановление.
Восстановительные свойства металлов широко используются в различных областях, таких как электрохимия, электротехника, металлургия и другие. Металлы играют важную роль в батареях, аккумуляторах, проводах и других устройствах, где необходим процесс передачи электронов.
Применение металлов в окислительных и восстановительных процессах
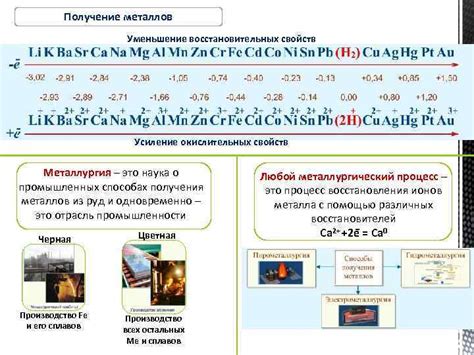
Металлы широко применяются как окислители и восстановители в различных процессах. Взаимодействие металлов с другими веществами может протекать как в окислительных, так и в восстановительных реакциях.
В окислительных процессах металлы могут отдавать свои электроны и приобретать положительный заряд. Окислительные свойства металлов проявляются при вступлении в реакцию с веществами, которые способны принять электроны, например, неметаллами или соединениями, содержащими неметаллы.
Восстановительные свойства металлов проявляются, когда они способны принимать электроны от других веществ. Такие процессы важны, например, в электрохимии, где металлы играют роль катодов и принимают электроны с анода.
Применение металлов в окислительных и восстановительных процессах широко распространено в промышленности. Многие металлы используются в производстве батарей, аккумуляторов и электродов. Например, в серебряно-цинковых батареях серебро является окислителем, а цинк - восстановителем. Также металлы применяются в процессах гальванизации, где они служат восстановителями и окислителями, позволяя создавать покрытия и защищать металлические поверхности.
Таким образом, металлы имеют важное значение в окислительных и восстановительных процессах, наряду с другими веществами, и являются незаменимыми компонентами в различных сферах деятельности человека.
Вопрос-ответ

Какие металлы обычно проявляют окислительные свойства?
Некоторые из самых распространенных металлов, которые проявляют окислительные свойства, включают алюминий, железо и медь.
Что значит, что металл может быть восстановителем?
Восстановительное свойство металла означает, что он способен переходить в более низкую степень окисления, передавая электроны другим веществам.
Как металлы взаимодействуют с кислородом?
Металлы могут взаимодействовать с кислородом, проявляя окислительные свойства. Например, железо может окисляться и ржаветь при воздействии кислорода.
