Водородные электрохимические системы – это передовые технологии, которые играют важную роль в различных сферах нашей жизни. Одним из ключевых компонентов таких систем является металл. Металлы применяются в этих системах для производства и хранения водорода, который является чистым и экологически безопасным источником энергии.
Применение металла в водородных электрохимических системах позволяет решить проблему хранения и транспортировки водорода, которая является одной из основных преград на пути к широкому использованию этого элемента как альтернативного источника энергии. Металлы, такие как железо, магний и алюминий, могут активно взаимодействовать с водородом и вступать с ним в химические реакции, образуя металлогидриды – соединения, в которых водород служит носителем энергии.
Металлогидридные системы на основе металлов широко применяются в промышленности, автомобильной отрасли, энергетике и других сферах. Они обладают такими преимуществами, как высокая энергетическая плотность, долгий срок службы, экологическая безопасность и возможность быстрого заправления. Кроме того, эти системы могут использоваться как альтернативные источники энергии в случае отключения основного энергетического источника.
Применение металла при использовании водородных электрохимических систем

Металлы играют важную роль в водородных электрохимических системах, таких как водородные генераторы и топливные элементы. Они используются в качестве катализаторов, электродов и структурных материалов, обеспечивая эффективную и стабильную работу данных систем.
Одним из ключевых применений металла в водородных электрохимических системах является его использование в качестве катализатора. Металлы, такие как платина, никель и родий, обладают высокой активностью при реакции водорода с кислородом или другими веществами. Они способствуют эффективному разложению воды на кислород и водород в электролизере, а также обратной реакции в топливной ячейке.
Кроме того, металлы используются в водородных электрохимических системах в качестве электродов. Например, в топливных элементах, металлы являются основными материалами для анода и катода. Металлические электроды обладают высокой проводимостью, что позволяет эффективно передавать электроны между электродами и реагентами.
Для обеспечения структурной прочности и долговечности водородных электрохимических систем также используются металлы. Металлические материалы обладают высокой механической прочностью и устойчивостью к окружающей среде, что позволяет им выдерживать экстремальные условия работы системы, такие как высокие температуры и агрессивные реагенты.
Таким образом, применение металла в водородных электрохимических системах является неотъемлемым элементом для обеспечения их эффективности и надежности. Металлы выполняют различные функции, включая катализ, проводимость электронов и структурную поддержку, что делает их необходимыми компонентами данных систем.
Роль металла в процессе электролиза воды
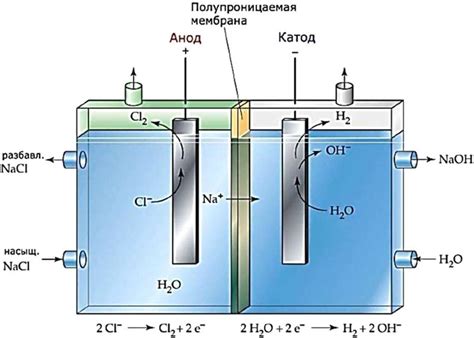
Металл играет важную роль в процессе электролиза воды, который является одним из ключевых методов для получения водорода. Электролиз воды основан на разложении молекул воды на составляющие ионы – катионы водорода и анионы кислорода – под воздействием электрического тока.
Металлы с высокой электропроводностью, такие как платина, золото или никель, используются в роли электродов в электролизере. Электроды в электролизере состоят из катода и анода, разделенных электролитом. Катод обеспечивает приток электронов, которые используются для редукции ионов водорода, а анод обеспечивает отток электронов, которые используются для окисления ионов кислорода.
Выбор металла для электрода играет решающую роль в эффективности процесса электролиза. Металл должен обладать низкой активностью в отношении химических реакций с водородом и кислородом, чтобы избежать нецелевых процессов. Также металл должен обладать высокой стойкостью к агрессивному окружающему среду и обладать достаточной электропроводностью для эффективного транспортирования электронов.
Кроме того, металлы могут быть использованы в виде катализаторов, чтобы ускорить скорость химической реакции электролиза воды. Катализаторы могут позволить снизить потребляемую энергию и повысить эффективность процесса. Металлы, такие как платина, их продукты либо их соединения, доказали свою эффективность в качестве катализаторов для электролиза воды.
Вопрос-ответ

Какова роль металла в водородных электрохимических системах?
Металл играет важную роль в водородных электрохимических системах, таких как водородные топливные ячейки. Он используется как катализатор при электролизе воды, разлагая ее на водород и кислород. Кроме того, металлы могут быть использованы в качестве электродов в водородных топливных ячейках для передачи электрического тока.
Какие металлы могут быть использованы в водородных электрохимических системах?
В водородных электрохимических системах могут быть использованы различные металлы, включая платину, никель, кобальт, железо и другие. Платина является одним из наиболее распространенных катализаторов для электролиза воды, так как она обладает высокой активностью и стабильностью. Однако, из-за своей высокой стоимости, исследователи работают над разработкой более доступных катализаторов на основе других металлов.
