Выделение водорода при взаимодействии металлов с соляной кислотой – это один из наиболее распространенных методов получения этого газа. Процесс основан на реакции металла с соляной кислотой, в результате чего образуется соль и водородный газ.
Реакция металла с соляной кислотой происходит при нагревании, что способствует активации химических процессов. Нагревание приводит к разрушению связей между атомами вещества, что обеспечивает более активную реакцию и выделение водорода.
Наиболее часто для проведения реакции используют металлы, такие как цинк, железо, алюминий и магний. Соляная кислота растворяет металл в результате химической реакции, при этом водород выводится в виде газа.
Выделение водорода при взаимодействии металлов с соляной кислотой находит широкое применение в промышленности. Полученный газ может использоваться в процессе производства водородных топливных элементов, при производстве аммиака и других химических соединений, а также в области оборудования для пайки и сварки.
Металл и соляная кислота: выделение водорода в процессе реакции
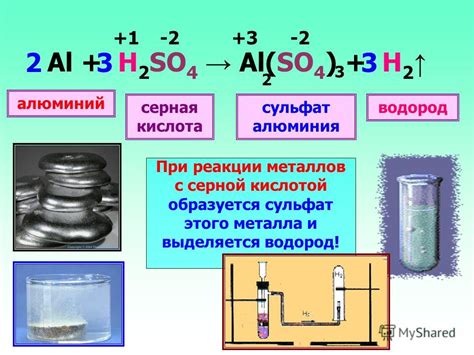
Реакция между металлом и соляной кислотой является одной из важнейших химических реакций, в результате которой выделяется водород. Этот процесс имеет большое значение в промышленности, а также является основой для проведения различных химических экспериментов и опытов.
В ходе реакции металл активно взаимодействует с соляной кислотой, что приводит к образованию химического соединения и выделению газообразного водорода. В этом процессе металл действует как восстановитель, обеспечивая процесс окисления кислорода в составе соляной кислоты.
Реакция выделения водорода между металлом и соляной кислотой может протекать при различных условиях. Как правило, используются металлы первых групп периодической таблицы, такие как цинк или алюминий. Но также возможно взаимодействие с несколькими другими металлами. Важным фактором является концентрация кислоты и температура, которые могут влиять на скорость реакции и количество выделяемого газа.
Результатом реакции выделения водорода является образование соли металла и воды. Водород, который образуется в результате реакции, может быть использован в различных целях, включая промышленность и энергетику. Это значение процесса выделения водорода несомненно придает ему важность и актуальность в современном мире.
Взаимодействие металла с соляной кислотой
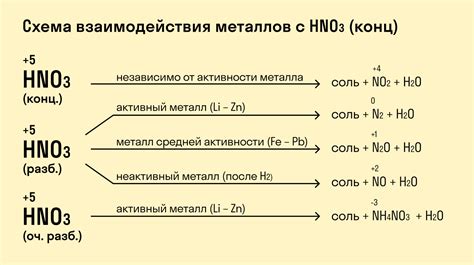
Взаимодействие металла с соляной кислотой - это процесс, при котором металл реагирует с соляной кислотой и выделяется водород. Эта реакция основана на окислительно-восстановительном процессе, где металл обеспечивает электроны, а соляная кислота - принимает их.
В результате этой реакции образуется хлорид металла и вода. Выделение водорода происходит благодаря тому, что он является легким газом и может легко выйти из реакционной смеси. Выделенный водород можно использовать в различных промышленных процессах.
При взаимодействии разных металлов с соляной кислотой скорость реакции может различаться. Например, активные металлы, такие как натрий или калий, реагируют очень быстро, выделяя большое количество водорода. В то время как менее активные металлы, такие как железо или медь, реагируют медленнее и образуют меньше водорода.
Взаимодействие металла с соляной кислотой может быть представлено в виде химического уравнения. Например, реакция железа с соляной кислотой представлена уравнением: Fe + 2HCl = FeCl2 + H2. В этом уравнении Fe обозначает металл железо, HCl - соляную кислоту, FeCl2 - хлорид железа и H2 - выделяющийся водород.
Химический процесс образования водорода

Образование водорода при взаимодействии металлов с соляной кислотой является реакцией окисления-восстановления. Под воздействием соляной кислоты, металлы окисляются, отдают свои электроны и переходят в ионное состояние.
Окисленные металлы затем реагируют со свободными протонами соляной кислоты, тем самым осуществляется процесс восстановления. В результате этой реакции образуется водородный ион H+, который связывается с другой свободной протоном, образуя молекулы водорода H2.
Химический процесс образования водорода может быть представлен упрощенной химической реакцией:
2HCl + Zn → ZnCl2 + H2
- 2HCl - соляная кислота (2 молекулы)
- Zn - металл (цинк)
- ZnCl2 - хлорид цинка
- H2 - молекулы водорода
Этот процесс является экзотермическим, то есть сопровождается выделением тепла. Выделение водорода происходит в виде пузырьков, которые можно наблюдать при проводке соляной кислоты через металлическую проволоку или при погружении металла в кислоту. Это образование водорода в результате взаимодействия металлов с соляной кислотой имеет важное практическое применение в различных процессах и технологиях.
Активность металла в реакции с соляной кислотой
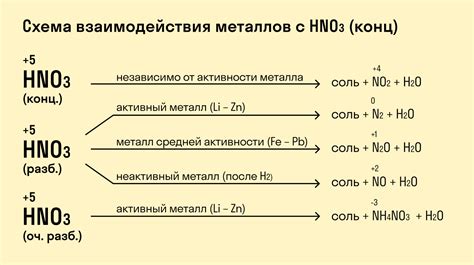
Активность металла в реакции с соляной кислотой определяется его способностью выделять водород. Периодическая таблица химических элементов разделяет металлы на активные и пассивные. Активные металлы, такие как цинк, алюминий и магний, реагируют с соляной кислотой, выделяя водород и образуя соответствующие соли. Эта реакция носит экзотермический характер, то есть сопровождается выделением тепла.
Интенсивность реакции между металлом и соляной кислотой зависит от активности металла. Чем выше активность металла, тем быстрее и интенсивнее протекает реакция. Например, цинк, который относится к самым активным металлам в реакции с соляной кислотой, выделяет водород очень быстро, иногда даже с плавным шипением и выбросом пара.
Наиболее активные металлы, такие как натрий и калий, реагируют с соляной кислотой настолько бурно, что могут вызвать вспышку или взрыв. Это связано с тем, что водород, выделяющийся при реакции, образует взрывоопасные смеси с воздухом. Поэтому при работе с такими металлами необходимо быть особенно осторожным и проводить эксперименты в соответствии с правилами безопасности.
- Активность металлов в реакции с соляной кислотой можно определить с помощью ряда реакций и наблюдения за выделением водорода.
- Реакция между металлом и соляной кислотой является классическим примером реакции металла с кислотой и применяется в химических лабораториях для получения водорода.
Важно отметить, что пассивные металлы, такие как медь и серебро, не реагируют с соляной кислотой под обычными условиями и не выделяют водород. Однако, при нагревании или в реакции с более концентрированной кислотой, они могут проявить активность и возможность выделять водород. Это связано с тем, что при изменении условий реакции, ионы водорода могут образовывать газовый продукт.
Вывод: активность металла в реакции с соляной кислотой определяется его способностью выделять водород. Более активные металлы проявляются в более интенсивной реакции, иногда с возможными опасностями, в то время как пассивные металлы не проявляют активность без изменения условий реакции.
Важность выделения водорода в промышленности

Выделение водорода в промышленности играет ключевую роль во многих отраслях, обеспечивая важные процессы и функции.
1. Энергетика: Водород широко используется как источник энергии в генерации электричества. Он может быть использован в водородных топливных элементах, которые производят электричество без выброса вредных веществ. Этот процесс является экологически безопасным и эффективным, что делает водород одним из основных вариантов возобновляемой энергии.
2. Химическая промышленность: Водород является важным сырьем для производства различных химических веществ. Он используется в процессах гидрогенизации, синтеза и дефосфоризации многих органических и неорганических соединений. Благодаря своим уникальным химическим свойствам, водород играет существенную роль в многих процессах, которые требуют высокой степени чистоты и эффективности.
3. Металлургия: Водород используется в металлургической промышленности для различных процессов обработки металлов. Например, он может быть использован в процессе восстановления, чтобы удалить примеси и нежелательные элементы из металла. Также водород используется в процессе атмосферной нитрировки, который улучшает механические свойства металлических изделий.
4. Электроника: Водород играет важную роль в производстве электронных компонентов, таких как полупроводники и солнечные батареи. Он используется в процессе осаждения и травления, чтобы создать и улучшить структуру полупроводниковых материалов. Водород также применяется в процессе производства микрочипов для удаления загрязнений и создания чистых поверхностей.
Таким образом, выделение водорода в промышленности является неотъемлемой частью многих процессов и важным источником энергии и сырья. Максимальное использование и улучшение процессов выделения водорода позволит улучшить эффективность, экологическую безопасность и экономическую эффективность промышленных производств.
Развитие технологий выделения водорода из металла и соляной кислоты
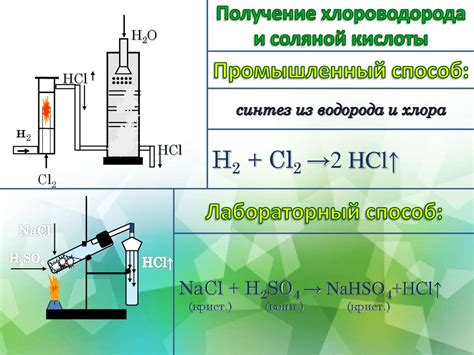
Выделение водорода из металла и соляной кислоты является важным процессом, который находит широкое применение в различных сферах. Начиная с первых экспериментов, проводимых в XIX веке, технологии выделения водорода продолжают развиваться и совершенствоваться.
Одним из наиболее эффективных методов выделения водорода является реакция металла с соляной кислотой. Используя этот метод, водород можно получить из таких металлов, как цинк, алюминий и железо. Сначала проводится реакция металла с соляной кислотой, в результате которой образуется хлорид металла и водород. Затем водород выделяется и очищается от остаточных газов и примесей.
Современные технологии выделения водорода из металла и соляной кислоты включают использование специализированных реакторов и катализаторов, которые позволяют увеличить эффективность процесса и повысить его безопасность. Также для повышения экономической эффективности процесса разрабатываются новые методы переработки отходов и использования более дешевых сырьевых материалов.
- Научные исследования в этой области направлены на поиск новых материалов, которые могут быть использованы для выделения водорода. Ведутся эксперименты с различными металлическими соединениями и катализаторами.
- Технологии выделения водорода из металла и соляной кислоты активно применяются в водородной энергетике. Водород является чистым и удобным источником энергии, который может быть использован для питания электромобилей, отопления домов и производства электроэнергии.
В заключение, развитие технологий выделения водорода из металла и соляной кислоты имеет большое значение для современной науки и промышленности. Эти технологии позволяют получать высокоочищенный водород, который может быть использован в различных сферах деятельности, способствующих снижению негативного воздействия на окружающую среду и развитию экологически чистых источников энергии.
Вопрос-ответ

Процесс выделения водорода из металла и соляной кислоты - как он происходит?
Для получения водорода из металла и соляной кислоты сначала необходимо добавить мелкораспыленный металл в соляную кислоту. В результате химической реакции между металлом и кислотой образуется хлорид металла и водород. Затем полученный газ, содержащий водород, необходимо собрать и очистить от примесей.
Какие металлы можно использовать для выделения водорода из соляной кислоты?
Для выделения водорода из соляной кислоты можно использовать различные металлы, такие как цинк, железо, магний и алюминий. Однако каждый металл обладает своими особенностями и требует определенных условий для реакции с кислотой.
Каким образом происходит химическая реакция между металлом и соляной кислотой?
Химическая реакция между металлом и соляной кислотой основана на обмене ионами. В процессе реакции металл отдает электроны, превращаясь в положительно заряженный ион, а ионы водорода из кислоты принимают эти электроны и образуют молекулы водорода.
Для чего выделяют водород из металла и соляной кислоты? Как он может быть использован?
Выделение водорода из металла и соляной кислоты является одним из способов получения этого газа. Водород может быть использован в различных областях, таких как производство химических соединений, питание топливных элементов, а также в качестве сжиженного газа для промышленных нужд.
Какие безопасностные меры следует соблюдать при проведении процесса выделения водорода из металла и соляной кислоты?
При проведении процесса выделения водорода из металла и соляной кислоты необходимо соблюдать ряд безопасностных мер. Во-первых, работу следует проводить в хорошо проветриваемом помещении или под вытяжной вентиляцией, чтобы избежать скопления взрывоопасного газа. Также важно использовать защитные очки и перчатки, чтобы защитить глаза и кожу от возможного контакта с кислотой или металлом. При обращении с соляной кислотой следует быть особенно осторожными, так как она является коррозионным веществом и может вызывать ожоги.
