Реакция металла с азотной кислотой является одним из важных процессов в химии. Металлы могут реагировать с азотной кислотой, образуя нитраты и оксиды металлов. Эта реакция происходит по принципу окисления-восстановления, где металл окисляется, а азотная кислота восстанавливается.
Особенности реакции зависят от свойств металла и концентрации азотной кислоты. Некоторые металлы, такие как медь и железо, реагируют с азотной кислотой с выделением газа и образованием характерных продуктов. Другие металлы, например, серебро и золото, не реагируют с азотной кислотой, так как они недостаточно активны химически.
Данная реакция имеет широкое применение в научных и промышленных целях. Образование нитратов может быть использовано в производстве удобрений, взрывчатых веществ и других химических соединений. Оксиды металлов, полученные в результате реакции, также имеют множество применений. Например, оксид железа используется в производстве магнитов и красок, а оксид алюминия – в производстве керамики и стекла.
Реакция металла с азотной кислотой является важным процессом в химии и имеет множество применений. Особенности реакции зависят от свойств металла и концентрации азотной кислоты. Результатом реакции являются нитраты и оксиды металлов, которые используются в различных отраслях промышленности.
Взаимодействие металла с азотной кислотой: реакции и химические свойства
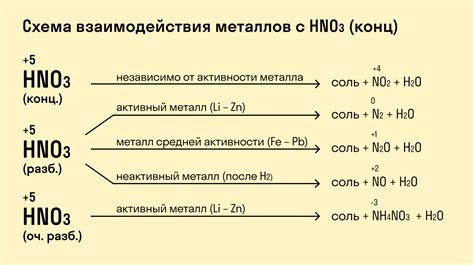
Азотная кислота (HNO3) — один из наиболее распространенных химических реагентов, который активно используется в различных химических процессах. Взаимодействие металлов с азотной кислотой приводит к проведению ряда реакций, которые определяют химические свойства данных элементов.
При взаимодействии металлов с азотной кислотой образуется азот оксид, вода и соответствующее металлическое нитратное соединение. Реакция происходит следующим образом: металл активно вступает в химическую связь с нитратным ионом, образуется оксид металла и выделяется азот оксид, который имеет красноватую окраску.
Взаимодействие металлов с азотной кислотой может протекать с разной интенсивностью в зависимости от их электрохимических свойств и реакционной способности. Некоторые металлы, например, железо, медь, свинец, серебро, могут активно реагировать с азотной кислотой, образуя соответствующие нитраты и азотные оксиды.
Основным применением реакции металла с азотной кислотой является получение нитратных соединений, которые широко используются в различных отраслях промышленности, сельском хозяйстве и медицине. Кроме того, данная реакция находит применение в лабораторных исследованиях, а также в процессе получения и очистки различных веществ.
Общая информация о азотной кислоте и металлах

Азотная кислота (HNO3) является одной из наиболее распространенных и важных неорганических кислот. Она представляет собой безцветную жидкость со специфическим запахом. Азотная кислота является сильным окислителем и ее реакция с металлами является одной из самых интересных и важных.
Взаимодействие азотной кислоты с металлами происходит с образованием азотных солей. Эти соли обладают особенностями, например, они могут быть подвергнуты реакциям доведения до высокого температуры с образованием оксидов или действовать как взрывчатые вещества.
Азотная кислота может реагировать с различными металлами, такими как железо, цинк, алюминий и т.д. Реакция может проходить с выделением газа (диоксида азота) и образованием соответствующих азотных солей. Реактивность металлов в реакции с азотной кислотой может различаться в зависимости от их свойств и состояния: некоторые металлы реагируют с азотной кислотой быстро и интенсивно, тогда как другие металлы могут реагировать медленно или даже пассивироваться.
Применение реакции металлов с азотной кислотой включает широкий спектр областей, от химического производства до аналитических исследований. Реакцию можно использовать для получения азотных солей, которые могут быть применены в производстве удобрений, взрывчатых веществ и других химических соединений. Также, реакция металла с азотной кислотой может служить методом определения присутствия металла в образце или исследований его активности.
Металлы и их реакции с азотной кислотой

Металлы и азотная кислота
Металлы могут реагировать с азотной кислотой, образуя соответствующие соли и выделяя оксиды азота. Реакция металлов с азотной кислотой обычно является быстрой и интенсивной, особенно при высоких концентрациях кислоты.
Химические свойства металлов
Металлы являются химическими элементами, обладающими характерными свойствами, такими как высокая электропроводность, блеск, пластичность и хорошая теплопроводность. Многие металлы имеют низкую степень реактивности и устойчивы к окислению, но некоторые металлы, такие как цинк, железо и алюминий, могут реагировать с азотной кислотой.
Реакция металлов с азотной кислотой
При реакции металла с азотной кислотой, металл окисляется, а азотная кислота восстанавливается. В результате реакции образуются соответствующие нитраты металлов и оксиды азота выделяются в виде газа. Реакция может быть сопровождена выделением тепла и пением. Некоторые металлы, такие как медь и серебро, обычно не реагируют с азотной кислотой.
Применение реакции металлов с азотной кислотой
Реакция металлов с азотной кислотой имеет ряд практических применений. Например, нитраты металлов, получаемые в результате реакции, используются в производстве удобрений и пиротехнических составов. Также данная реакция может служить методом анализа металлов, позволяя определить их наличие и концентрацию в образцах.
Применение реакции металла с азотной кислотой
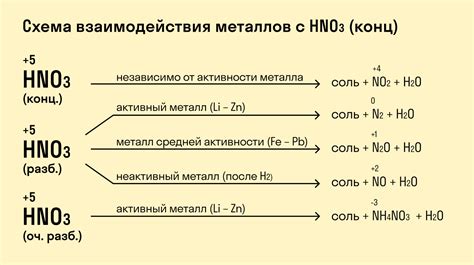
1. Получение азотных соединений. Реакция металла с азотной кислотой является эффективным способом получения азотных соединений. В результате этой реакции образуются нитраты металлов, которые широко используются в промышленности и сельском хозяйстве.
2. Производство химических удобрений. Многие азотные удобрения, такие как аммиачная селитра и аммиачная фосфатная селитра, производятся с использованием реакции металла с азотной кислотой. Эти удобрения являются важными компонентами для повышения урожайности сельскохозяйственных культур.
3. Производство взрывчатых веществ. Нитроэфиры, которые используются в производстве взрывчатых веществ, могут быть получены путем реакции металла с азотной кислотой. Эта реакция играет важную роль в производстве взрывчаток и пиротехники.
4. Аналитическая химия. Реакция металла с азотной кислотой широко используется в аналитической химии для определения содержания металлов в различных образцах. Эта реакция позволяет проводить качественный и количественный анализ металлов с высокой точностью.
Таким образом, реакция металла с азотной кислотой имеет множество применений в различных областях, от промышленности до науки. Она позволяет получать азотные соединения, производить химические удобрения и взрывчатые вещества, а также проводить анализ металлов. Эта реакция является важной составляющей современной химии и используется в различных отраслях промышленности.
Практическое использование особенностей реакции металла с азотной кислотой
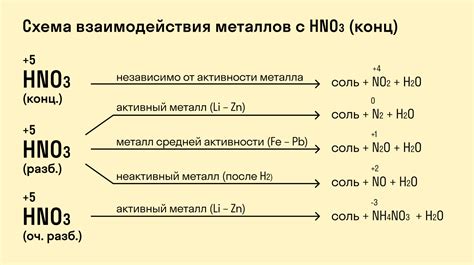
Реакция металла с азотной кислотой является одной из важных химических реакций, которая находит широкое практическое применение. Основным компонентом реакции является азотная кислота (HNO3), которая взаимодействует с металлом, образуя соответствующую соль и выделяя водород. В зависимости от металла и условий реакции можно получить различные продукты.
Одним из практических применений реакции металла с азотной кислотой является получение нитратов. Азотная кислота используется в производстве различных удобрений, таких как аммиачная селитра. В данном случае реагентом выступает аммиак, который реагирует с азотной кислотой, образуя нитрат аммония. Этот нитрат широко используется в сельском хозяйстве для повышения урожайности растений.
Другим применением реакции металла с азотной кислотой является получение взрывчатых веществ. Азотные дериваты, полученные из азотной кислоты, обладают сильными взрываемыми свойствами и широко применяются в промышленности, армии и пиротехнике. Примером такого вещества является тринитротолуол (ТНТ), который получается в результате нитрирования толуола азотной кислотой.
Кроме того, реакция металла с азотной кислотой может использоваться для очистки поверхностей металлических изделий от окислов и примесей. При реакции азотной кислоты с металлом происходит процесс образования растворимых солей, которые после промывки можно легко удалить.
Таким образом, практическое использование особенностей реакции металла с азотной кислотой обширно и разнообразно. Она находит применение в производстве удобрений, получении взрывчатых веществ и очистке металлических поверхностей, что делает ее особенно важной и полезной в различных отраслях промышленности и науки.
Вопрос-ответ

Какие металлы реагируют с азотной кислотой?
С азотной кислотой реагируют различные металлы, включая медь, железо, цинк, алюминий и др.
Каков механизм реакции металла с азотной кислотой?
При реакции металла с азотной кислотой происходит окислительно-восстановительная реакция, в результате которой образуется соль металла и выделяется окислительный газ - оксид азота или двуокись азота (NO2).
