Реакция металла с водным раствором соляной кислоты является одной из наиболее распространенных химических реакций. Она характеризуется выделением водорода и образованием соли металла. Данная реакция имеет множество практических применений и обладает рядом особенностей, которые важно учитывать при ее изучении и использовании.
Одним из основных контекстов, в котором встречается реакция металла с соляной кислотой, является химия металлов. Нередко она используется для получения водорода, который затем может быть использован в процессах синтеза других веществ или как энергетический источник. Также, реакция металла с соляной кислотой применяется в качестве метода анализа металлов, позволяя определить их наличие и количество.
Следует отметить, что реакция металла с соляной кислотой не происходит с каждым металлом. Некоторые металлы, такие как золото или платина, нереактивны с водным раствором соляной кислоты. Однако, большинство металлов, таких как железо, цинк или алюминий, образуют с соляной кислотой химическую реакцию, сопровождающуюся испусканием пузырьков водорода и выделением тепла.
Изучение и понимание реакции металла с соляной кислотой позволяет не только расширить теоретические знания в области химии, но и найти практическое применение данной реакции в различных областях науки и промышленности.
Разлагающийся металл и реакция с соляной кислотой

Разлагающийся металл – это металлическая составляющая, которая обладает способностью разлагаться при взаимодействии с другими химическими соединениями или растворами. В реакции с соляной кислотой разлагающиеся металлы могут проявлять различные свойства и химические реакции. Результат такой реакции может быть как образование нового вещества, так и выделение газов или тепла.
Реакция металла с соляной кислотой является классическим примером реакции металла с кислотой. Данная реакция протекает с образованием соли и выделением водорода. Многие металлы, такие как цинк, железо или алюминий, способны разлагаться вводной раствор соляной кислоты, давая активное взаимодействие с ней.
Реакция между металлом и соляной кислотой может протекать в различных условиях: при комнатной температуре или под действием нагревания. Нагревание ускоряет ход реакции и повышает интенсивность разложения металла. Протекание реакции можно наблюдать через возникновение пузырьков газа и изменение цвета или состояния раствора.
Реакция металла с соляной кислотой имеет множество приложений. Она широко используется в химической и промышленной отраслях для получения солей, которые используются в производстве различных продуктов. Кроме того, данная реакция может применяться для очистки металлических поверхностей от окислов и загрязнений, а также в лабораторных исследованиях для получения газов или изучения химических свойств металлов.
Механизм взаимодействия

Реакция металла с водным раствором соляной кислоты происходит по следующему механизму. Сначала происходит диссоциация соляной кислоты на ион водорода (H+) и ион хлора (Cl-). Затем ион водорода образует гидратированный протон (H3O+), который является основным активным компонентом в данной реакции.
На следующем этапе металл, вступая в реакцию с протоном, отдает электроны и превращается в положительно заряженный ион металла. Это является окислительно-восстановительной реакцией, так как происходит одновременное окисление металла и восстановление водорода до иона H3O+.
Особенностью взаимодействия металла с соляной кислотой является выделение водорода и образование соли металла. Выделение водорода происходит в виде газа и сопровождается пузырьками, которые можно наблюдать на поверхности металла. Соль металла же остается в растворе в виде иона, взаимодействуя с ионами хлора, образуя хлорид металла.
Реакция металла с водным раствором соляной кислоты имеет широкое применение в различных областях. Например, она используется в металлургической промышленности для получения хлоридов металлов, которые являются важными компонентами в производстве аккумуляторов и электролитов для солевых батарей. Также данная реакция широко применяется в аналитической химии для определения содержания металла в образце, поскольку выделение водорода позволяет определить количество металла в исследуемом растворе.
Выделение газа и тепла
Металлы реагируют с водным раствором соляной кислоты, образуя газ и выделяя тепло. Газ, который выделяется в результате реакции, это водород. Он образуется в результате взаимодействия атомов металла с соляной кислотой. Водород обладает свойством быть легким и воспламеняемым газом.
Выделение тепла в процессе реакции связано с тем, что реакция между металлом и кислотой является экзотермической. При этом энергия, накопленная в связях между атомами металла и кислоты, освобождается в виде тепла. Такая реакция происходит самоподдерживаемо, без необходимости внешнего источника тепла.
Выделение газа и тепла в процессе реакции металла с водным раствором соляной кислоты находит применение в различных областях. Например, процесс выделения водорода из воды с помощью металла и соляной кислоты используется водородные энергетические системы, а также в производстве различных химических соединений. Кроме того, тепло, выделяемое в процессе реакции, можно использовать для нагрева жидкостей или газов, что также имеет практическое применение.
Влияние концентрации кислоты на скорость реакции

При изучении реакции металла с водным раствором соляной кислоты особое внимание уделяется влиянию концентрации кислоты на скорость реакции. Использование различных концентраций соляной кислоты позволяет исследовать зависимость скорости реакции от ее концентрации и выявить особенности процесса.
Эксперименты показывают, что с увеличением концентрации соляной кислоты скорость реакции между металлом и кислотой увеличивается. Это объясняется тем, что повышение концентрации приводит к увеличению количества водородных ионов, что способствует более активной реакции с металлом.
Однако, при слишком высокой концентрации кислоты может наблюдаться обратный эффект - снижение скорости реакции. Это связано с насыщением поверхности металла водородными ионами, что препятствует дальнейшему взаимодействию молекул кислоты с металлом.
Изучение влияния концентрации кислоты на скорость реакции имеет практическое значение. Например, при разработке процессов химической обработки металлических поверхностей учитывается оптимальная концентрация кислоты, при которой достигается максимальная скорость реакции, обеспечивающая эффективное удаление окислов и загрязнений с поверхности.
Особенности реакции с различными металлами

1. Реакция с активными металлами:
Активные металлы, такие как натрий, калий и магний, реагируют с водным раствором соляной кислоты достаточно быстро и интенсивно. При этом образуется водородный газ и соответствующие соли металлов. Например, активный металл натрий при реакции с соляной кислотой образует хлорид натрия и выделяет водород.
2. Реакция с менее активными металлами:
Менее активные металлы, как например цинк и железо, также могут реагировать с водным раствором соляной кислоты. Однако, скорость реакции будет меньше, чем с активными металлами, и образуется меньшее количество водорода. Также образуются соответствующие соли металлов и высвобождаются ионы водорода.
3. Нереактивные металлы:
Некоторые металлы, например свинец и золото, практически не реагируют с водным раствором соляной кислоты. Имея низкую реактивность, эти металлы не вступают во взаимодействие с кислотой и не образуют соли или водородный газ. Такие металлы используются для конструкций, которые не должны реагировать с кислотами или другими реагентами.
4. Реакция с щелочными металлами:
Щелочные металлы, включая литий и калий, реагируют с соляной кислотой, но при этом образуются соответствующие хлориды и гидроксиды. Реакция с щелочными металлами более сложная и требует регулирования условий окружающей среды, чтобы избежать избытка водородного газа и опасности возгорания.
Таким образом, реакция металла с водным раствором соляной кислоты может происходить по-разному в зависимости от активности металла. Результаты реакции могут быть использованы в различных областях, включая химическую промышленность, аналитическую химию и в исследованиях различных свойств металлов.
Реакция алкалийных металлов
Алкалийные металлы (литий, натрий, калий, рубидий, цезий) являются самыми активными элементами в химической периодической системе. Их реакция с водным раствором соляной кислоты происходит с выделением газа водорода и образованием солей алкалийных металлов.
В ходе реакции алкалийные металлы активно взаимодействуют с агрессивным соляным раствором. При этом происходит выделение водорода, который образуется в результате реакции алкалийного металла с протонами соляной кислоты. Образование водорода происходит в виде пузырьков, которые постепенно поднимаются вверх и выходят из раствора.
Реакция алкалийных металлов с водным раствором соляной кислоты может быть использована в рамках химических опытов и демонстраций. Это явление хорошо наглядно и позволяет продемонстрировать процесс взаимодействия активного металла и кислоты. При этом необходимо соблюдать меры предосторожности, так как реакция сопровождается выделением горючего водорода.
Реакция аллюминия и цинка

Реакция аллюминия и цинка является одной из классических примеров реакции металла с водным раствором соляной кислоты. Эта реакция происходит при взаимодействии аллюминия или цинка с соляной кислотой, при которой образуются соли алюминия и цинка, а также выделяется водород.
В результате реакции, взаимодействуя с соляной кислотой, алюминий образует соль алюминия – алюминий хлорид (AlCl3). Соли алюминия в широком спектре применяются в промышленности, особенно в производстве красителей, лаков, пигментов и других продуктов.
Цинк также реагирует с соляной кислотой, образуя соответствующую соль – цинк хлорид (ZnCl2). Цинк используется во многих отраслях промышленности, включая строительство, автомобильное производство, производство батарей, а также в производстве других металлических изделий.
Реакция аллюминия и цинка с водным раствором соляной кислоты имеет широкое применение в химической промышленности и лабораторных исследованиях. В этой реакции можно наблюдать выделение пузырьков водорода, что делает ее примечательной и удобной для изучения. Кроме того, данная реакция помогает углубить знания о свойствах металлов и их взаимодействии с кислотами.
Важность реакции металла с водным раствором соляной кислоты в промышленности
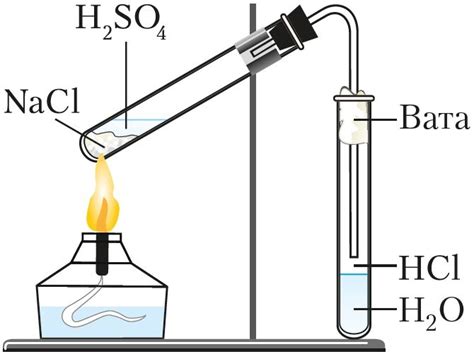
Реакция металла с водным раствором соляной кислоты является одной из важнейших химических реакций в промышленности. Это процесс, при котором металл вступает в реакцию с соляной кислотой, образуя хлорид металла и выделяясь водород. Реакция широко применяется в различных отраслях промышленности благодаря своим уникальным свойствам и возможностям.
Одним из основных применений реакции металла с соляной кислотой является получение хлорида металла. Хлориды металлов широко используются в производстве различных продуктов, таких как пластмассы, текстиль, стекло, электроника и другие. Они обладают рядом полезных свойств, таких как высокая электропроводность, стойкость к коррозии и теплостойкость, что делает их незаменимыми материалами для многих отраслей промышленности.
Кроме получения хлорида металла, реакция металла с соляной кислотой также может использоваться для очистки и обработки металлических поверхностей. В процессе реакции образующийся водород может выполнять роль растворяющего агента, который удаляет загрязнения и окислы с поверхности металла. Это позволяет получить чистый и гладкий металлический поверхность, исключая необходимость использования других химических веществ и механических методов обработки.
Важное значение реакции металла с соляной кислотой видно и в аналитической химии. Реакция является одним из базовых методов определения металлов в различных образцах. Она используется для получения растворов металлических ионов, которые затем могут быть проанализированы различными методами, такими как спектрофотометрия, вольтамперометрия и другие.
Вопрос-ответ

Что происходит при реакции металла с водным раствором соляной кислоты?
При реакции металла с водным раствором соляной кислоты образуется соль и выделяется водород газ. Происходит окислительно-восстановительная реакция, при которой металл восстанавливается, а водород окисляется.
Какие металлы реагируют с водным раствором соляной кислоты?
С водным раствором соляной кислоты реагируют многие металлы, такие как железо, цинк, алюминий, медь и др. Однако нежелезные металлы, такие как серебро и золото, не реагируют с соляной кислотой.
Какие особенности имеет реакция металла с водным раствором соляной кислоты?
Одной из особенностей реакции металла с водным раствором соляной кислоты является выделение водорода газа, что может сопровождаться появлением пузырьков и шипением. Кроме того, реакция протекает довольно быстро и снятие образовавшегося водорода может быть опасно, так как он является взрывоопасным газом.
В каких областях применяется реакция металла с водным раствором соляной кислоты?
Реакция металла с водным раствором соляной кислоты находит широкое применение в различных областях. Например, она используется в лабораториях для получения газового водорода, который затем может быть использован в качестве топлива или в других процессах. Также эта реакция может применяться в химическом анализе для определения наличия и количества определенных металлов в пробе.
