Связь между металлами и неметаллами — одна из важнейших тем в химии. Исследование этой связи позволяет понять, каким образом металлы и неметаллы образуют соединения и взаимодействуют друг с другом. Научные исследования в этой области помогают разрабатывать новые материалы с улучшенными свойствами и применениями.
Металлы и неметаллы - это химические элементы, обладающие различными физическими и химическими свойствами. Они имеют разную электроотрицательность и способность образовывать химические связи. Металлы обычно обладают металлическим блеском, отличной тепло- и электропроводностью, а также гибкостью и пластичностью. Неметаллы обычно обладают прозрачностью, хрупкостью и меньшей электропроводностью.
Связь между металлами и неметаллами может быть реализована в различных типах химических связей. Одним из часто встречающихся типов связи является ионная связь, которая основана на притяжении положительно заряженных металлических и отрицательно заряженных неметаллических ионов друг к другу. Еще одним типом связи является ковалентная связь, которая образуется за счет общего электронного облака между атомами металла и неметалла. Также существует металлическая связь, основанная на образовании "моря" электронов, свободно движущихся между атомами металла. Эти типы связей определяют свойства и характер соединений между металлами и неметаллами.
Взаимодействие металла и неметалла: основные аспекты
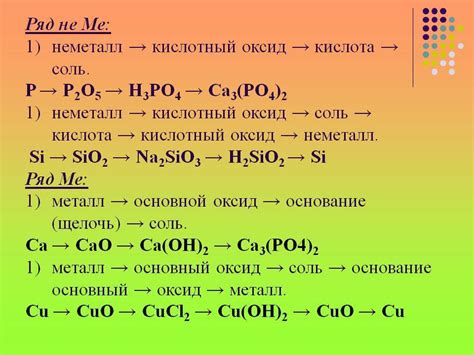
Взаимодействие металла и неметалла является одной из основных тем, изучаемых в химии. Этот процесс представляет собой соединение двух разных элементов, имеющих разные свойства и химическую природу.
Основной тип связи, который образуется при взаимодействии металла и неметалла, называется ионной связью. В такой связи между металлом и неметаллом происходит передача электронов. Металл отдает электроны, превращаясь в положительный ион, а неметалл принимает эти электроны, образуя отрицательный ион. Таким образом, образуется соединение, которое имеет структуру кристаллической решетки.
При взаимодействии металла и неметалла также происходит образование нескольких типов химических связей. Одним из них является ковалентная связь, которая возникает при обмене электронами между атомами металла и неметалла. Также может образоваться металлическая связь, которая происходит при перемещении электронов внутри металлической решетки.
Взаимодействие металла и неметалла имеет важное значение в различных областях науки и технологии. Например, металлоиды - элементы, обладающие свойствами как металла, так и неметалла, широко применяются в электронике и полупроводниковой промышленности. Также соединения металла и неметалла используются в химической промышленности для производства разнообразных материалов и веществ.
Связь между металлом и неметаллом: как исследовать взаимодействие
Взаимодействие между металлом и неметаллом представляет собой сложный процесс, который требует специальных исследований для понимания его механизмов. Одним из основных методов исследования является анализ химической связи, которая образуется между атомами металла и неметалла.
Для анализа химической связи между металлом и неметаллом применяются различные методы, такие как рентгеноструктурный анализ, спектроскопия, электронная микроскопия и другие. Рентгеноструктурный анализ позволяет определить расстояние между атомами и угол между химическими связями. Спектроскопия позволяет изучать энергетические уровни атомов и молекул, а также определять характер связи между ними.
Исследование взаимодействия между металлом и неметаллом также может включать изучение реакционной способности и кинетики реакций. Для этого проводятся эксперименты, в которых металл и неметалл подвергаются воздействию различных веществ и измеряются скорость и характер продуктов реакции.
Важно отметить, что связь между металлом и неметаллом может иметь различные типы, такие как ионная связь, ковалентная связь или смешанная связь. Тип связи зависит от электроотрицательности атомов, расстояния между ними и других факторов. Исследование типов связей позволяет понять особенности взаимодействия между металлом и неметаллом и предсказать их свойства и способность к образованию соединений.
Ионная связь: принцип и примеры

Ионная связь - это тип химической связи, образующийся между атомами, которые образуют ионы разных зарядов. Одними из основных условий для образования ионной связи являются большая разница в электроотрицательности между атомами и наличие свободных электронов.
Примерами веществ, обладающих ионной связью, являются натриевый хлорид (NaCl) и кальций фторид (CaF2). В натриевом хлориде натрий отдает свой электрон атому хлора, что приводит к образованию положительного иона натрия (Na+) и отрицательного иона хлора (Cl-). Эти ионы притягиваются друг к другу благодаря противоположным зарядам и создают кристаллическую решетку.
Кальций фторид образуется путем передачи одного электрона из атома кальция (Ca2+) к атому фтора (F-). В результате образуются положительные ионы кальция и отрицательные ионы фтора, которые также притягиваются друг к другу, образуя кристаллическую решетку.
Ионная связь является очень сильной и защищает ионы вещества от разделения, поскольку для этого требуется значительное количество энергии. Поэтому вещества с ионной связью обычно обладают высокими точками плавления и кипения.
Ковалентная связь: основные черты и применение
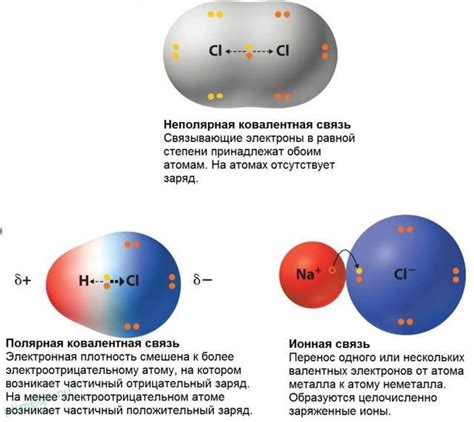
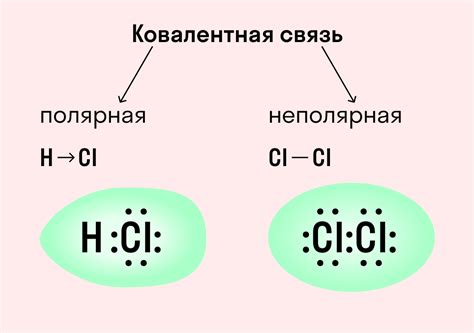
Ковалентная связь – это тип химической связи, который возникает между неметаллами, когда они делят между собой электроны своих валентных оболочек. В результате этого образуется общая область с высокой плотностью электронов, что обусловливает силу удержания атомов в молекуле. Основным признаком ковалентной связи является обмен электронами между атомами для достижения стабильного состояния.
Ковалентная связь обусловливает химическую устойчивость молекул и позволяет им образовывать различные химические соединения. Благодаря этому типу связи возможно образование сложных органических соединений, таких как углеводороды, аминокислоты, простейшие и другие биологически активные вещества.
Ковалентные связи характеризуются определенной длиной и углом между связанными атомами. Длина связи зависит от радиусов атомов и может быть различной в различных химических соединениях. Угол между связанными атомами в молекуле также имеет значение и влияет на ее структуру и свойства.
Ковалентная связь имеет широкое применение в различных областях науки и техники. Она используется для создания искусственных материалов, таких как пластик, синтетические волокна, полимеры и другие. Ковалентные связи также играют важную роль в фармацевтике, где используются сложные молекулы для создания лекарственных препаратов. Кроме того, ковалентная связь применяется в электронике и каталитической химии, а также в областях, связанных с энергетикой и окружающей средой.
Металлическая связь: особенности и роль в различных процессах

Металлическая связь представляет собой особый тип химической связи, который образуется между атомами металла. Эта связь является одной из основных и наиболее сильных, обуславливающих уникальные физические и химические свойства металлов. Особенностью металлической связи является общий электронный газ, образованный свободными электронами.
Металлическая связь играет важную роль в различных процессах, включая проводимость электричества и тепла, механическую прочность и пластичность, а также способность к формированию металлических соединений. Благодаря наличию свободных электронов, металлы обладают высокой электропроводностью. Они способны передавать электроны от одного атома к другому без существенного сопротивления, что позволяет использовать их в различных электрических устройствах и проводящих материалах.
Основными особенностями металлической связи являются высокая пластичность и прочность материалов. Это обусловлено способностью атомов металла с легкостью перемещаться друг относительно друга без нарушения связи, благодаря наличию общего электронного газа. Металлическая связь также позволяет металлам образовывать различные соединения, в том числе сплавы и металлоиды. Это позволяет изменять и улучшать их физические и химические свойства в зависимости от конкретных требований и потребностей.
Таким образом, металлическая связь является основой для многих важных процессов и явлений, определяющих свойства и применение металлов. Этот вид связи обладает уникальными характеристиками, которые делают металлы одним из наиболее важных и незаменимых материалов в нашей жизни.
Вопрос-ответ

Какие металлы образуют связь с неметаллами?
Металлы могут образовывать связи с различными неметаллами, например, железо может образовывать связи с кислородом, серой или углеродом. Алюминий может образовывать связи с кислородом, фтором или хлором. В общем случае, металлы могут образовывать связи с неметаллами, если их электроотрицательности различаются.
Какие типы связей могут образовываться между металлом и неметаллом?
Между металлами и неметаллами могут образовываться различные типы связей. Один из наиболее распространенных типов - ионическая связь, при которой один атом (обычно металла) отдает электрон(ы) другому атому (обычно неметалла). Также может образовываться ковалентная связь, при которой электроны между атомами металла и неметалла распределяются равномерно и образуют общие пары электронов. Еще один тип связи - металлическая, которая характеризуется наличием свободных электронов, образующих "облако", окружающее положительно заряженные ионы металла.
Как можно определить, какой тип связи преобладает в соединении между металлом и неметаллом?
Определение типа связи между металлом и неметаллом можно провести различными методами. Например, можно анализировать электроотрицательности атомов металла и неметалла - если разность электроотрицательностей большая, скорее всего, в соединении преобладает ионическая связь. Если металл и неметалл имеют близкие электроотрицательности, то возможна ковалентная связь. Также можно использовать физические методы, например, определение точки плавления или проводимости вещества, чтобы сделать вывод о типе связи.
