Металлы в нашей жизни окружают нас повсюду, их использование в различных областях промышленности и науки является неотъемлемой частью современного мира. Однако, при контакте металлов с кислотными оксидами происходят различные химические реакции, которые могут иметь как положительные, так и отрицательные последствия.
При взаимодействии металлов с кислотными оксидами образуются соединения, которые могут быть как стабильными, так и нестабильными. Стабильные соединения металла с кислотным оксидом могут использоваться в различных областях промышленности. Например, цинк оксид – устойчивое соединение, которое используется в производстве керамики, лакокрасочных материалов и электронных компонентов.
Однако, при взаимодействии некоторых металлов с кислотными оксидами могут образовываться нестабильные соединения, которые могут вызвать негативные последствия. Например, реакция железа с оксидами серы приводит к образованию серы в виде газа, что приводит к загрязнению окружающей среды. Также, некоторые металлы могут реагировать с кислотными оксидами очень активно, что может привести к опасным взрывам или пожарам.
Таким образом, взаимодействие металлов с кислотными оксидами является важным аспектом химической реакции, который необходимо учитывать при использовании металлов в различных областях промышленности и науки. Правильное сочетание и контроль при взаимодействии металлов с кислотными оксидами позволяет использовать эти процессы в положительных целях и создать новые действующие вещества со специфическими свойствами.
Взаимодействие металла с кислотным оксидом
Кислотные оксиды - это соединения, которые образуются при соединении элемента с кислородом. Они обладают кислотными свойствами и могут реагировать с различными веществами, в том числе с металлами.
Взаимодействие металла с кислотным оксидом может привести к образованию солей. Это происходит в результате реакции окисления металла и восстановления кислотного оксида.
Примером такого взаимодействия является реакция железа с кислородом. При нагревании металла в присутствии кислорода, образуется оксид железа. Данная реакция широко используется в металлургии при производстве стали.
Кроме того, взаимодействие металла с кислотными оксидами может приводить к образованию коррозии. Например, при контакте железа с оксидом серы, образуется серная кислота, что вызывает повреждение металла.
В общем, взаимодействие металла с кислотным оксидом зависит от химических свойств обоих веществ и может приводить как к образованию полезных соединений, так и к негативным последствиям, таким как коррозия металла.
Процесс окисления и образование соединений
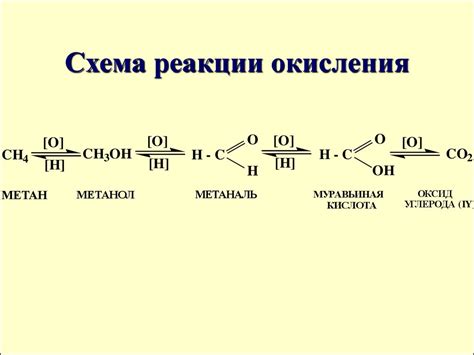
Металлы и кислотные оксиды могут вступать в реакцию, которая называется окислительно-восстановительной реакцией. В результате этой реакции происходит окисление металла и образование соединений.
Окисление металла происходит путем передачи электронов от металла к кислотному оксиду. В процессе окисления металла образуются положительно заряженные ионы, а кислотный оксид приобретает дополнительные отрицательные заряды.
Образовавшиеся ионы металла и оксионные ионы соединяются в результате электростатического притяжения и образуют новые соединения, которые называются оксидами металла.
Процесс окисления металла и образование соединений может происходить только при наличии достаточного количества кислотного оксида. Если количество оксида недостаточно, то образуется неполное оксидированное соединение металла.
Реакция между металлом и кислотным оксидом может протекать с выделением тепла или поглощением тепла. В зависимости от условий реакции и свойств металла и оксида, окислительно-восстановительная реакция может быть самопроизвольной или требовать дополнительной энергии.
Физические и химические изменения

Взаимодействие металла с кислотным оксидом приводит к различным физическим и химическим изменениям.
При контакте металла с кислотным оксидом происходит электрохимическая реакция, в результате которой образуется соль металла и выделяется газ. Этот процесс называется окислением металла.
Физическое изменение, которое можно наблюдать при взаимодействии металла и кислотного оксида, - это изменение цвета. Например, железо при взаимодействии с кислородом образует ржавчину, которая имеет красно-коричневый оттенок.
Химические изменения включают образование новых соединений, изменение pH среды и выделение тепла или света. Например, при реакции алюминия с кислородом образуется оксид алюминия и выделяется большое количество тепла.
Другим примером химического изменения при взаимодействии металла с кислотным оксидом является образование соляной кислоты. Например, при реакции железа с кислородом и водой образуется ржавчина и соляная кислота.
Возможные реакции и их использование

При взаимодействии металла с кислотным оксидом могут происходить различные реакции, в зависимости от характеристик веществ и условий эксперимента. Одной из наиболее распространенных реакций является образование соли и выделение газа.
Например, при взаимодействии металла с оксидом кислорода может образоваться соль металла и выделяться диоксид кислорода. Это явление можно наблюдать, например, при взаимодействии железа с оксидом углерода (II):
- Fe + CO2 → FeCO3 + CO2
Такие реакции могут использоваться в промышленности для получения различных соединений и газов. Например, образование соли меди и выделение диоксида серы при взаимодействии меди с оксидом серы (IV) используется для получения серной кислоты:
- Cu + SO2 → CuSO4 + SO2
Также возможны реакции, в результате которых образуются оксиды металлов. Например, при взаимодействии железа с оксидом азота (II) образуется оксид железа (III), который может использоваться в процессах каталитического окисления:
- Fe + NO → Fe2O3 + NO
Таким образом, взаимодействие металла с кислотным оксидом может привести к образованию солей, выделению газов или образованию оксидов металлов. Эти реакции широко применяются в различных областях, включая промышленность и химическую лабораторию.
Влияние внешних факторов на процесс

Взаимодействие металла с кислотным оксидом может быть значительно изменено различными внешними факторами.
Температура: Повышение температуры может ускорить процесс реакции между металлом и кислотным оксидом. Высокая температура обычно приводит к более интенсивному испарению растворителя, что ускоряет протекание реакции.
Концентрация раствора: Увеличение концентрации раствора кислотного оксида может ускорить реакцию с металлом. Это связано с увеличением количества доступных активных частиц на поверхности металла.
Размер частиц металла: Более мелкие частицы металла имеют большую поверхность контакта с кислотным оксидом, что увеличивает скорость реакции. Кроме того, меньший размер частиц может способствовать более равномерному распределению тепла и массы в системе.
Давление: Изменение давления может влиять на процесс реакции между металлом и кислотным оксидом. Высокое давление может способствовать более близкому контакту между частицами, что ускоряет протекание реакции. Однако, при слишком высоком давлении могут возникать и другие эффекты, например, изменение растворимости веществ или образование новых структур.
Окружающая среда: Воздействие окружающей среды также может оказывать влияние на процесс реакции. Например, наличие других реактивов может ускорить или замедлить реакцию, а изменение pH раствора может повлиять на характер процесса.
Присутствие катализаторов: Наличие катализаторов может значительно ускорить процесс реакции между металлом и кислотным оксидом. Катализаторы обычно увеличивают скорость реакции, предоставляя альтернативные пути реакции с более низким энергетическим барьером.
Влияние этих внешних факторов может быть варьирующим и зависит от конкретной системы реакции между металлом и кислотным оксидом.
Вопрос-ответ

Какова реакция металла с кислотным оксидом?
Взаимодействие металла с кислотным оксидом приводит к образованию соли и выделению воды. При этом металл замещает водород в кислотном оксиде, образуется соответствующая соль и выделяется вода.
Какие факторы влияют на скорость реакции металла с кислотным оксидом?
Скорость реакции металла с кислотным оксидом зависит от нескольких факторов, включая температуру, концентрацию реагентов, поверхность контакта и наличие катализаторов. Более высокая температура, более высокая концентрация реагентов и большая поверхность контакта способствуют увеличению скорости реакции.
Какая реакция происходит при взаимодействии цинка с оксидом серы(IV)?
При взаимодействии цинка с оксидом серы(IV) образуется соль серы(IV) и выделяется вода. Уравнение реакции выглядит следующим образом: Zn + SO₂ → ZnSO₃ + H₂O.
