Металлы и кислоты - две вещества, имеющие совершенно разные свойства и химические реакции. Однако существуют исключения из этого правила, когда металлы не реагируют с определенными кислотами при обычной температуре. Одним из таких случаев является взаимодействие металлов с концентрированной серной кислотой.
Серная кислота (H2SO4) - сильная кислота, обладающая высокой степенью диссоциации. Взаимодействуя с металлами, она способна образовывать соли - сульфаты металлов. Однако, многие металлы не реагируют с серной кислотой в нормальных условиях, то есть при комнатной температуре и давлении.
Это объясняется тем, что некоторые металлы образуют защитную пленку оксида на своей поверхности, которая предотвращает дальнейшее взаимодействие с кислотой. Например, алюминий образует оксидное покрытие - алюминиевый оксид (Al2O3), железо - оксидное покрытие - железо(III) оксид (Fe2O3).
Также стандартные электродные потенциалы металлов и концентрированной серной кислоты показывают, что реакция проходит с выделением водорода, но только при повышенной температуре или с наличием катализатора (например, платины).
Таким образом, металлы и концентрированная серная кислота не реагируют при обычной температуре из-за образования оксидных покрытий на поверхности металла и конкуренции с водородом. Однако, при повышенной температуре или при наличии катализатора может протекать реакция, сопровождающаяся выделением водорода.
Металл и концентрированная серная кислота
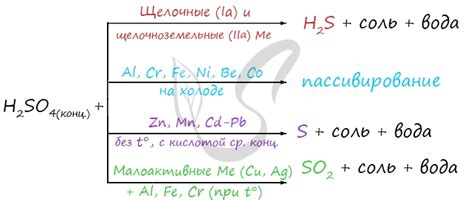
Металл и концентрированная серная кислота обладают совершенно разными свойствами и взаимодействием друг с другом. При обычной температуре они не реагируют между собой. Значит, металл не окисляется и не растворяется в серной кислоте, и серная кислота не обладает достаточной активностью для взаимодействия с металлом.
Металлы обычно обладают электропроводностью и благодаря этому имеют достаточно сильные связи между атомами. Это препятствует взаимодействию металла с серной кислотой, так как серная кислота, как кислота, обычно реагирует с протонами, а не с атомами металла.
Однако, при повышенной температуре или при использовании более активных форм серной кислоты, возможно взаимодействие с металлом. Например, может происходить растворение металла в серной кислоте или формирование солей металла с серной кислотой.
Таким образом, отсутствие реакции между металлом и концентрированной серной кислотой при обычной температуре является результатом недостаточной активности серной кислоты и сильных связей между атомами металла. Для взаимодействия требуется использование более активных условий или других сильных окислителей или кислот, которые могут разрушить связи между атомами металла и способствовать их реакции с серной кислотой.
Отсутствие реакции при обычной температуре

Взаимодействие металлов с концентрированной серной кислотой является известной химической реакцией. Однако, при обычной температуре некоторые металлы не проявляют активность и не реагируют с серной кислотой.
Одной из причин отсутствия реакции является пассивация металла. Некоторые металлы, такие как алюминий и титан, обладают защитным слоем оксида на своей поверхности. Этот оксидные слой предотвращает контакт металла с серной кислотой и защищает его от реакции.
Другой причиной отсутствия реакции может быть низкая химическая активность металла. Например, платина и золото являются малоактивными металлами, поэтому они не реагируют с серной кислотой при обычной температуре.
Также стоит отметить, что некоторые металлы, такие как медь и железо, могут реагировать с серной кислотой при повышенной температуре или при наличии катализаторов. Но при обычной комнатной температуре эти реакции не происходят.
В целом, отсутствие реакции металлов с концентрированной серной кислотой при обычной температуре объясняется пассивацией металла, низкой химической активностью или требованием особых условий для реакции, таких как повышенная температура или наличие катализаторов.
Свойства металла в отношении концентрированной серной кислоты

Концентрированная серная кислота является одним из наиболее агрессивных химических соединений, способных взаимодействовать с металлами. Однако не все металлы проявляют реакцию при обычных температурах.
Алюминий, например, обладает особой защитной пленкой оксида, которая формируется на его поверхности и предотвращает дальнейшее взаимодействие с серной кислотой. Это объясняет его высокую устойчивость к данной кислоте.
Свинец и железо также не реагируют с концентрированной серной кислотой при нормальных условиях, так как образуется защитная пленка оксида на их поверхности. Однако, в отличие от алюминия, данная пленка на железе и свинце образуется с трудом и может быть разрушена при возросшей кислотности.
Медь и проявляют активность в отношении концентрированной серной кислоты. Имея устойчивость к оксидации, эти металлы реагируют с кислотой, образуя соответствующие соли и выделяя водород. В результате металлы растворяются и образуются соответствующие ионы в растворе.
Таблица ниже иллюстрирует реактивность различных металлов в отношении концентрированной серной кислоты:
| Металл | Реакция с серной кислотой |
|---|---|
| Алюминий | Нет реакции |
| Железо | Нет реакции при нормальных условиях, возможно растворение при повышенной кислотности |
| Медь | Образуется сульфат меди и выделяется водород |
| Цинк | Образуется сульфат цинка и выделяется водород |
Таким образом, свойства металлов в отношении концентрированной серной кислоты можно определить исходя из их способности образовывать защитные оксидные пленки на поверхности или вступать в химическую реакцию с кислотой, образуя соответствующие соли и водород.
Применение металла в присутствии концентрированной серной кислоты

Металлы являются важными и широко используемыми материалами во многих отраслях промышленности и научных исследованиях. Однако, взаимодействие металлов с концентрированной серной кислотой требует особого внимания и контроля, так как может привести к различным реакциям и ранениям.
В присутствии концентрированной серной кислоты некоторые металлы образуют нерастворимые соли, что ограничивает их применение. Например, железо и алюминий образуют соответствующие соли, которые обладают низкой растворимостью и могут забивать трубопроводы или вызывать повреждения в процессе смешивания с серной кислотой.
Однако, некоторые металлы, такие как золото и платина, обладают нейтральной реакцией в присутствии концентрированной серной кислоты и не подвергаются разрушительным процессам. Эти металлы могут использоваться в различных областях, включая электронику, химическую промышленность и лабораторные исследования.
Одним из применений металлов в присутствии концентрированной серной кислоты является их использование в процессе электролиза. Например, серебро и медь используются для покрытия поверхности различных предметов, чтобы защитить их от коррозии и повысить их электропроводность. Этот процесс является важным в производстве электронной техники и коммуникационных систем.
Также, металлы в сочетании с концентрированной серной кислотой могут использоваться для получения водорода. Этот процесс известен как водородная эволюция и является одним из способов получения чистого водорода, который широко используется в промышленности, водородных топливных элементах и других технических процессах.
В целом, применение металла в сочетании с концентрированной серной кислотой может быть весьма разнообразным и полезным. Однако, необходимо учитывать специфические свойства каждого металла и контролировать реакции, чтобы избежать опасных ситуаций и обеспечить безопасность в использовании данной комбинации в различных сферах деятельности.
Вопрос-ответ

Почему при обычной температуре нет реакции между металлом и концентрированной серной кислотой?
Ответ: Это происходит из-за того, что серная кислота не является достаточно активным окислителем при нормальных условиях. Таким образом, она не способна окислять металлы, и поэтому нет реакции между ними.
Какие реакции возможны при взаимодействии металла с концентрированной серной кислотой?
Ответ: Взаимодействие металла с концентрированной серной кислотой может привести к различным реакциям в зависимости от активности металла. Например, активные металлы, такие как натрий или калий, могут реагировать со серной кислотой с образованием гидрогена и соли серной кислоты. Однако большинство металлов, включая железо или медь, не реагируют с серной кислотой при обычной температуре и нормальных условиях.
Могут ли некоторые металлы реагировать с концентрированной серной кислотой при повышенных температурах?
Ответ: Да, при повышенных температурах некоторые металлы могут реагировать с концентрированной серной кислотой. Например, сильно нагретое железо может реагировать с серной кислотой, образуя сернистый газ SO2 и водород. Однако при обычной температуре такая реакция не происходит из-за недостаточной активности серной кислоты в качестве окислителя.
