Металл М, находящийся в группе 13 периодической системы элементов, обладает способностью образовывать различные оксиды. Один из таких оксидов — это высший оксид под названием M2O3, где М обозначает атом данного металла. Этот оксид имеет особое значение в научных и промышленных кругах благодаря своим уникальным свойствам и применениям.
Электронная формула M2O3 на валентном энергетическом уровне атома М позволяет нам представить структуру данного оксида и вывести законы его взаимодействия с другими веществами. В электронной формуле атом М представлен символом М, а оксиген атомов — символом O. Число 2 перед атомом М указывает на его двукратную валентность, в то время как число 3 после атома О указывает на трехкратную валентность оксигена.
Электронная формула M2O3 на валентном энергетическом уровне атома М является ключом к пониманию свойств высшего оксида M2O3. Он обладает высокой степенью устойчивости и прочности благодаря особому расположению атомов М и О в его структуре. Изучение электронной формулы M2O3 позволяет установить особенности химических и физических процессов, в которых участвует данный оксид, что открывает новые перспективы его использования в различных областях промышленности и науки.
Металл М образует высший оксид M2O3

Металл М имеет особую способность образовывать высшие оксиды, в том числе M2O3. Этот оксид М2O3 показывает особые химические свойства благодаря электронной формуле, которая указывает на валентный энергетический уровень атома М в этом оксиде.
Электронная формула M2O3 означает, что в оксиде каждый атом М связан с двумя атомами кислорода (О) и обладает степенью окисления, которая соответствует валентному энергетическому уровню атома М. Такая структура оксида M2O3 обусловлена электронной конфигурацией и химическими свойствами металла М.
Высший оксид M2O3 является одним из наиболее стабильных оксидов металла М. Он обладает высокой температурной стойкостью, химической инертностью и способностью формировать кристаллическую структуру. Это обусловлено особыми свойствами валентного энергетического уровня атома М в оксиде M2O3, который обеспечивает стабильность и устойчивость структуры.
Оксид M2O3 используется в различных отраслях промышленности, таких как производство керамики, электроника, лакокрасочные материалы и другие. Его высокая температурная стойкость, устойчивость к химическим реакциям и способность образовывать кристаллическую структуру делают его важным компонентом для многих технологических процессов и материалов.
Структура оксида М2O3 и его валентный энергетический уровень
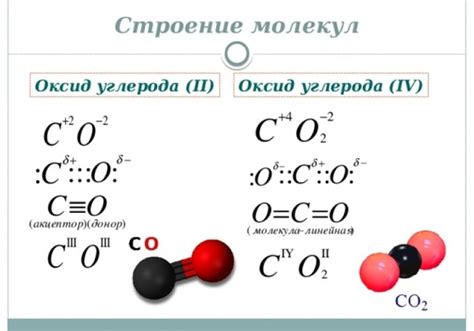
Оксид М2O3 имеет сложную структуру, которая зависит от конкретного элемента Металла М. В основном, оксид M2O3 образует кристаллическую решетку с ионом М в центре и окружающими его атомами кислорода О. Такая структура может быть описана с использованием различных моделей кристаллической решетки, таких как кубическая, гексагональная или ромбоэдрическая.
Валентные энергетические уровни атома М в оксиде М2O3 зависят от его электронной конфигурации. Атом Металла M в оксиде M2O3 имеет несколько энергетических уровней, при которых происходит заполнение электронами. Валентный энергетический уровень представляет собой самый высокий уровень, на котором находятся валентные электроны атома М.
На валентном энергетическом уровне атома Металла М в оксиде M2O3 находятся электроны, которые могут участвовать в химических реакциях и образовании связей с другими атомами. Эти электроны имеют определенное количество энергии, которое зависит от их состояния и расположения в энергетической структуре атома М.
Знание о структуре оксида M2O3 и его валентном энергетическом уровне позволяет более глубоко понять его свойства и способность взаимодействовать с другими веществами. Это важно при изучении и применении оксида M2O3 в различных областях, таких как химия, электроника и материаловедение.
Электронная формула оксида M2O3 и его влияние на валентный энергетический уровень атома М

Оксид M2O3 представляет собой химическое соединение, в состав которого входит атом металла М и три атома кислорода О. Это вещество обладает высокой степенью окислительных свойств и широко применяется в различных отраслях промышленности.
На валентном энергетическом уровне атома М оксид M2O3 влияет следующим образом: в соединении атомы металла образуют ковалентные связи с атомами кислорода. При этом атом М отдает электроны на валентный уровень кислорода, формируя положительный заряд. В результате образуется положительно заряженный ион М3+, который вступает во взаимодействие с отрицательно заряженными ионами кислорода.
Электронная формула M2O3 отображает распределение электронов на различных орбиталях атомов компонентов соединения. На валентном энергетическом уровне атома М находится определенное количество электронов, которые обеспечивают его взаимодействие с другими атомами. Этот уровень определяет химические свойства и реактивность атома М в соединении.
Оксид M2O3 играет важную роль в металлургии и химической промышленности, так как обладает высокой степенью стабильности и устойчивости. Он используется для получения различных металлических соединений, катализаторов и материалов для изготовления электронных приборов. Поэтому понимание электронной формулы M2O3 и его воздействия на валентный энергетический уровень атома М является важным для разработки новых материалов и технологий.
Способы получения исследуемого вещества с высокой степенью окисления
Исследуемое вещество с высокой степенью окисления - высший оксид M2O3, может быть получено различными способами. Одним из наиболее распространенных способов является термическое разложение соответствующего низшего оксида.
Для этого низший оксид MО сначала получают через реакцию взаимодействия металла с кислородом или через прямое окисление металла. Затем полученный низший оксид подвергают термическому разложению при определенной температуре и условиях.
Еще одним способом получения исследуемого вещества является метод электролиза или электрохимического осаждения. В этом случае используют электролит, содержащий соответствующий металл, и проводят электролиз при определенных условиях. В результате этого процесса на электроде осаждается исследуемый высший оксид.
Также возможен метод химического окисления. Для этого используют реагенты, способные окислить металл до нужной степени окисления. Реакции окисления проводятся в соответствующих растворах или смесях реагентов, и в результате образуется исследуемый высший оксид.
Исследуемое вещество с высокой степенью окисления имеет важное применение в различных отраслях науки и техники. Его свойства и возможности применения исследуются в таких областях, как химия материалов, электроника, катализ и многие другие.
Анализ химических реакций при получении и использовании оксида M2O3
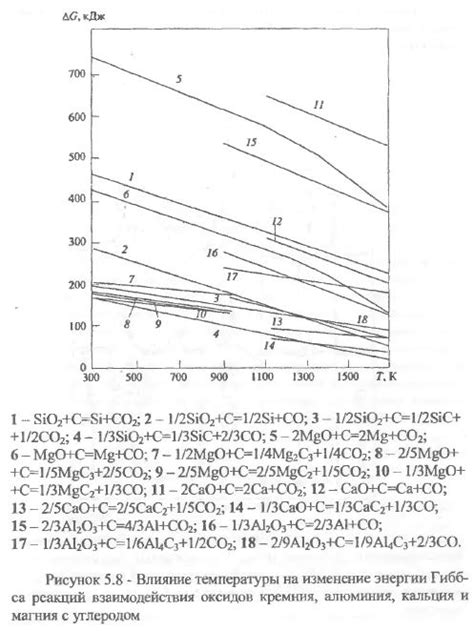
Оксид M2O3 является высшим оксидом металла М и образуется путем окисления этого металла. Химическая реакция при получении оксида M2O3 может быть представлена следующим образом:
M + 3/2 O2 -> M2O3
В данной реакции металл М окисляется до своего высшего оксидного состояния, а молекула кислорода вступает в связь с атомами металла, образуя молекулу оксида M2O3.
Оксид M2O3 имеет широкое применение в различных отраслях промышленности. Например, этот оксид используется в производстве керамики, стекла и электронных компонентов. Также он применяется в составе катализаторов и в процессе синтеза различных органических соединений.
Оксид M2O3 обладает химической активностью и способен вступать в реакции с другими веществами. Например, при обработке оксида M2O3 водой, происходит реакция гидролиза:
M2O3 + 3H2O -> 2MO(OH)3
В результате этой реакции оксид M2O3 превращается в гидроксид MO(OH)3, который находит применение в производстве красителей и пигментов.
Также оксид M2O3 может вступать в реакцию с кислотами, образуя соли металла М:
M2O3 + 6HCl -> 2MCl3 + 3H2O
Данная реакция приводит к образованию хлорида металла М и молекулы воды. Такие соли металла М находят применение, например, в производстве стекла и керамики.
Изменение свойств оксида M2O3 при взаимодействии с другими веществами

Оксид M2O3 обладает рядом свойств, которые могут изменяться при взаимодействии с другими веществами. Одним из таких веществ может быть кислород, который может реагировать с оксидом M2O3, образуя новые оксиды и изменяя его структуру.
Если оксид M2O3 взаимодействует с кислородом, то может образоваться более высокий оксид М2О5. В этом случае структура оксида меняется, и он становится менее стабильным. Это может привести к потере его основных свойств и способности реагировать с другими веществами.
Кроме кислорода, оксид M2O3 также может взаимодействовать с другими элементами и соединениями, такими как кислоты и основания. При таких реакциях могут образовываться соли, которые могут изменять свойства оксида M2O3 и его способность взаимодействовать с другими веществами.
Взаимодействие оксида M2O3 с водой также может изменять его свойства. Вода может вызывать гидролиз оксида, образуя гидроксиды и ионы. Это может привести к изменению структуры оксида и его растворимости в воде.
Таким образом, оксид M2O3 может проявлять различные свойства и взаимодействовать с другими веществами, что может влиять на его структуру и способность реагировать с окружающей средой.
Важные прикладные аспекты оксида M2O3 и его использование в современных технологиях

Оксид M2O3 является одним из наиболее важных соединений металла М, благодаря своим уникальным свойствам и широкому спектру применений в современных технологиях. Электронная формула данного оксида на валентном энергетическом уровне атома М представляется как М(III)O3.
Оксид M2O3 обладает высокой химической стабильностью и является непроводящим материалом. Это позволяет использовать его в качестве диэлектрического слоя в различных электронных устройствах. Экспериментальные исследования показывают, что оксид M2O3 может быть использован в качестве полупроводника. Благодаря этим свойствам оксид M2O3 нашел широкое применение в производстве полупроводниковых компонентов и микрочипов.
Кроме того, оксид M2O3 обладает высокой термической и химической стабильностью, что делает его идеальным материалом для использования в высокотемпературных и агрессивных условиях. Он применяется в производстве катализаторов, которые используются в процессах газоочистки и производстве синтетических материалов.
В современных технологиях оксид M2O3 широко используется в производстве электронных устройств, аккумуляторов, солнечных батарей, светодиодов и других устройств, работающих на основе полупроводниковых компонентов. Он также применяется в производстве керамики, стекла и защитных покрытий благодаря своей высокой термической и химической стойкости.
Выводя наши рассуждения, мы можем сделать вывод о важных прикладных аспектах оксида M2O3 и его использовании в современных технологиях. Этот материал обладает высокой химической и термической стабильностью, а также имеет уникальные свойства, которые позволяют ему быть использованным в различных сферах, таких как электроника, полупроводники, катализ и защитные покрытия.
Вопрос-ответ

Какая электронная формула на валентном энергетическом уровне атома М?
На валентном энергетическом уровне атома М металла М формируется электронная формула MO3, где M - символ для металла, а 3 - указывает на количество кислородных атомов.
Почему металл М образует высший оксид M2O3?
Металл М образует высший оксид M2O3, так как в его электронной формуле валентная оболочка атома М может принять три электрона от трех молекул кислорода, образуя трехвалентный катион M3+. В результате такой обмен электронами формируется структура оксида M2O3.
