Металлы и неметаллы – это два основных класса химических элементов, которые встречаются в природе и широко используются в промышленности. Но сколько веков назад появились эти вещества в своих нынешних формах? Какую роль они играют в развитии живых организмов и окружающей среды?
Начнем с металлов. Эти твердые, блестящие и хорошо проводящие тепло и электричество вещества обладают рядом уникальных свойств, делающих их незаменимыми в различных отраслях экономики. Первые металлы, обнаруженные человеком, были медь, свинец, железо и золото. Их добыча и использование принесли огромные выгоды обществам, ускорив развитие технологий и промышленности.
С другой стороны, неметаллы – это вещества, которые обычно не обладают металлическими свойствами, такими как блеск и хорошая теплопроводность. Они играют важную роль в органической химии, их соединения используются в производстве пластмасс, керамики, стекла и других материалов. Некоторые неметаллы, такие как кислород и азот, являются необходимыми для жизни живых организмов и составляют значительную долю земной атмосферы.
История эволюции металлов и неметаллов до сих пор остается предметом научных исследований. Однако, несмотря на то, что металлы были обнаружены и использованы раньше, неметаллы также играют важную роль в развитии жизни на Земле.
В итоге, хотя металлы и неметаллы различаются по своим химическим и физическим свойствам, они оба важны для жизни на планете Земля. Их встречают в природе в разных соединениях и использование их в промышленности имеет огромное значение для человеческого прогресса.
Внутреннее строение атома
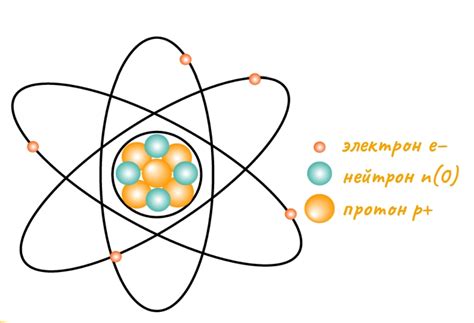
Атом - это наименьшая единица вещества, имеющая все его химические свойства. Внутренняя структура атома состоит из ядра и электронной оболочки. Ядро находится в центре атома и состоит из протонов и нейтронов. Протоны имеют положительный заряд, а нейтроны не имеют заряда и являются нейтральными частицами.
Именно в ядре атома находится большая часть массы атома, в то время как электроны находятся в оболочке вокруг ядра. Электроны имеют отрицательный заряд и обладают очень малой массой по сравнению с протонами и нейтронами. Их количество в атоме равно количеству протонов и определяет его химические свойства и валентность.
Электроны располагаются в энергетических уровнях или оболочках. Каждая оболочка может содержать определенное количество электронов: первая оболочка может содержать до 2 электронов, вторая - до 8 электронов, третья - до 18 электронов и так далее. Оболочки расположены одна за другой и электроны могут двигаться на разных энергетических уровнях вокруг ядра.
Взаимодействие электронов и ядра атома обусловлено электромагнитными силами. Протоны и электроны притягиваются друг к другу, так как протоны имеют положительный заряд, а электроны - отрицательный. Нейтроны не взаимодействуют электростатически с электронами, так как они нейтральны. Ядро является стабильной частью атома и определяет его химические и физические свойства.
Основные составляющие атома
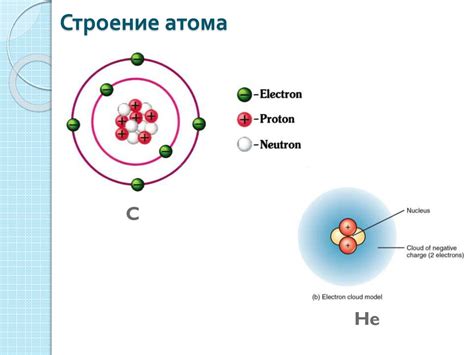
Атом - наименьшая частица вещества, обладающая свойствами элемента. Он состоит из нескольких основных составляющих: ядра и электронной оболочки.
Ядро атома содержит протоны и нейтроны. Протоны имеют положительный заряд, а нейтроны не имеют заряда вообще. Вместе они определяют массу атома и называются нуклонами.
Электронная оболочка атома содержит электроны - отрицательно заряженные частицы. Они обращаются по орбитальным уровням вокруг ядра и определяют электрическую структуру атома. Количество электронов в атоме равно количеству протонов в ядре, что обеспечивает электрическую нейтральность атома.
Строение и свойства атомов различаются в зависимости от элемента. Элементы отличаются друг от друга количеством протонов в ядре, а следовательно, их атомные номера различны. Атомы с одинаковым атомным номером, но разным числом нейтронов, называются изотопами.
Расположение электронов в атоме
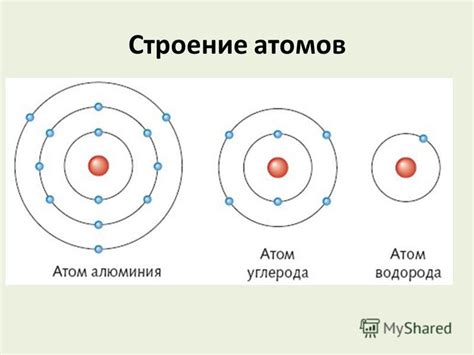
Атом состоит из ядра, в котором находятся протоны и нейтроны, а также электронов, которые обращаются по определенным орбитам вокруг ядра. Расположение электронов в атоме определяет его химические свойства и поведение в химических реакциях.
Электроны в атоме могут находиться на различных энергетических уровнях, которые называются электронными оболочками. На каждом энергетическом уровне может находиться ограниченное количество электронов. Первая электронная оболочка может вместить только 2 электрона, вторая - 8 электронов, третья - 18 электронов и т.д.
Электроны в атоме распределены по орбиталям - трехмерным областям пространства, в которых с большей вероятностью можно обнаружить электрон. Орбитали бывают различных форм и направлений, они могут быть сферическими, плоскими или сложными по форме.
Распределение электронов по орбиталям соблюдает правила заполнения, которые определяют порядок заполнения и максимальное количество электронов на каждой орбитали, а также условия исключения (принцип Паули) и закона сохранения спина (принцип Хунда).
Химические свойства металлов

Металлы являются категорией химических элементов с отличительной группой свойств. Они обладают высокой теплопроводностью, являются хорошими проводниками электричества и способны подвергаться пластической деформации без разрушения.
Металлы также обладают высокой плотностью и твердостью, а их атомы образуют кристаллическую решетку, что обусловливает их металлический блеск. Они часто образуют сплавы с другими металлами или неметаллами, что позволяет улучшать их механические и химические свойства.
Химические реакции металлов хорошо изучены и определяются их положением в периодической системе. Металлы активно взаимодействуют с кислородом, образуя оксиды. Они также способны реагировать с водой, выделяя водород. Металлы могут вытеснять друг друга из их соединений, используя силу своей окислительной способности.
Металлы обычно образуют катионы и обладают положительным окислительным числом. Они могут образовывать ионы разных зарядов, обуславливая возможность существования различных степеней окисления металлов. Металлы химически активны и могут участвовать во множестве реакций, образуя соединения с другими элементами.
Химические свойства неметаллов

Неметаллы – это элементы, обладающие особыми химическими свойствами, которые отличают их от металлов. Они обычно образуют ковалентные соединения и обладают высокой электроотрицательностью. Неметаллы являются прекрасными изоляторами тепла и электричества, что делает их особенно полезными в электронике и строительстве.
Одно из самых важных химических свойств неметаллов – их способность образовывать кислотные оксиды. Кислотные оксиды реагируют с водой, образуя кислоты. Например, оксид серы (SO2) реагирует с водой и образует серную кислоту (H2SO4). Это свойство позволяет неметаллам играть важную роль в химической промышленности и в процессе формирования климата на Земле.
Неметаллы также обладают способностью образовывать соли с металлами. Например, хлор (Cl) образует соль с натрием (NaCl), известную как поваренная соль. Это свойство неметаллов является основой для создания множества химических соединений, в том числе и лекарственных препаратов.
Некоторые неметаллы, такие как кислород, азот и фосфор, играют важную роль в жизни организмов. Они являются частью молекул, составляющих ДНК, белки и другие вещества, необходимые для поддержания жизнедеятельности. Без неметаллов невозможно существование биологических организмов и процессов.
Переходные элементы и их роль

Переходные элементы представляют собой группу химических элементов, у которых число электронов во внешней электронной оболочке может изменяться. Они находятся в двух блоках таблицы химических элементов - d-блоке и f-блоке.
Одной из главных ролей переходных элементов является их способность образовывать ионные соединения различных степеней окисления. Это связано с возможностью изменения заряда переходных металлов благодаря взаимодействию их электронов с окружающими элементами.
Переходные элементы также служат важными катализаторами в химических реакциях. Благодаря своей способности изменять свою электронную структуру, они способны активировать реагенты, ускоряя химические процессы.
Другая значимая роль переходных элементов заключается в их способности образовывать комплексные соединения с другими элементами. Комплексные соединения переходных элементов имеют сложную структуру и обладают уникальными свойствами, такими как изменение цвета или магнитные свойства. Именно эти свойства делают переходные элементы незаменимыми в различных сферах науки и техники.
В целом, переходные элементы играют важную роль в химии и природе, обладая уникальными свойствами, которые обусловлены их электронной структурой и способностью изменять свою орбитальную конфигурацию. Изучение переходных элементов позволяет не только расширить наши знания о химических свойствах элементов, но и применять их в различных областях науки и техники.
Эволюция элементов в природе

Эволюция элементов в природе – это процесс изменения и развития химических элементов на протяжении миллионов лет. Каждый элемент имеет свою историю возникновения и эволюции, которая связана с геологическими процессами и преобразованиями внутри Земли.
В самом начале существования Вселенной после Большого взрыва образовались самые легкие элементы - водород и гелий. Они стали основой для образования звезд и галактик. В звездных ядрах происходят ядерные реакции, в результате которых образуются более тяжелые элементы, такие как кислород, карбон и железо.
Дальнейшая эволюция элементов происходит при взаимодействии звезд. В результате вспышек сверхновых звезд могут образовываться тяжелые элементы, такие как золото, серебро и уран. Эти элементы распространяются по всей Вселенной и затем, при определенных условиях, могут попадать на Землю в виде метеоритов.
На Земле происходят и другие процессы эволюции элементов, связанные с геологическими процессами. Например, при вулканической активности могут образовываться новые минералы и руды, содержащие различные элементы. Эти минералы могут быть добыты человеком и использованы для производства различных материалов.
Важно отметить, что эволюция элементов в природе не является линейным процессом, и разные элементы могут появляться и развиваться в разное время. Некоторые элементы, такие как вольфрам, формировались в основном во время ранней истории Земли, в то время как другие элементы, такие как свинец, железо и магний, появились позже.
Сравнение распространенности металлов и неметаллов
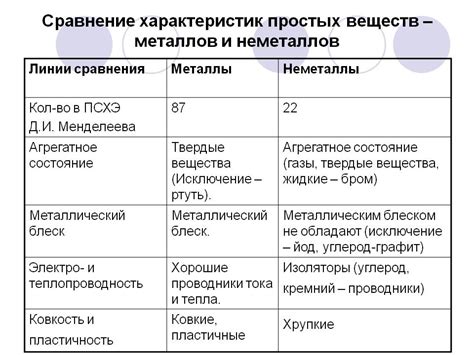
Металлы и неметаллы - это две основные категории химических элементов, которые имеют существенные различия в своих свойствах и распространенности в природе.
Металлы обладают высокой тепло- и электропроводностью, высокой пластичностью и прочностью. Они широко распространены в земной коре и составляют около 75% периодической таблицы элементов. Некоторые наиболее распространенные металлы, такие как железо, алюминий и медь, имеют широкое применение в промышленности и строительстве.
Неметаллы, в отличие от металлов, обладают низкой теплопроводностью, не обладают металлическим блеском и часто имеют низкую пластичность и прочность. Они составляют около 25% периодической таблицы элементов и включают такие элементы, как кислород, сера и фосфор. Неметаллы встречаются в различных природных материалах, таких как воздух, вода, органические соединения и минералы.
Оба типа элементов необходимы для поддержания жизни на Земле. Металлы используются в различных отраслях промышленности, производстве, строительстве и энергетике. Неметаллы играют важную роль в биологических процессах, химической промышленности и производстве электроники.
В целом, металлы и неметаллы являются важными элементами нашей окружающей среды и их распространенность в природе, химические свойства и применение существенно отличаются, делая их уникальными и неотъемлемыми компонентами нашего мира.
Вопрос-ответ

В каком периоде возникла первая металлическая форма в природе?
Первая металлическая форма - свинец возник в природе примерно 7 тысяч лет назад.
Можно ли сказать, что металлы появились раньше неметаллов?
Да, металлы появились в природе раньше неметаллов. Самыми ранними металлами, которые были обнаружены человеком, являются золото, медь и свинец.
Какие неметаллы были известны раньше металлов?
Самыми ранними известными неметаллами являются сера, фосфор и углерод. Они были известны человечеству задолго до открытия металлов.
Какие примеры можно привести в качестве неметаллов, известных из древности?
Неметаллы, известные из древности, включают серу, углерод, фосфор, йод и многое другое. Они использовались в различных областях, включая медицину, строительство и производство огнестрельного оружия.
