Вода является одним из наиболее распространенных веществ на Земле и играет важную роль в химических реакциях. Одной из таких реакций является взаимодействие воды с неорганическими соединениями металлов. Такие реакции широко применяются в различных отраслях науки и промышленности.
Вода проявляет активность при взаимодействии с металлическими ионами, образуя гидроксиды металлов. Это связано с тем, что вода обладает способностью как выполнять роль акцептора электронов, так и донора. В результате этого взаимодействия образуются гидроксоны, которые влияют на различные процессы и свойства металлов и их соединений.
Важным аспектом реакции воды с неорганическими соединениями металлов является образование гидроксид-ионов, которые способны взаимодействовать с другими веществами и обеспечивать разнообразные химические реакции. Кроме того, реакция воды с металлами может сопровождаться образованием газовых продуктов, таких как водород.
Изучение реакции воды с неорганическими соединениями металлов является важной задачей современной науки. Это позволяет получить новые знания о химических свойствах металлов и их соединений, а также использовать эти реакции в промышленности для производства различных соединений и материалов.
Вода - идеальный растворитель для неорганических соединений

Вода является одним из самых распространенных и важных растворителей неорганических соединений металлов. Благодаря своей универсальности и уникальным химическим свойствам, она предоставляет много возможностей для реакций с различными металлическими соединениями. Например, растворение металлов в воде может быть использовано для получения и изучения различных веществ и материалов.
Вода обладает способностью образовывать соединения с различными ионами металлов. Она может образовывать гидраты, в которых ионы металла окружены молекулами воды. Гидраты могут иметь различные структуры и свойства в зависимости от ионной радиуса и заряда металла.
Вода также может служить средой для гидролиза неорганических соединений металлов, при котором они расщепляются на ионы металла и ионы гидроксида. Гидролиз может быть важным процессом для понимания и изучения свойств и реакций неорганических соединений.
Кроме того, вода может быть использована для получения растворов разных концентраций, с помощью которых можно изменять условия реакций с неорганическими соединениями металлов. Разные концентрации водных растворов могут оказывать различное влияние на скорость и характер реакций, что открывает широкие возможности для исследований и применений в области химии металлов.
Таким образом, вода является идеальным растворителем для неорганических соединений металлов, обладая своими уникальными химическими свойствами и способностью образовывать различные типы соединений с металлами. Это делает ее незаменимым инструментом для изучения и применения неорганической химии металлов.
Обзор процесса взаимодействия
Вода – универсальный растворитель, способный взаимодействовать с различными неорганическими соединениями металлов. Это происходит за счет химических реакций, которые происходят в процессе совместного действия воды и металлических ионов.
Важным аспектом этого процесса является реакция воды с ионами металла, которая может привести к образованию гидроксидов. Гидроксиды металлов обладают особыми свойствами и могут выступать в качестве оснований или кислотных оксидов в различных химических реакциях.
Кроме того, вода может оказывать влияние на процесс окисления и восстановления металлов. Вода способна участвовать в окислительно-восстановительных реакциях и, в зависимости от условий, может активировать процесс окисления металлов или наоборот, действовать как восстановитель.
Обзор процесса взаимодействия воды с неорганическими соединениями металлов поможет лучше понять химические свойства и реактивность металлов в различных средах. Это важно для многих областей научного и технического развития, включая металлургическую промышленность, химическую промышленность, электрохимию и другие.
Металлы и их реакция с водой

Металлы, как класс химических элементов, отличаются способностью вступать в реакцию с водой. Реакция металлов с водой может быть различной: от медленной и бесшумной до мгновенной и с производством газа или конкретного вещества.
Некоторые металлы не реагируют с водой вообще, как, например, золото и платина, и являются химически инертными. Другие металлы, такие как натрий и калий, реагируют мгновенно с водой, образуя щелочные растворы и выделяя водородный газ.
Реакция металлов с водой определяется их активностью. Чем активнее металл, тем более сильна его реакция с водой. Наиболее активные известные металлы - щелочные и щелочноземельные металлы, такие как литий, натрий, калий, магний и кальций.
Реакция металлов с водой может быть использована в различных процессах и применениях. Например, в производстве водорода, когда металлы, такие как алюминий или цинк, реагируют с водой, образуя водородный газ. Также реакция металлов с водой может применяться для очистки и удаления загрязнений с поверхностей металлических изделий.
Важно отметить, что реакция металлов с водой может быть опасной, и во время проведения экспериментов или промышленных процессов необходимо соблюдать соответствующие меры безопасности. Кроме того, некоторые металлы могут образовывать токсичные соединения при взаимодействии с водой, поэтому важно быть внимательным и осторожным при обработке металлических материалов.
Термические и химические аспекты

Реакция воды с неорганическими соединениями металлов является процессом, в котором вода вступает во взаимодействие с различными химическими веществами, содержащими металлы. Эта реакция может быть как термической, так и химической по своей природе.
Термические аспекты реакции представляют собой процессы затраты или выделения тепла при соприкосновении воды с металлом. В ряде случаев, при взаимодействии с водой, некоторые металлы могут реагировать с активным выделением тепла. Это связано с процессами окисления, при которых энергия связей металла с кислородом воды высвобождается в виде тепла.
Химические аспекты реакции включают в себя изменения химической структуры и свойств исходных веществ при воздействии воды. Некоторые металлические соединения могут быть растворимы в воде и образовывать ионы, что приводит к возникновению химических реакций с образованием новых соединений. Такие реакции особенно значимы в процессе коррозии металлов, когда вода приводит к разрушению поверхности металла и образованию окислов и гидроксидов.
Термические и химические аспекты реакции воды с неорганическими соединениями металлов играют важную роль в различных областях науки и промышленности, включая энергетику, химическую промышленность, металлургию и другие отрасли.
Осадки и растворение в процессе

Вода является универсальным растворителем и способна реагировать с различными неорганическими соединениями металлов, образуя осадки или идя в растворение. Эти процессы являются важными в различных областях науки и техники, таких как химия, геология и аналитическая химия.
Осадки могут образовываться, когда реакция между водой и неорганическими соединениями металлов приводит к образованию нерастворимых соединений. Например, при реакции железа с водой образуется окись железа, которая является нерастворимым осадком. При наличии других ионов в растворе, осадки могут образовываться в виде кристаллов или аморфных частиц.
С другой стороны, некоторые неорганические соединения металлов могут растворяться в воде, образуя ионы металла и анионы. Например, соляная кислота растворяет металлический алюминий, образуя алюминий хлорид и водород. Этот процесс называется растворением металла.
Осадки и растворение являются важными процессами в химических реакциях с неорганическими соединениями металлов. Они могут быть использованы для выделения конкретных металлов из растворов и обеспечения чистоты и плотности получаемых продуктов. Кроме того, они имеют важное значение для понимания геологических процессов и формирования природных ресурсов.
Влияние pH на скорость процесса

Положительные или отрицательные ионы в реакции воды с неорганическими соединениями металлов могут влиять на скорость процесса в зависимости от значения pH раствора. Реакция воды с металлическими соединениями может происходить быстрее в кислых или щелочных условиях, поскольку протоны и гидроксидные ионы могут взаимодействовать с ионами металла, ускоряя или замедляя реакцию.
При нейтральном pH вода обычно проявляет слабую взаимодействие с неорганическими соединениями металлов, что может приводить к более медленной скорости реакции. Однако при более кислых условиях, когда в растворе присутствуют достаточные количества протонов, реакция может произойти более быстро. Также, при щелочных условиях, когда в растворе присутствуют гидроксидные ионы, реакция может протекать с большей скоростью.
Влияние pH на скорость процесса также может быть связано с образованием сложных соединений металла с водой или другими веществами в растворе. Например, в растворах с низкими значениями pH может образовываться кислый комплексный ион, который может существенно ускорять реакцию между водой и соединением металла. Наоборот, в растворах с высокими значениями pH может образовываться щелочной комплексный ион, который может замедлить реакцию.
Роль воды в коррозии металлов
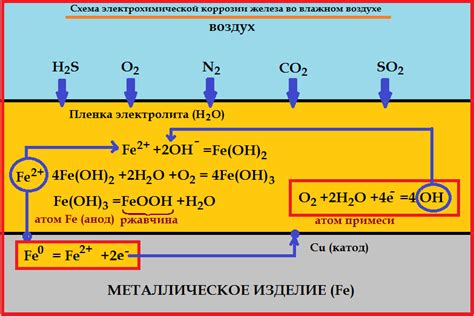
Вода играет важную роль в коррозии металлов. Коррозия представляет собой процесс, в результате которого металлы подвергаются разрушению из-за химической реакции с окружающей средой. Вода, содержащая в себе различные растворенные соли и газы, является одним из наиболее распространенных факторов, вызывающих коррозию.
Вода может способствовать коррозии металлов, так как является электролитом, то есть в ней содержатся свободные ионы, которые могут участвовать в химических реакциях с поверхностью металла. К примеру, вода может разлагать металл на ионы, что приводит к образованию окислов и гидроксидов металла, что и вызывает коррозию.
Особенно неблагоприятными для металлов являются воды с пониженной или повышенной кислотностью. Кислотная среда может приводить к активному разложению металла и образованию коррозионных пятен и продуктов. С другой стороны, щелочные среды также способны вызвать коррозию путем разлагания оксидных пленок на поверхности металла.
Однако не все металлы одинаково подвержены коррозии в воде. Некоторые металлы, такие как алюминий и цинк, обладают более высокой коррозионной активностью и могут быстро разлагаться в присутствии воды. В то время как другие металлы, например, нержавеющая сталь или платина, обладают стойкостью к коррозии в большей степени.
В целом, понимание роли воды в коррозии металлов позволяет разработать эффективные методы защиты металлов от коррозии, такие как покрытия и покрытия для предотвращения контакта с водой и другими коррозионно-активными средами.
Вопрос-ответ

Как происходит реакция воды с металлом?
Реакция воды с металлом может происходить двумя способами: непосредственно с металлом или через образование соединения, в котором металл уже окислен.
Что происходит при непосредственной реакции воды с металлом?
При непосредственной реакции воды с металлом образуется гидроксид металла и выделяется водородный газ. Например, при реакции воды с железом образуется гидроксид железа и выделяется водородный газ по следующей реакции: Fe + 2H2O -> Fe(OH)2 + H2.
Что происходит при реакции воды с оксидами металлов?
При реакции воды с оксидами металлов образуется гидроксид металла. Например, при реакции оксида натрия с водой образуется гидроксид натрия по следующей реакции: Na2O + H2O -> 2NaOH.
Какие факторы влияют на скорость реакции воды с металлом?
Скорость реакции воды с металлом зависит от ряда факторов. Одним из них является активность металла - чем активнее металл, тем быстрее будет протекать реакция. Также влияет наличие катализаторов, концентрация реагентов, температура и давление.
