Металлы - это вещества, которые обладают специфическими химическими и физическими свойствами. Одним из таких свойств является малое число атомов металла. Атомы металла обычно имеют небольшое количество электронов в своей внешней оболочке, что делает их стабильными и способными к химическим реакциям.
Малое число атомов металла также обусловлено специфической структурой их кристаллической решетки. Атомы металла образуют регулярную многомерную сетку, в которой каждый атом окружен своими соседями. Эта структура делает металлы прочными и пластичными, что способствует их использованию в различных промышленных отраслях.
Малое число атомов металла также обусловлено их высокими физическими свойствами. Металлы обладают высокой теплопроводностью и электропроводностью, благодаря чему они находят применение в электронике и энергетике. Кроме того, металлы обладают высокой плотностью, что делает их полезными материалами для строительства и изготовления различных изделий.
Малое число - особенность атомов металла

Атомы металлов характеризуются малым числом электронов в своей внешней оболочке. Это основная особенность их строения. В общем случае, атом состоит из ядра и облака электронов, расположенных на различных энергетических уровнях.
Малое число электронов в внешней оболочке атома металла обусловлено его положением в периодической системе элементов. Металлы находятся в левой части системы и их атомы имеют небольшое количество электронов во внешней оболочке, чаще всего один или два.
Эта особенность атомов металла делает их химически активными, так как они стремятся стабилизировать свою электронную конфигурацию, передавая электроны другим атомам. Именно из-за этой способности металлы обладают хорошей проводимостью тока и тепла, а также обладают высокой пластичностью и металлическим блеском.
Малое число электронов во внешней оболочке также позволяет атомам металла образовывать кристаллическую решетку, где атомы металла образуют плотно упакованный кристаллический решетки. Это также обеспечивает металлам высокую плотность и твердость.
Атомы металлов имеют небольшое количество электронов

Металлы - это группа химических элементов, которые обладают определенными физическими и химическими свойствами. Одним из основных характеристик металлов является их строение на атомном уровне.
В отличие от неметаллов, которые имеют большое количество электронов во внешней оболочке, у атомов металла количество электронов внешней оболочке достаточно низкое. Это свойство влияет на их химическую активность и способность образовывать связи с другими элементами.
Малое число электронов в внешней оболочке атомов металла позволяет им быть легкоионизируемыми, то есть иметь способность отдавать электроны другим элементам. Это является основой для формирования ионных связей в металлах и их соединениях.
Кроме того, малое количество электронов в внешней оболочке атомов металла обуславливает их высокую электропроводность. Образование свободных электронов в металле позволяет электронам свободно двигаться в его структуре, что обеспечивает передачу электрического тока.
В целом, малое число электронов в атомах металлов способствует их специфическим свойствам, таким как гибкость, хорошая теплопроводность и высокая пластичность. Эти особенности делают металлы важными материалами в различных областях промышленности и технологии.
Одна из особенностей металлических атомов - низкая электроотрицательность
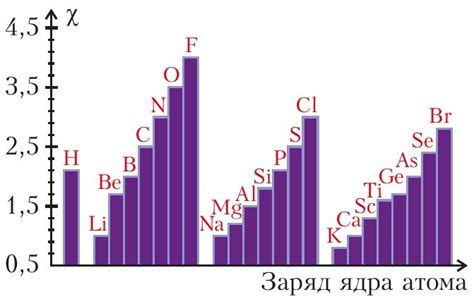
Металлические атомы отличаются низкой электроотрицательностью, что является одной из характерных особенностей этого класса элементов. Электроотрицательность - это способность атома притягивать к себе электроны в химической связи. Чем выше электроотрицательность, тем сильнее атом притягивает электроны и тем более полярную связь он может образовывать.
Металлы обладают малым числом электроотрицательности из-за своей специфической структуры атомов. В металлах электроны находятся в общей зоне проводимости, что позволяет им свободно двигаться через кристаллическую решетку и образовывать электрический ток. Сила притяжения атомов к электронам в металлах оказывается меньше по сравнению с атомами неметаллов, где электроны занимают определенные области вокруг ядер.
- Низкая электроотрицательность металлов обусловливает их способность отдавать электроны другим атомам. Именно этим обусловлены характерные химические свойства металлов, например, способность к образованию положительных ионов.
- Металлические связи, в которых металлы предоставляют свои электроны в общую электронную оболочку, обеспечивают уникальные свойства металлов, такие как высокая теплопроводность и электропроводность.
- Электроотрицательность металлов также определяет химическую активность металлических соединений, которая нередко проявляется в реакциях с кислотами, восстановительных свойствах и способности образовывать сложные соединения.
Важно отметить, что существуют различия в электроотрицательности между различными элементами металлов. Например, литий и калий обладают высокой электроотрицательностью по сравнению с другими металлами, что делает их особыми в контексте реакций и свойств соединений, в которых они принимают участие.
Низкая масса атомов металла – причина их малого размера
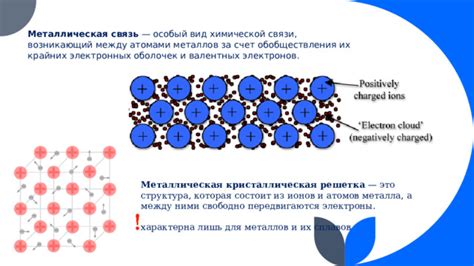
Металлы – элементы периодической таблицы, обладающие высокой проводимостью тепла и электричества, а также обычно имеющие блестящую поверхность. Одним из характерных свойств металлов является их малый размер атомов. Это является результатом низкой массы атома металла.
Атомы металлов отличаются довольно малой массой по сравнению с другими элементами периодической таблицы. Низкая масса атомов металла обуславливает их малый размер. Как известно, атом состоит из позитивно заряженного ядра, вокруг которого движутся отрицательно заряженные электроны. Они находятся на определенных энергетических уровнях. Малая масса атома металла обуславливает их близкое расположение друг к другу.
Такое близкое расположение атомов металла влияет на их свойства. Малый размер атомов обеспечивает металлам своеобразное строение кристаллической решетки. В этой решетке атомы металла располагаются в виде плотно упакованных сфер, образуя плоскости и ряды. Благодаря этому металлы обладают высокой плотностью и прочностью. Низкий размер атомов также позволяет металлам образовывать дефекты кристаллической решетки, такие как проводимость, магнетизм и термическое расширение.
Металлические атомы и их высокая проводимость электричества

Одной из характеристик металлических атомов является их высокая проводимость электричества. Это связано с особенностями строения и связи между атомами в металлической решетке.
Металлы обладают специфической структурой, называемой кристаллической решеткой, в которой атомы расположены в определенном порядке и тесно связаны друг с другом. В этой решетке атомы находятся на фиксированных позициях, образуя трехмерную сетку.
Электрическая проводимость металлов обусловлена наличием свободных электронов. В металлической решетке электроны, находящиеся на внешних энергетических уровнях атомов, могут свободно перемещаться по всей структуре. Они являются общими для всех атомов металла и образуют так называемое "электронное облако".
Электрический ток представляет собой перемещение заряженных частиц. В случае металлов это перемещение свободных электронов. Когда между двумя точками в металле устанавливается разность потенциалов, свободные электроны начинают двигаться под действием электрического поля. Они передают энергию друг другу в процессе соударений, образуя электрический ток.
Таким образом, наличие свободных электронов и их возможность свободного перемещения позволяют металлам обладать высокой проводимостью электричества. Это делает металлы незаменимыми материалами во многих областях, включая электротехнику, электронику и электроэнергетику.
Вопрос-ответ

Почему малое число характерно для атомов металла?
Малое число характерно для атомов металла из-за особенностей их структуры. Атомы металла имеют большой размер и массу, поэтому пространство между ними в кристаллической решетке металла является значительным. Это приводит к малой плотности атомов в металле и, как следствие, к малому числу атомов в данной массе металла.
Какая связь между размером атомов металла и их количеством?
Размер атомов металла влияет на их количество в данной массе металла. Атомы металла имеют большой размер и массу, поэтому пространство между ними в кристаллической решетке металла является значительным. Чем больше размер атома, тем больше пространства между атомами и, соответственно, меньше количество атомов в данной массе металла.
Какие факторы влияют на количество атомов металла в данной массе?
Количество атомов металла в данной массе зависит от размера атомов, их плотности и кристаллической решетки металла. Атомы металла имеют большой размер и массу, поэтому пространство между ними в кристаллической решетке металла является значительным. Чем больше размер атома и меньше его плотность, тем меньше количество атомов в данной массе металла.
