Магний - химический элемент с атомным номером 12, относящийся к группе щелочноземельных металлов. Он представляет собой легкий, серебристо-белый металл, обладающий высокой жаропрочностью и качественными физическими свойствами. Хлор, в свою очередь, является химическим элементом с атомным номером 17, принадлежащим к галогенам. Он обладает ярко-зеленой окраской и является одним из наиболее распространенных и химически активных неметаллов.
Взаимодействие магния и хлора является одним из типичных примеров реакции между металлом и неметаллом. Когда магний и хлор вступают в контакт, происходит химическая реакция, которая разрушает структуру магния, образуя хлорид магния. Эта реакция является экзотермической, то есть сопровождается выделением тепла и света.
Хлорид магния обладает рядом уникальных свойств. Во-первых, он является белым кристаллическим веществом с высокой степенью растворимости в воде. Во-вторых, хлорид магния используется в медицине, промышленности и сельском хозяйстве. Он может использоваться как добавка в пищевых продуктах, а также в производстве бумаги, текстиля и предметов личной гигиены.
Реакция магния с хлором

Реакция магния с хлором является классическим примером реакции между металлом и неметаллом. Магний (Mg) и хлор (Cl) - это элементы химической системы, которые обладают разными физическими и химическими свойствами.
В химической реакции магния с хлором магний передает электроны хлору, образуя ион магния и ион хлора. Это ионно - ковалентная связь, где между магнием и хлором возникают ковалентные связи, а ионы находятся в ионных решетках.
Реакция происходит следующим образом: Mg + Cl2 -> MgCl2. При этом образуется соль магния и хлора - хлорид магния.
Хлорид магния (MgCl2) - это белый кристаллический порошок, который обладает высокой растворимостью в воде. Он используется в медицине, а также в промышленности для производства металлов и других химических соединений.
Реакция магния с хлором является экзотермической, то есть сопровождается выделением тепла. Она происходит при нагревании магния или при воздействии на него энергией.
Химические свойства магния

Магний - химический элемент, обладающий множеством уникальных свойств.
Магний является активным металлом, который легко вступает во взаимодействие с кислородом и образует оксид магния. Он активно реагирует с водой, образуя гидроксид магния и выделяясь в виде горючей водородной смеси.
Интересной особенностью магния является его способность к горению. Взаимодействуя с кислородом воздуха, магний горит с ярким, белым пламенем, образуя оксид. Это свойство нашло применение в различных пиротехнических устройствах и фотоэлементах.
Магний также обладает хорошей проводимостью электричества и используется для производства прочных и лёгких сплавов с другими металлами. Он входит в состав магниевых сплавов, используемых в авиационной и автомобильной промышленности.
Стоит отметить, что магний реагирует с рядом кислот, образуя соли магния. Однако он не реагирует с щелочами, поэтому не может замещать металлы в соответствующих солях.
В целом, магний характеризуется высокой химической активностью и наличием уникальных свойств, которые находят применение в различных областях науки и техники.
Химические свойства хлора
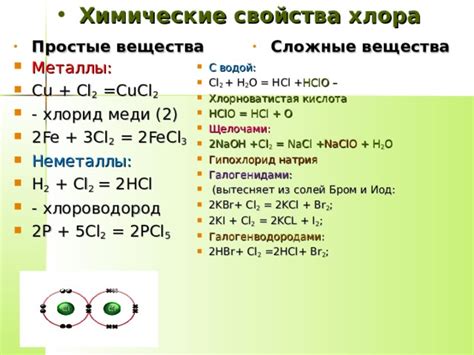
Хлор - элемент группы галогенов, обладает характерными свойствами данной группы: высокой реакционной способностью и окрашенностью в желтую зеленую оттенок. Химический символ - Cl, атомный номер - 17.
Хлор легко образует соединения с другими элементами, реагируя с большинством металлов и неметаллов. Он может образовывать как ковалентные, так и ионные связи.
Одной из наиболее известных реакций хлора является его взаимодействие с металлами, в результате которого образуется соль. Например, хлор реагирует с натрием, образуя хлорид натрия (NaCl) - наиболее распространенную соль хлора.
Хлор сильный окислитель и способен взаимодействовать с многими органическими и неорганическими веществами. Он может принимать электроны, образуя отрицательные ионы хлорида (Cl-), которые широко используются в различных процессах, включая производство пластмасс, дезинфекцию воды и снабжение питьевой водой.
Хлор имеет высокую плотность и низкую температуру плавления и кипения, что делает его важным реагентом во многих процессах, таких как производство полимеров, хлорированных органических соединений и многих других.
Области применения магния и хлора

Магний и хлор являются важными химическими элементами, которые имеют широкие области применения.
Магний является легким металлом с высокой прочностью и хорошей коррозионной стойкостью. Он находит применение в авиационной и автомобильной промышленности, где используется для производства легких и прочных сплавов. Магний также используется в производстве батарей и электроинструментов, благодаря своим хорошим электропроводным свойствам. Ещё одной областью применения магния является производство огнетушителей, благодаря его способности быстро реагировать с кислородом и гасить пламя.
Хлор является одним из самых распространенных химических элементов и используется во многих сферах. Одной из главных областей применения хлора является обработка питьевой воды. Хлор используется для дезинфекции воды и уничтожения бактерий и вирусов. Также хлор широко применяется в производстве пластика и других полимерных материалов. Его химические свойства позволяют использовать его в процессе получения ряда химических соединений, таких как галогены, пластик и многое другое.
Таким образом, магний и хлор находят применение в различных отраслях промышленности и производства, благодаря своим уникальным химическим и физическим свойствам.
Роль магния и хлора в живых организмах

Магний является одним из важнейших макроэлементов, необходимых для нормального функционирования организма. Он играет ключевую роль во многих биологических процессах. Магний участвует в регуляции работы сердца и нервной системы, улучшает функцию мышц и костей, способствует нормализации сна и настроения. Кроме того, магний входит в состав многих ферментов, участвует в обмене веществ и энергетическом обмене.
Хлор также имеет важное значение для организма. Он является одним из основных анионов внутриклеточной и межклеточной жидкости. Хлор участвует в регуляции кислотно-щелочного равновесия, обеспечивает нормальное давление в клетках, регулирует обмен электролитов и воды. Кроме того, хлор принимает участие в процессах пищеварения и выработке желудочного сока.
Оба этих элемента находятся в организме в виде ионов и активно взаимодействуют друг с другом. Магний и хлор образуют соединения, которые участвуют в многих планах обмена веществ и энергии. Они синергично влияют друг на друга, участвуя в регуляции работы различных органов и систем организма.
Вопрос-ответ

Какие особенности взаимодействия магния и хлора можно выделить?
Одной из особенностей взаимодействия магния и хлора является то, что они образуют соль – хлорид магния (MgCl2). Эта соль широко используется в различных отраслях промышленности и имеет множество применений.
Какие свойства имеет хлорид магния?
Хлорид магния обладает некоторыми интересными свойствами. Например, эта соль обладает гигроскопичностью – способностью притягивать влагу из воздуха. Также хлорид магния обладает хорошей растворимостью в воде и имеет высокую проводимость электрического тока в растворе. Кроме того, этот вещество обладает антивирусными и антибактериальными свойствами и широко применяется в медицинских целях.
