Изучение электродных потенциалов металлов – одна из основных задач в химическом анализе и электрохимии. Электродный потенциал является мерой активности металлов и позволяет предсказать их реакционную способность и возможность служить электродами в различных электрохимических процессах.
Лабораторная работа по изучению электродных потенциалов металлов позволяет оценить их влияние на химический процесс и разработать методику определения конкретного металла по его потенциалу. В ходе работы студентам предлагается измерить потенциалы различных металлов путем сравнения с исследуемыми пробами в стандартном растворе хлорида меди.
Основной прибор, используемый при проведении лабораторной работы, – вольтметр. Для измерения электродного потенциала металлов используется электродная ячейка, состоящая из исследуемого металла и эталонного электрода. Измерения проводятся при температуре 20 °C, чтобы исключить влияние изменения температуры на потенциал металла.
Электродные потенциалы металлов
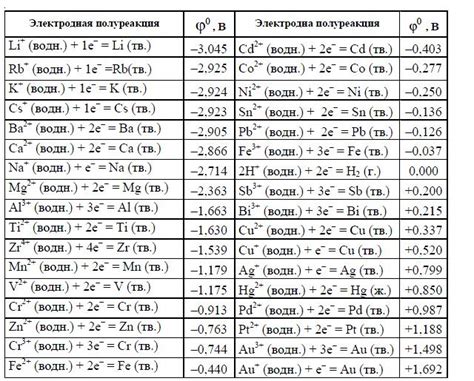
Электродные потенциалы металлов - это характеристики, связанные с их способностью участвовать в электрохимических реакциях. Они отражают способность металла переходить в ионное состояние при контакте с различными растворами.
Электродные потенциалы металлов могут быть ионного (также называемого стандартным) и абсолютного потенциалами. Ионный потенциал измеряется относительно стандартного водородного электрода, которому присваивается нулевое значение. Абсолютный потенциал является абсолютным значением электродного потенциала металла.
Значение электродного потенциала металла зависит от его химической активности. Металлы с более высокими электродными потенциалами являются более активными и склонны к окислению, тогда как металлы с более низкими электродными потенциалами более стабильны и склонны к восстановлению.
Электродные потенциалы металлов определяют их электрохимическую реакционную способность и электролитическую активность. Они играют ключевую роль в процессах гальванической коррозии, электролиза и других электрохимических реакциях.
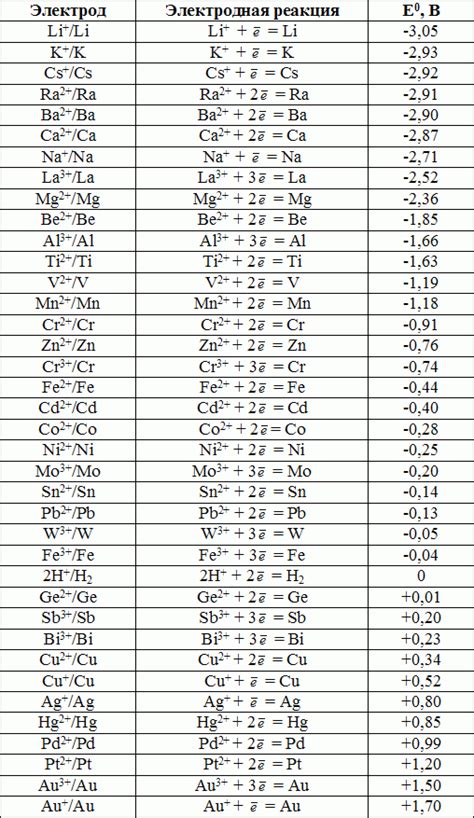
Для определения электродных потенциалов металлов проводятся специальные лабораторные исследования. Результаты этих исследований могут быть представлены в виде электродных потенциальных рядов металлов, которые помогают определить последовательность их активности в электрохимических реакциях.
Определение электродного потенциала металлов
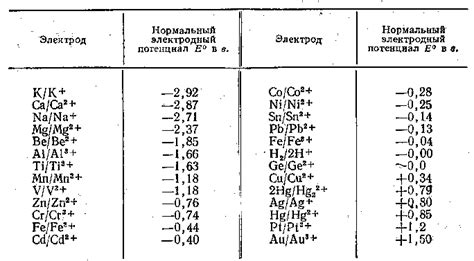
Электродный потенциал металлов - это величина, которая характеризует способность металла отдавать или принимать электроны при контакте с другими веществами или электролитами. Он измеряется в вольтах и служит для сравнения химической активности различных металлов.
Определение электродного потенциала металлов проводится с помощью электрохимических методов, таких как измерение разности потенциалов между металлом и стандартным электродом или проведение гальванических элементов.
Для определения электродного потенциала металлов используется стандартный водородный электрод (SHE) как эталонный. При этом металл помещается в раствор, контактирующий с водородным электродом, и измеряется разность потенциалов между этими двумя электродами.
Электродный потенциал металла зависит от его химической природы и зависит от окружающей среды. Для металлов с положительными потенциалами характерны высокая активность и способность легко отдавать электроны, а металлы с отрицательными потенциалами могут легко принимать электроны.
Измерение электродного потенциала металлов имеет важное практическое значение в различных областях, таких как электрохимия, материаловедение, гальваника и другие. Оно позволяет предсказывать возможность электрохимических реакций, определять коррозионную стабильность металлов и выбирать подходящие материалы для различных приложений.
Использование электродных потенциалов в лабораторной работе
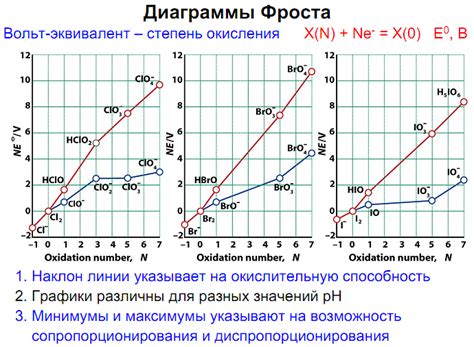
Электродные потенциалы являются важным физическим параметром, который используется в лабораторной работе для изучения и анализа свойств металлов.
В ходе лабораторной работы проводятся различные эксперименты, например, измерение потенциалов различных металлов при контакте с определенными растворами или электролитами. Эта информация позволяет определить, какие металлы имеют большую или меньшую активность, и какие из них могут быть использованы в различных электрохимических процессах.
Для проведения таких измерений часто используется референтный электрод, который имеет известный и постоянный потенциал. Он позволяет сравнивать потенциалы других металлов и определять их относительную активность.
Результаты измерений электродных потенциалов металлов могут быть представлены в виде таблицы с указанием значений потенциалов для каждого металла. Это позволяет исследователям сравнивать и анализировать свойства различных металлов и применять эти знания в различных областях, таких как электрохимия, материаловедение и строительство.
Также, электродные потенциалы металлов могут быть использованы для определения состава смесей. Путем измерения потенциалов при контакте с определенными растворами и сравнения их со значениями в таблице, можно определить присутствие или отсутствие определенного металла в смеси.
Использование электродных потенциалов в лабораторной работе предоставляет исследователям мощный инструмент для изучения и анализа свойств металлов. Он помогает определить их активность, состав смесей и применение в различных областях науки и техники.
Определение коррозионной активности металлов
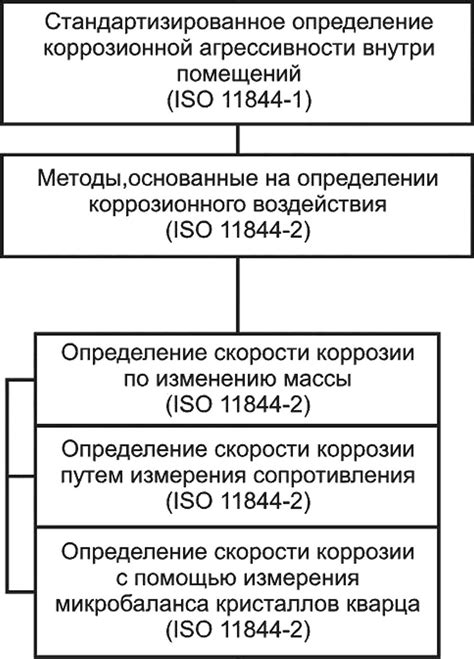
Коррозия является одной из основных проблем, связанных с эксплуатацией и сохранением металлических материалов. Коррозионная активность металлов может быть определена с помощью электродных потенциалов, которые являются основными характеристиками металлов в химических реакциях с окружающей средой.
Определение коррозионной активности металлов проводится с помощью специальных методов и приборов, таких как электроды и электрохимические ячейки. Эти приборы позволяют измерять электродный потенциал металлов и сравнивать его с электродными потенциалами других металлов. Чем выше электродный потенциал металла, тем он более активен коррозионно. Таким образом, с помощью этих измерений можно определить, какие металлы будут наиболее склонны к коррозии, а какие - менее активны.
Определение коррозионной активности металлов имеет важное практическое применение. Это позволяет выбирать наиболее подходящие материалы для различных условий эксплуатации, учитывая их коррозионную стабильность. Например, в строительных конструкциях, где металлы подвергаются воздействию агрессивных сред, таких как влага и соли, необходимо выбирать материалы с низкой коррозионной активностью. Такие материалы будут менее подвержены разрушению и продлевят срок службы конструкций.
Определение коррозионной активности металлов является неотъемлемой частью изучения и исследования коррозионных процессов. Это позволяет более глубоко понять механизмы коррозии и разработать эффективные методы ее предотвращения. Такие методы, например, включают применение покрытий и антикоррозионных покрытий, а также правильную конструкцию и эксплуатацию металлических изделий.
Значение электродных потенциалов металлов в практических приложениях
Электродные потенциалы металлов играют важную роль во многих практических приложениях, связанных с электрохимией и материаловедением. Они определяют, какой металл является анодом, а какой катодом при электрохимических процессах, таких как гальваническая коррозия и электрохимические реакции.
Значение электродных потенциалов металлов также определяет возможность использования металлов в различных конструкционных материалах. Металлы с более высокими электродными потенциалами, такими как платина и золото, обычно используются в электронике и других высокотехнологичных приложениях, где требуется высокая электропроводность и устойчивость к коррозии.
С другой стороны, металлы с более низкими электродными потенциалами, такие как железо и алюминий, часто используются в строительстве и других инженерных приложениях. Эти металлы обладают хорошей прочностью и долговечностью, что делает их подходящими для конструкционных материалов, таких как опоры линий электропередач и здания.
Электродные потенциалы металлов также учитываются при выборе материалов для контактов и электрических соединений. Когда два разных металла соприкасаются, возникает потенциал для возникновения электрохимической коррозии, называемой гальванической коррозией. Правильный выбор материалов сравнивается их электродных потенциалов, чтобы минимизировать вероятность коррозии.
В целом, электродные потенциалы металлов имеют большое значение в практических приложениях, связанных с электрохимией, материаловедением, строительством и производством. Знание этих потенциалов позволяет подобрать подходящие металлы для конкретных условий эксплуатации, обеспечивая надежность и долговечность материалов и изделий.
Вопрос-ответ

Зачем проводить лабораторную работу по электродным потенциалам металлов?
Лабораторная работа по электродным потенциалам металлов позволяет изучить свойства металлов, их способность к окислению и восстановлению, а также определить их электрохимическую активность. Этот эксперимент помогает установить порядок металлов по их электродному потенциалу, что имеет большое значение для различных электрохимических процессов и применений металлов.
Какие материалы и оборудование нужны для проведения лабораторной работы по электродным потенциалам металлов?
Для проведения лабораторной работы по электродным потенциалам металлов потребуются следующие материалы и оборудование: металлические образцы различных металлов, растворы электролитов, гальванические элементы, соединительные провода, амперметр и вольтметр. Кроме того, может понадобиться лабораторное оборудование для измерения и контроля реакций металлов.
Каким образом можно определить электродные потенциалы металлов в лабораторной работе?
Определение электродных потенциалов металлов в лабораторной работе можно провести методом гальванической серии или методом потенциостатического титрования. При использовании метода гальванической серии металлические образцы размещаются в растворах электролитов, а для измерения потенциала используется вольтметр. При методе потенциостатического титрования металлические образцы окисляются или восстанавливаются, а для контроля процесса используется амперметр. Оба метода позволяют определить электродные потенциалы металлов с высокой точностью и достоверностью.
