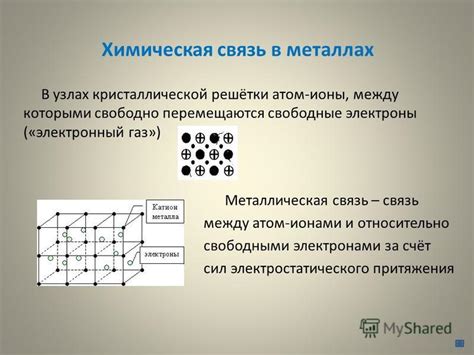
Кристаллическая структура является основной характеристикой металлов и определяет их свойства и поведение в различных условиях. Возможность образования такой структуры обусловлена особенностями взаимодействия атомов металлов и позволяет им образовывать крупные и прочные кристаллические решетки.
Одним из наиболее распространённых видов кристаллических решеток является кубическая решётка, которую образуют, например, атомы железа. Каждый атом в данной решётке окружён восемью соседними атомами, и такая структура обеспечивает металлу высокую плотность, прочность и термическую стабильность. Благодаря этому железо является одним из основных строительных материалов и широко используется в машиностроении, судостроении и других отраслях промышленности.
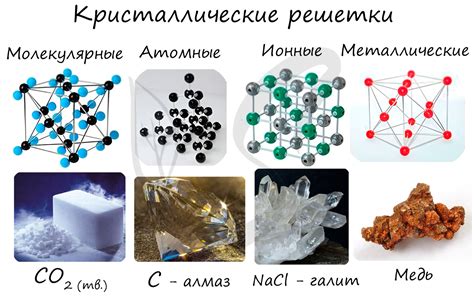
Углерод, в свою очередь, образует другую кристаллическую решётку, а именно ромбическую решётку. В данной структуре каждый атом углерода окружён четырьмя соседними атомами. Это обеспечивает высокую прочность и твёрдость углерода и позволяет использовать его в производстве алмазов и других твёрдых материалов. Кроме того, благодаря этой структуре углерод может образовывать различные аллотропные модификации и представлять собой как графит, так и алмаз. Графит обладает сложной ламинарной структурой, а алмаз является одним из самых твёрдых известных природных материалов.
Описание кристаллических решеток наиболее распространённых металлов
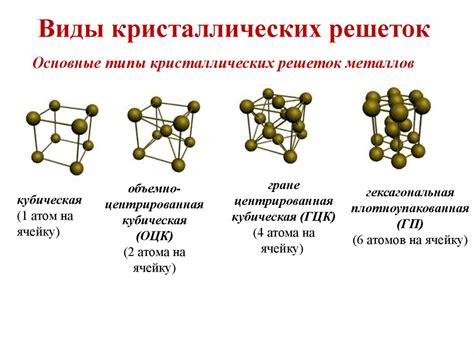
Железо является одним из наиболее распространённых металлов на Земле. В его кристаллической решетке атомы железа расположены в простейшей кубической решетке. Каждый атом имеет восемь ближайших соседей, образуя кубодиагональные центрированные грани и грани по осям координат. Такая структура придает железу его прочность и способность к магнитной поляризации.
Алюминий также имеет простую кубическую кристаллическую решетку. В этом металле атомы алюминия также образуют кубодиагональные грани и грани по осям координат. Однако, в отличие от железа, у алюминия каждый атом имеет шесть ближайших соседей.
Медь образует тетрагональную кристаллическую решетку, в которой атомы меди располагаются на каждом вершине тетраэдра. У меди каждый атом имеет по два ближайших соседа, образуя своеобразные связи, которые обеспечивают ее хорошие электропроводящие свойства.
Серебро имеет кубическую кристаллическую решетку, но в отличие от железа, атомы серебра находятся только в узлах решетки, а не на гранях. Как и у алюминия, каждый атом серебра имеет шесть ближайших соседей.
Золото также образует кубическую решетку, атомы которого располагаются в узлах решетки. Каждый атом золота имеет по два дополнительных ближайших соседа, что придает золоту его особенные свойства, такие как высокая электропроводность и химическая инертность.
Таблица ниже показывает типы кристаллических решеток для указанных металлов:
| Металл | Тип решетки |
|---|---|
| Железо | Простая кубическая |
| Алюминий | Простая кубическая |
| Медь | Тетрагональная |
| Серебро | Простая кубическая |
| Золото | Простая кубическая |
В итоге, химические и физические свойства наиболее распространённых металлов определяются их кристаллическими решетками, которые обеспечивают упорядоченное расположение атомов и специфичные связи между ними.
Изучение строения металлических кристаллических решеток
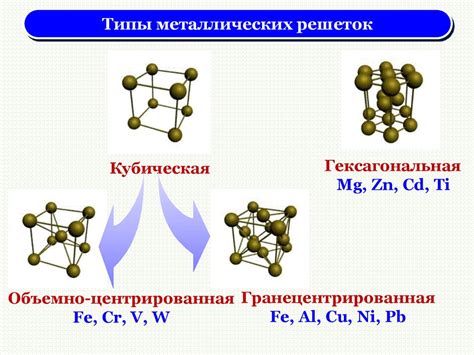
Строение металлических кристаллических решеток является одной из важных характеристик металлов, влияющих на их свойства и применение. Изучение строения решеток позволяет понять, как атомы металла организованы в пространстве и какие взаимодействия между ними происходят.
Для анализа строения металлических кристаллических решеток используются различные методы и техники. Одним из наиболее распространенных методов является рентгеноструктурный анализ, который основан на рассеянии рентгеновских лучей на атомах металла. Этот метод позволяет определить параметры решетки, а также распределение электронной плотности внутри кристалла.
При изучении строения металлических кристаллических решеток также широко применяются методы электронной микроскопии. С помощью электронного микроскопа можно визуализировать поверхность и внутреннюю структуру металла с высоким разрешением. Этот метод позволяет увидеть детали структуры решетки и обнаружить дефекты, такие как дислокации или деформации.
Изучение строения металлических кристаллических решеток имеет важное значение не только с научной, но и с практической точки зрения. Знание о строении решеток позволяет разрабатывать новые материалы с улучшенными свойствами, а также контролировать и оптимизировать процессы обработки и производства металлических изделий.
Кристаллическая решетка металла железа
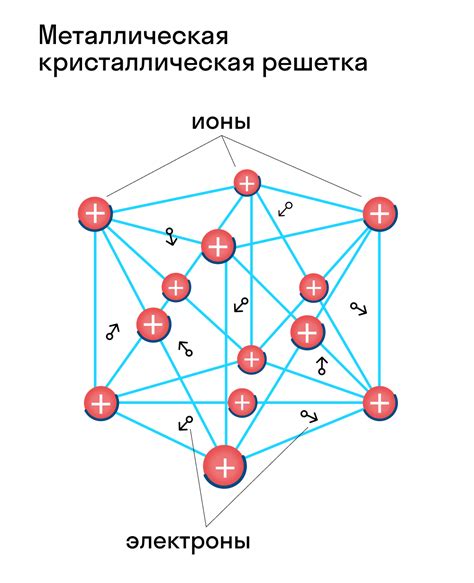
Металл железо является одним из наиболее распространенных металлов на Земле. Он имеет кристаллическую структуру, которая определяется его уникальными свойствами.
Кристаллическая решетка металла железа состоит из атомов железа, которые объединены в трехмерную структуру. В этой структуре атомы железа расположены в упорядоченном и регулярном паттерне.
У решетки металла железа есть основные элементы: кристаллографические плоскости и узлы. Кристаллографические плоскости определяются атомами железа, расположенными на определенном расстоянии друг от друга. Узлы же являются точками пересечения кристаллографических плоскостей.
В железе существует несколько различных типов кристаллических решеток, таких как кубическая решетка, гексагональная решетка и т.д. В каждом типе решетки атомы железа имеют определенное расположение и координационное число.
Кристаллическая решетка металла железа имеет важное значение в его свойствах и поведении. Она определяет такие характеристики, как прочность, упругость и пластичность металла. Поэтому изучение решетки металла железа является важной задачей в материаловедении и металлургии.
Структура кристаллической решетки меди
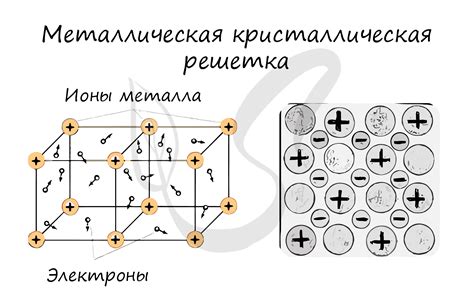
Медь – это металл, который широко используется в различных отраслях, включая электронику, строительство и производство ювелирных изделий. Его кристаллическая решетка отличается особым строением, обеспечивая меди уникальные физические и химические свойства.
Структура кристаллической решетки меди основана на гранецентрированной кубической (fcc) структуре. Каждый атом меди окружен шестью ближайшими атомами, которые расположены по углам куба. Таким образом, у меди имеется 12 ближайших соседей, а общее число атомов в кристаллической решетке равно 4.
Структура медной решетки подобна структуре решеток других металлов, таких как алюминий и свинец. Однако, из-за особенностей расположения атомов, медь обладает высокой электропроводностью и теплопроводностью. Это делает ее идеальным материалом для проводников и различных электронных устройств.
Медь также обладает особым цветом – красным или оранжевым оттенком. Это объясняется тем, что при поглощении света атомами меди происходит омеднение, и в спектре отраженного света преобладают длины волн в диапазоне красного и оранжевого цветов.
В целом, структура кристаллической решетки меди обуславливает его уникальные свойства и широкое применение в различных отраслях промышленности.
Особенности строения решетки алюминия

Алюминий - это довольно распространенный металл, который обладает рядом интересных особенностей в строении своей кристаллической решетки.
Первое, что следует отметить, это то, что алюминий образует решетку типа гексагонального ближнего упаковки (ГБУ). Такая структура образуется при упаковке атомов алюминия в решетке и определяет многие его физические свойства.
Кристаллическая решетка алюминия состоит из слоев атомов, которые расположены в плоскостях. Атомы в каждой плоскости смещены относительно соседних плоскостей. Это приводит к образованию специальной последовательности слоев в алюминии, которая называется структурой ГБУ.
Каждый слой в решетке алюминия содержит шестиугольные и пятиугольные отверстия, в которые встраиваются атомы других элементов при образовании сплавов. Это отверстия называются октавными полостями и играют важную роль в формировании свойств сплавов алюминия. Они позволяют контролировать размер и форму атомов, что влияет на твердость и механические свойства материала.
Кристаллическая решетка алюминия обладает высокой плотностью упаковки атомов. Это, в сочетании с его низкой плотностью и высокой электропроводностью, делает его идеальным материалом для использования в многих сферах, включая авиацию, строительство и производство электроники.
Химический состав и кристаллическая структура металла свинца
Свинец, химический элемент с атомным номером 82, обладает символом Pb на периодической системе химических элементов. Он принадлежит к группе элементов, известных как постсеребряные металлы, и является одним из самых широко распространенных металлов в мире. Химический состав свинца включает в себя только один изотоп, а именно Pb-208, что делает его стабильным элементом и не подверженным радиоактивному распаду.
Кристаллическая структура свинца является фцк (гранецентрированная кубическая), что означает, что атомы свинца упакованы в кубическую решетку, где каждый угол кубика образуется атомами, а каждая грань кубика также образуется атомами. В каждой координатной точке кубической решетки находится один атом свинца. Такая упаковка атомов обеспечивает свинцу характерные механические свойства, такие как пластичность и деформируемость. Кроме того, кристаллическая структура свинца обуславливает его химическую реактивность и взаимодействие с другими элементами.
Помимо своей распространенности, свинец обладает рядом уникальных свойств, которые делают его ценным материалом в различных областях. Например, свинец является отличным тепло- и электропроводником, поэтому его широко используют в производстве электроники и электротехники. Кроме того, свинец является химически стойким и устойчивым к окислению, что делает его незаменимым материалом для создания различных сплавов, включая оловосвинцовые сплавы и припои. Важно отметить, что свинец также может быть ядовитым для человека и окружающей среды, поэтому его использование требует соблюдения соответствующих мер предосторожности и контроля.
Кристаллические решетки никеля и кобальта
Никель – это металл серебристо-белого цвета, который обладает высокой стойкостью к коррозии. Кристаллическая решетка никеля является граноцентрированной кубической, с атомами никеля, занимающими угловые и центральные места в кубе. Расстояние между атомами в этой решетке составляет 0,352 нм.
Кобальт – металл серебристо-белого цвета с голубым оттенком. Кристаллическая решетка кобальта также является граноцентрированной кубической. Она состоит из атомов кобальта, занимающих угловые и центральные позиции в кубе. Расстояние между атомами в решетке кобальта составляет 0,354 нм.
Никель и кобальт принадлежат к группе платиновых металлов и обладают множеством сходных свойств. Они имеют высокую плотность, тугоплавки, хорошо проводят электричество. Кристаллические решетки никеля и кобальта обязательно учитываются при изучении их физических и химических свойств, а также при создании сплавов и материалов с предельными прочностными характеристиками.
| Свойство | Решетка никеля | Решетка кобальта |
|---|---|---|
| Тип решетки | Граноцентрированная кубическая | Граноцентрированная кубическая |
| Расстояние между атомами | 0,352 нм | 0,354 нм |
Сопоставление кристаллических решеток никеля и кобальта позволяет лучше понять структуру и особенности данных металлов, а также использовать эту информацию для прогнозирования и улучшения их свойств в различных областях промышленности и технологии.
Кристаллическая структура металла цинка
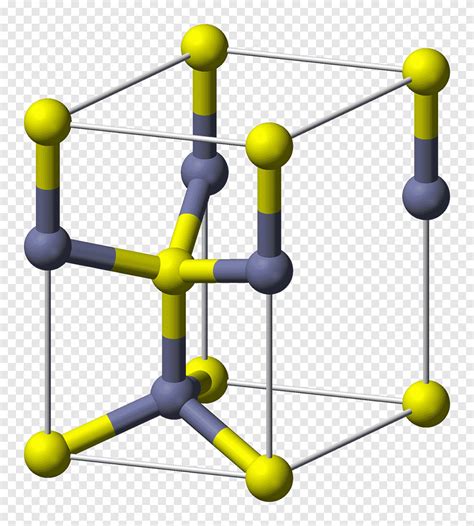
Цинк является одним из наиболее распространенных металлов и обладает своеобразной кристаллической структурой. Типичная решетка цинка относится к гексагонально-ближайшей упаковке (hcp).
В кристаллической структуре цинка каждый атом соединен с шестью ближайшими атомами, а основная часть атомов находится в плоскости, образующей гексагон. Такая структура обусловлена особенностями орбитального распределения электронов и формирует устойчивую кристаллическую решетку.
Цинк является мягким и пластичным металлом, что также связано с его кристаллической структурой. В результате движения атомов в решетке цинка металл проявляет высокую деформационную способность и способность к образованию так называемых дефектов кристаллической решетки.
Кристаллическая структура цинка обуславливает его множественные свойства и применение. Цинк используется в производстве сплавов, гальваническом покрытии, производстве аккумуляторных батарей и других изделий. Благодаря своей кристаллической структуре цинк обладает высокой электропроводностью и прочностью, что делает его незаменимым материалом в разнообразных отраслях промышленности.
Строение и особенности кристаллической решетки серебра

Строение решетки:
Серебро - блестящий белый металл, который образует кубическую решетку типа простой гранцентрированной кубической (ccf). Такая решетка характеризуется тем, что атомы серебра располагаются на углах куба и в центре каждой грани.
Особенности решетки серебра:
Серебро обладает интересными особенностями в своей кристаллической решетке. Во-первых, оно обладает высокой плотностью упаковки атомов, что обуславливает его отличные физические и механические свойства. Во-вторых, межатомные расстояния в решетке серебра очень малы, что увеличивает его прочность и твердость. Помимо этого, серебро также обладает высокой электропроводностью и теплопроводностью, что делает его ценным материалом для использования в различных отраслях промышленности.
Описание кристаллической решетки:
Кристаллическая решетка серебра представляет собой трехмерную сетку атомов, в которой атомы серебра расположены на углах кубических ячеек и в центре каждой грани. Такая упаковка атомов обеспечивает максимальную плотность упаковки и прочность материала. Межатомные расстояния в решетке серебра составляют около 2.89 ångstroms, что делает его одним из самых плотных и прочных металлов.
Заключение:
Кристаллическая решетка серебра имеет специфическую структуру, которая обеспечивает его высокую прочность, твердость, электропроводность и теплопроводность. Серебро используется в различных отраслях промышленности, таких как электроника, ювелирное дело и медицина, благодаря своим уникальным свойствам и кристаллической решетке.
Вопрос-ответ

Какие металлы имеют кристаллическую решетку?
Кристаллическая решетка встречается у большинства металлов, включая железо, медь, алюминий, свинец, золото и другие.
Каковы особенности кристаллической решетки у железа?
Кристаллическая решетка железа имеет простую кубическую структуру, где каждый атом железа окружен 8 ближайшими соседями. Это делает железо прочным и податливым металлом.
