Щелочные металлы являются одной из основных групп элементов периодической системы химических элементов. К ним относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Одной из важных характеристик щелочных металлов является их способность образовывать кристаллические решетки. Кристаллическая решетка - это упорядоченная структура атомов, которая образуется при кристаллизации вещества.
Структура кристаллической решетки щелочных металлов имеет свои особенности. Она основана на принципе, известном как плотная упаковка, который описывает наиболее эффективное расположение атомов в кристаллической решетке. В случае щелочных металлов, атомы образуют простую кубическую решетку с гранцентрированным остатком. Это означает, что каждый атом окружен в области своего положения шестью соседними атомами, а также имеет дополнительные атомы в центрах граней решетки.
Такая структурная особенность у щелочных металлов обусловлена их химическими свойствами. Внешний электронный слой щелочных металлов содержит один электрон, что делает их химически активными. В процессе кристаллизации, атомы щелочных металлов стремятся установить наиболее энергетически выгодное положение, образуя структуру с минимальной энергией.
Структура кристаллической решетки щелочных металлов:
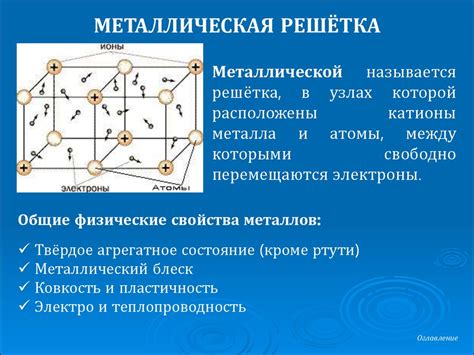
Щелочные металлы являются группой элементов периодической системы, характеризующихся особым типом кристаллической решетки. В их структуре присутствуют некоторые особенности, которые делают их уникальными среди других элементов.
Основными представителями щелочных металлов являются литий, натрий, калий, рубидий, цезий и франций. Они обладают одинаковой кристаллической структурой, которая называется кубической гранецентрированной. В этой структуре каждый атом металла окружен восьмью атомами других металлов, образуя кубическую ячейку.
Кристаллическая решетка щелочных металлов обладает высокой плотностью и пространственной плотностью. Она также обладает высокой упругостью и пластичностью, что позволяет этим металлам быть гибкими и легкообрабатываемыми.
Кубическая гранецентрированная структура дает щелочным металлам множество полезных свойств. Например, они обладают высокой электропроводностью, что делает их востребованными материалами для применения в электронике. Они также обладают высокой химической активностью и способностью к образованию сплавов.
Кристаллическая структура щелочных металлов также имеет важное значение для понимания их физических и химических свойств. Изучение этой структуры позволяет лучше понять атомное взаимодействие и связи в металлах, что может быть полезно для разработки новых материалов и технологий.
Особенности структуры

Структура кристаллической решетки щелочных металлов обладает рядом особенностей, которые определяют их уникальные свойства. В основе структуры лежит кубическая решетка со стороной, равной параметру кристаллической ячейки. Эта решетка образована атомами металла, которые связаны друг с другом ковалентной или ионной связью.
Одной из особенностей структуры щелочных металлов является наличие простейшей кубической решетки, где каждый атом окружен восемью соседними атомами. Это обуславливает их хорошую деформационную способность, а также высокую пластичность и проводимость электричества и тепла.
Кроме того, структура щелочных металлов обладает высокой степенью упорядоченности. Атомы располагаются в решетке с определенным порядком, что позволяет им образовывать компактные структуры и обладать высокой плотностью.
Структура щелочных металлов также характеризуется наличием свободных электронов, что обуславливает их высокую электропроводность. Эти свободные электроны отвечают за подвижность зарядов и являются основой для различных физических и химических свойств этих металлов.
Свойства кристаллической решетки
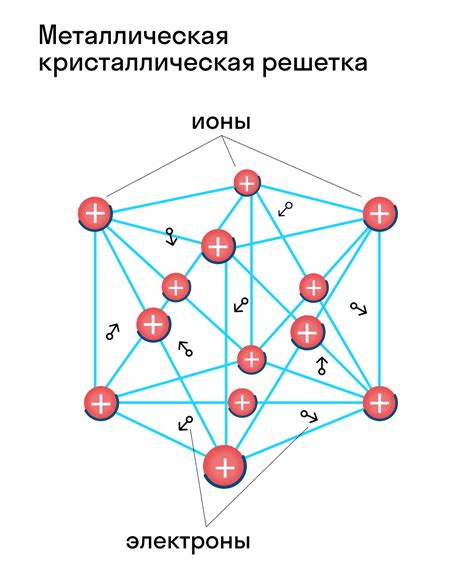
Кристаллическая решетка щелочных металлов обладает рядом уникальных свойств, которые делают их важными и широко применяемыми материалами в различных областях науки и техники.
Одним из важных свойств кристаллической решетки щелочных металлов является ее высокая структурная упорядоченность. В кристаллической решетке атомы щелочных металлов располагаются в регулярном и повторяющемся порядке, образуя кристаллы с определенными формами и размерами. Это свойство позволяет щелочным металлам обладать высокой механической прочностью, жесткостью и стабильностью.
Кристаллическая решетка также обладает хорошей электрической проводимостью. Атомы щелочных металлов имеют свободные электроны в валентной зоне, которые легко могут передвигаться по кристаллической решетке и создавать электрический ток. Это свойство делает щелочные металлы хорошими проводниками электричества и основой для создания электрических контактов и проводов.
Другим важным свойством кристаллической решетки щелочных металлов является их способность к легкому формированию и распространению дефектов. Решетка может содержать в себе вакансии, дислокации, межзерристый кислород, сегрегацию зерна или предела зерна. Это позволяет щелочным металлам обладать высокой пластичностью, что особенно важно для процессов обработки и формирования материалов.
Также кристаллическая решетка щелочных металлов обладает высокой теплопроводностью и термостойкостью. Кристаллическая структура обеспечивает эффективную передачу тепла от одной части материала к другой, что позволяет использовать щелочные металлы в различных тепловых устройствах и высокотемпературных процессах.
Вопрос-ответ

Какова структура кристаллической решетки щелочных металлов?
Кристаллическая решетка щелочных металлов обычно имеет гранецентрированную кубическую структуру.
Какие особенности имеет структура кристаллической решетки щелочных металлов?
Особенностью структуры кристаллической решетки щелочных металлов является их регулярное расположение атомов, образующих кубическую сетку, а также наличие интерстициальных положений, занимаемых атомами других элементов.
Какие свойства проявляет структура кристаллической решетки щелочных металлов?
Структура кристаллической решетки щелочных металлов обуславливает их высокую пластичность, низкую твёрдость и хорошую электропроводность. Она также влияет на их магнитные и оптические свойства.
Почему кристаллическая решетка щелочных металлов имеет кубическую структуру?
Кристаллическая решетка щелочных металлов имеет кубическую структуру из-за особенностей их химического строения. Атомы щелочных металлов имеют одну валентную электронную оболочку, что приводит к кубической симметрии их кристаллической решетки.
Каким образом структура кристаллической решетки щелочных металлов влияет на их химические свойства?
Структура кристаллической решетки щелочных металлов влияет на их химические свойства, определяя способность реагировать с другими веществами и образовывать ионы. Благодаря структуре решетки, щелочные металлы обладают сильной металлической связью и малой энергией ионизации.
