Ковалентная полярная связь представляет собой особый тип химической связи, который возникает между атомами металлов. Подобная связь является результатом взаимодействия между одноположительно заряженными ядрами металлических атомов и электронами других атомов. В результате образуется устойчивая молекула металла, в которой частично растворяются атомы другого металла.
Одной из особенностей ковалентной полярной связи между металлами является перенос электронов между атомами. Это приводит к возникновению полярного характера связи, поскольку один атом становится более отрицательно заряженным, а другой - более положительно. Таким образом, связь между металлами может быть названа полярной, поскольку существует разделение заряда.
Ковалентная полярная связь между металлами обладает рядом уникальных свойств. Она обеспечивает прочность и стабильность молекулы металла, а также определяет ее физические и химические свойства. Кроме того, полярность связи значительно влияет на электронные свойства металла, такие как проводимость электричества и теплоотдача. Благодаря этим особенностям, ковалентная полярная связь между металлами имеет широкое применение в различных областях, включая промышленность и научные исследования.
Ковалентная полярная связь
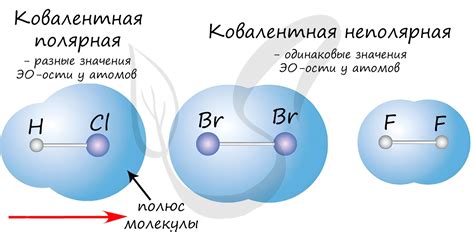
Ковалентная полярная связь — это химическая связь, которая возникает между атомами, когда они разделяют одну или несколько пар электронов. В отличие от ковалентной неполярной связи, в ковалентной полярной связи электроны не распределяются равномерно между атомами, а смещаются в сторону одного из атомов, создавая разницу в электронной плотности.
Полярность ковалентной связи определяется разницей в электроотрицательности атомов, образующих связь. Атом с большей электроотрицательностью удерживает электроны ближе к себе и приобретает небольшой отрицательный заряд, а атом с меньшей электроотрицательностью становится частично положительно заряженным.
Примером ковалентной полярной связи является связь между атомами водорода и кислорода в молекуле воды. В этом случае кислород, обладающий большей электроотрицательностью, притягивает электроны к себе, приобретая отрицательный заряд, тогда как водород становится положительно заряженным.
Важной особенностью ковалентной полярной связи является наличие диполя — разделенного на две части заряда. Внешним образом это проявляется в возможности ковалентно связанного атома влиять на близлежащие молекулы или ионы с помощью полюсов диполя.
Ковалентная полярная связь встречается во многих органических и неорганических соединениях. Она играет важную роль в определении структуры и свойств вещества, а также в реакционной активности молекул и их взаимодействии с окружающей средой.
Особенности связи

Ковалентная полярная связь между металлами обладает рядом особенностей, которые отличают ее от других видов связей.
- Одной из особенностей ковалентной полярной связи является совместное использование электронов металлами. В этом случае электроны образуют общую область, где они движутся вместе. Это позволяет металлам обладать характерными свойствами, такими как хорошая проводимость электричества и тепла.
- Ковалентная полярная связь также характеризуется положительным зарядом ядра металла и отрицательным зарядом электронов. Это создает силу притяжения между атомами и делает связь более прочной и стабильной.
- Кроме того, ковалентная полярная связь обладает направленностью. Это означает, что электроны движутся в определенном направлении вокруг ядра металла, что определяет форму и структуру кристаллической решетки металла.
Важно отметить, что связь между металлами может быть как сильной, так и слабой, в зависимости от ряда факторов, таких как радиус атомов металлов, зарядовые состояния и наличие примесей.
Таким образом, ковалентная полярная связь между металлами имеет свои специфические особенности, которые делают ее уникальной и важной для понимания свойств и поведения металлических материалов.
Примеры связи между металлами

Ковалентная полярная связь между металлами может проявляться в различных соединениях. Одним из примеров такой связи является образование салицидов. Салицид – это соединение металла с серой или галогенами. Например, натрий вступает в ковалентную полярную связь с серой и образует натрийсалицид (Na2S).
Еще одним примером связи между металлами является образование гидридов. Гидрид – это соединение водорода с металлом. Например, железо может образовывать железный гидрид (FeH2), в котором водород вступает в ковалентную полярную связь с железом.
Также ковалентная полярная связь может проявляться в образовании интерметаллических соединений. Это соединения, в которых металлы вступают в ковалентную полярную связь друг с другом. Например, цирконий и никель могут образовывать соединение ZrNi, в котором эти элементы вступают в ковалентную полярную связь.
Ковалентная полярная связь между металлами также проявляется в бинарных соединениях, содержащих два различных металла. Например, медь и цинк могут образовывать бинарное соединение CuZn, в котором медь и цинк вступают в ковалентную полярную связь.
Вопрос-ответ

Каковы особенности ковалентной полярной связи между металлами?
Ковалентная полярная связь между металлами имеет несколько особенностей. Во-первых, она образуется между атомами различных элементов, одним из которых является металл. Во-вторых, она характеризуется неравномерным распределением электронной плотности между атомами, что приводит к образованию полярной связи. Это означает, что один атом притягивает электроны сильнее, чем другой. В-третьих, ковалентная полярная связь между металлами обладает дипольными свойствами, то есть она создает разделение зарядов в молекуле. Все эти особенности влияют на свойства и химическую активность веществ, образованных такой связью.
Какие элементы могут образовывать ковалентную полярную связь с металлами?
Ковалентная полярная связь между металлами может образовываться с различными элементами. Например, металлы могут образовывать такую связь с неметаллами, такими как кислород, азот, сера и другими. Такие соединения могут иметь разнообразные свойства и применения в различных областях науки и промышленности.
Какова роль ковалентной полярной связи между металлами в химических реакциях?
Ковалентная полярная связь между металлами играет важную роль в химических реакциях. Она обеспечивает прочность соединений, образованных между металлами и неметаллами, что позволяет им образовывать стабильные химические соединения. Кроме того, эта связь влияет на реакционную способность веществ и может определять их активность в реакциях с другими веществами. Например, связь между металлом и неметаллом может влиять на скорость реакции, образуемые продукты и их свойства.
Каковы применения ковалентной полярной связи между металлами в промышленности?
Ковалентная полярная связь между металлами находит применение в различных областях промышленности. Например, такие связи используются при производстве специальных сплавов с заданными свойствами, таких как прочность, устойчивость к коррозии и теплоте, проводимость электричества и многие другие. Эти сплавы применяются в авиационной и космической промышленности, электронике, металлообработке и других сферах производства.
