Коррозия металлов – это процесс физико-химического взаимодействия металла с окружающей средой, приводящий к разрушению материала и ухудшению его функциональных свойств. Одним из наиболее распространенных видов коррозии является электрохимическая коррозия, основанная на потенциальной разнице между различными металлами или их поверхностями.
При наличии в окружающей среде влаги или веществ, способных производить электролитическое растворение, металл подвергается окислительно-восстановительным процессам, приводящим к коррозии. Результатом этих процессов является образование оксидов и солей металла, которые накапливаются на поверхности.
Коррозия металлов может быть вызвана различными факторами, такими как контакт с агрессивными веществами, повышенная влажность или температура, механические повреждения или дефекты покрытия. Для предотвращения коррозии металлов используются различные методы, такие как нанесение защитных покрытий, использование специальных сплавов или добавок и контроль окружающей среды.
Однако, несмотря на применение защитных мер, коррозия металлов остается актуальной проблемой, требующей постоянного улучшения технологий и разработки новых методов предотвращения.
Коррозия металлов имеет серьезные экономические последствия, так как приводит к уменьшению срока службы и прочности конструкций из металла, а также увеличивает затраты на их ремонт или замену. Поэтому, изучение и понимание процессов коррозии являются важными задачами для научных и инженерных исследований.
Влияние окружающей среды на коррозию

Коррозия – это физико-химический процесс разрушения металлических материалов под воздействием окружающей среды. Окружающая среда имеет огромное влияние на скорость и механизм коррозии.
Одной из основных причин коррозии является взаимодействие металлов с воздухом. В основном кислород, содержащийся в воздухе, вызывает окисление металлов, что приводит к образованию коррозионных продуктов.
Кроме воздуха, вода также является одним из главных факторов, способствующих коррозии. Влажность воздуха и воды сыграет важную роль в ускорении процесса коррозии металлов. Особенно вредны капли дождя и конденсат, которые содержат различные летучие соединения и загрязнения, которые способствуют росту коррозии.
Кроме атмосферных условий, на коррозию металлов могут влиять и химически активные вещества, такие как кислоты, щелочи и соли. Воздействие этих веществ на поверхность металла может вызывать различные физико-химические реакции, приводящие к коррозии.
При выборе материалов для различных конструкций или изделий необходимо учитывать условия эксплуатации и окружающую среду. Таким образом, защита от коррозии должна быть рассмотрена на самом начальном этапе проектирования и изготовления, чтобы максимально продлить срок службы металлических изделий.
Роль влаги в процессе коррозии
Влага играет ключевую роль в процессе коррозии металлов. Коррозия - это нежелательное физико-химическое взаимодействие металла с окружающей средой, обусловленное проникновением влаги. Вода является необходимым фактором для возникновения и протекания коррозии.
Влага способствует активации электрохимического процесса коррозии. Вода содержит растворенные в ней соли и газы, которые усиливают воздействие на металл. Когда вода попадает на поверхность металла, происходит образование электролитической среды. Наличие влаги приводит к ее положительному или отрицательному заряду, а также к образованию микрогальванических электрических элементов.
Вода также служит медиумом для распространения электролитов, что увеличивает скорость коррозии металла. Влага воздействует на поверхность металла, вызывая окисление и разрушение его структуры. Она способствует образованию оксидов, гидроксидов и других соединений, которые приводят к образованию коррозионного покрытия на металлической поверхности.
Кроме того, влага увеличивает активность агрессивных веществ, таких как кислоты или соли, которые могут проникать через покрытие на поверхность металла. Вода также способствует растворению и растворению продуктов коррозии, что может привести к дальнейшему повреждению металла.
Влияние кислорода на коррозию
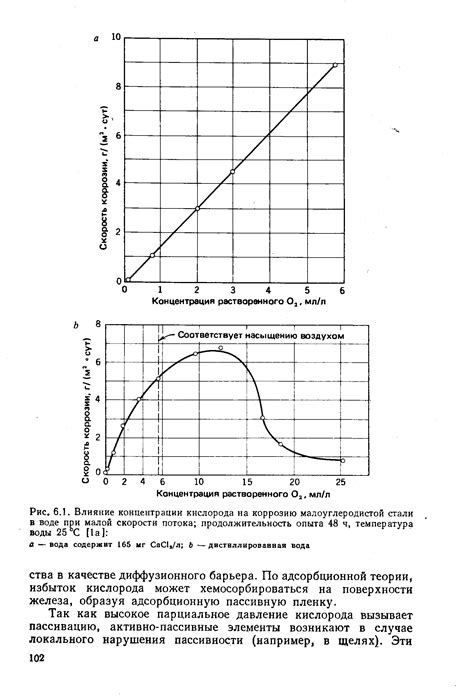
Кислород является одним из основных факторов, влияющих на процесс коррозии металлов. Он реагирует с поверхностью металла, образуя оксидные пленки, которые могут оказывать как положительное, так и отрицательное воздействие на металлическую поверхность.
С одной стороны, образование оксидных пленок может служить защитной функцией и предотвращать проникновение агрессивных сред внутрь металла. Это связано с тем, что оксидные пленки обладают барьерными свойствами и формируются на поверхности металла в результате взаимодействия с кислородом из воздуха.
Однако, с другой стороны, некоторые оксидные пленки могут быть пористыми и не предоставлять должной защиты металла от коррозии. Это особенно характерно для некоторых металлов, например, алюминия и нержавеющей стали. Пористые оксидные пленки могут способствовать коррозии металла, так как они создают условия для проникновения агрессивных сред внутрь металлической структуры.
Также кислород может способствовать развитию электрохимических реакций на поверхности металла, что также может приводить к его коррозии. Один из примеров - окисление железа, при котором на поверхности металла образуется ржавчина. Это явление часто наблюдается на металлических изделиях, которые находятся под влиянием воды и влаги, так как кислород растворен в воде и способен образовывать различные оксиды металлов.
Таким образом, важно учитывать влияние кислорода при рассмотрении процесса коррозии, так как он может как защищать, так и способствовать повышению скорости коррозионных процессов.
Механизм процесса коррозии

Коррозия металлов является процессом физико-химического взаимодействия металла с окружающей средой, в результате которого происходит разрушение и изменение свойств поверхности металла. Механизмы коррозии могут быть различными, но все они объединяются общими факторами, такими как наличие электролита, присутствие кислорода и наличие электрохимических потенциалов.
Одним из наиболее распространенных механизмов коррозии является электрохимическая коррозия, которая основана на разности потенциалов между анодом и катодом. В случае металла, анодом является место, где происходит окисление металла, а катодом - место, где происходит восстановление металла. Электролит, который окружает металл, действует в качестве проводника для перемещения электронов между анодом и катодом.
Другим механизмом коррозии является химическая коррозия, которая связана с прямыми химическими реакциями между металлом и веществом окружающей среды. Химическая коррозия может происходить как при наличии электролита, так и без него. Например, воздействие кислот или щелочей может вызывать быстрое разрушение металла без участия электролита.
Одно из самых известных проявлений коррозии металлов - ржавчина. Ржавчина – это окисление железа под воздействием кислорода. Когда металл подвергается коррозии, он может терять свою прочность и становиться менее устойчивым к механическим нагрузкам. Поэтому, предотвращение коррозии является важной задачей в различных отраслях промышленности и строительства.
Электрохимический характер коррозии

Коррозия металлов представляет собой электрохимический процесс, основанный на взаимодействии металла с окружающей его средой. Электрохимический характер этого процесса обусловлен тем, что металл является электрохимическим элементом и коррозия протекает в результате внутренних электрохимических реакций.
При взаимодействии металла с окружающей средой образуется электрическая двухфазовая среда, где металл выступает в качестве одной из фаз. На металле образуется анод и катод, между которыми происходит электронный перенос. Анод является местом, где протекает окислительно-восстановительная реакция, сопровождающаяся потерей электронов металлом в окружающую среду. Катод, в свою очередь, является местом, где происходит редокс-процесс, сопровождающийся приемом электронов от окружающей среды.
Электрохимический характер коррозии позволяет нам рассмотреть этот процесс с точки зрения электрохимических реакций. В результате окислительно-восстановительных процессов на аноде происходит растворение металла и образование ионов металла. Эти ионы могут реагировать с компонентами окружающей среды и образовывать нерастворимые соединения, что способствует образованию коррозионных отложений и повышению скорости коррозии.
Таким образом, электрохимический характер коррозии определяет причину разрушения металла и позволяет нам разрабатывать методы защиты от коррозии на основе применения различных электрохимических принципов. Например, катодная защита основана на создании условий для прохождения электронов на катоде, что позволяет предотвратить протекание электрохимической реакции коррозии. Также электрохимические методы могут применяться для активизации защитного слоя на поверхности металла и предотвращения коррозионных процессов.
Реакции окисления и восстановления в процессе коррозии
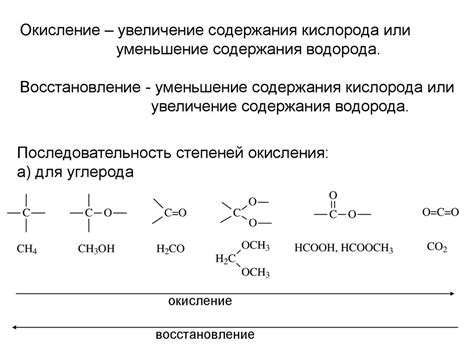
Коррозия металлов — это процесс физико-химического взаимодействия металла с окружающей средой, который приводит к повреждению его структуры и свойств. Одним из основных механизмов коррозии являются реакции окисления и восстановления.
Реакции окисления представляют собой процессы, в результате которых металл отдает электроны, образуя положительные ионы, а окислитель получает электроны и приобретает отрицательный заряд. В окружающей среде может присутствовать вода, кислоты, основания и другие вещества, которые могут выступать в роли окислителей.
Реакции восстановления, напротив, происходят при передаче электронов от окислителя к металлу. Металл принимает электроны, становится отрицательно заряженным, а вещество, служащее в данном случае восстановителем, образует положительные ионы.
В процессе коррозии реакции окисления и восстановления играют важную роль, определяя скорость и механизм протекания процесса. К примеру, при контакте металла с кислородом из воздуха происходит окисление металла, а затем восстановление на поверхности металла, что приводит к образованию окисной пленки.
Окисная пленка, в свою очередь, является защитным слоем, который предотвращает дальнейшую коррозию металла. Однако, в некоторых условиях окисная пленка может быть разрушена, что приводит к возобновлению реакций окисления и восстановления и продолжению коррозионного процесса.
Предотвращение коррозии

Коррозия металлов – это процесс физико-химического взаимодействия между металлом и окружающей средой, в результате которого происходит разрушение материала. Для предотвращения коррозии применяются различные методы и технологии.
Одним из основных методов предотвращения коррозии является использование защитных покрытий на металлических поверхностях. Такие покрытия могут быть нанесены с помощью покраски, нанесения защитных пленок или гальванического покрытия. Они создают барьер между металлом и агрессивной средой, предотвращая контакт и взаимодействие.
Другим методом предотвращения коррозии является использование специальных антикоррозионных добавок в металлических материалах. Эти добавки нейтрализуют действие агрессивных элементов в окружающей среде, что позволяет увеличить срок службы металла и защитить его от коррозии.
Важным аспектом предотвращения коррозии является также проведение регулярного технического обслуживания и контроля состояния металлических конструкций. Это позволяет выявить возможные повреждения или дефекты в ранние стадии и принять меры по их устранению.
Кроме того, при проектировании металлических конструкций можно применять специальные методы и конструктивные решения, направленные на предотвращение коррозии. Например, использование инертных материалов, обработка поверхностей или создание системы защитных слоев.
В целом, предотвращение коррозии металлов требует комплексного подхода, включающего применение защитных покрытий, антикоррозионных добавок, регулярное обслуживание и использование специальных методов проектирования. Такой подход позволяет сохранить долговечность и надежность металлических конструкций в условиях воздействия агрессивной окружающей среды.
Использование защитных покрытий

Коррозия металлов является серьезной проблемой, которая может привести к разрушению материала и снижению его прочности. Для защиты металлических поверхностей от коррозии применяются различные методы, включая использование защитных покрытий.
Защитные покрытия представляют собой специальные слои материала, которые наносятся на металлическую поверхность. Они обладают высокой стойкостью к агрессивным средам и создают барьер между металлом и окружающей средой, предотвращая проникновение влаги, кислорода и других веществ, способных вызвать коррозию.
Существует множество различных типов защитных покрытий, включая органические и неорганические. Органические покрытия, такие как лаки или краски, используются для создания защитного слоя на металлической поверхности. Они обладают хорошими адгезионными свойствами и обеспечивают эстетически привлекательный внешний вид. Неорганические покрытия, например, антикоррозионные покрытия на основе цинка или хрома, обладают более высокой стойкостью к агрессивным средам и являются более долговечными.
Выбор защитного покрытия зависит от многих факторов, включая условия эксплуатации, тип металла и требования к внешнему виду. При выборе покрытия необходимо учитывать его стойкость к агрессивным средам, способ нанесения, стоимость и эффективность защиты.
Использование защитных покрытий является важным способом предотвращения коррозии металлов. Правильно нанесенное покрытие может значительно увеличить срок службы металлической конструкции и снизить затраты на ее обслуживание и ремонт. Поэтому при работе с металлами рекомендуется обратить внимание на выбор и использование подходящего защитного покрытия.
Вопрос-ответ

Что такое коррозия металлов?
Коррозия металлов - это процесс физико-химического взаимодействия металла с окружающей средой, при котором происходят разрушение и разложение металлической структуры под воздействием различных факторов, таких как влага, кислород, соли и другие агрессивные вещества.
Какие факторы влияют на коррозию металлов?
Факторы, влияющие на коррозию металлов, включают в себя влагу, кислород, соли, кислоты, щелочи, температуру, электрический ток и другие агрессивные среды. Кроме того, механическое воздействие, такое как трение и удары, также может способствовать процессу коррозии.
Какие методы можно использовать для защиты от коррозии металлов?
Существует несколько методов защиты от коррозии металлов. Один из них - нанесение защитных покрытий на поверхность металла, таких как краска, лак, эмаль или пленка. Другой метод - использование анодной защиты или катодной защиты, при которой создается электрический ток, который способствует сохранению металла от коррозии. Также можно применять специальные антикоррозийные покрытия и добавки в материалы, которые помогают защитить металл от коррозии.
