Коррозия металла является одной из основных проблем в инженерии и строительстве. Это процесс разрушения металлических материалов под воздействием окружающей среды. Процесс коррозии основан на электрохимических реакциях, вызываемых различными факторами, такими как влага, кислоты, соли и другие агрессивные вещества.
Главной причиной коррозии является окисление металла, которое происходит при взаимодействии его с кислородом воздуха или другими окружающими средами. В результате окисления металла возникают оксиды и гидроксиды, которые образуют защитную пленку на поверхности металла. Однако, если данная пленка повреждается или разрушается, то металл становится уязвимым к дальнейшей коррозии.
Механизм электрохимического процесса коррозии включает в себя несколько стадий. Первой стадией является анодное растворение металла, где происходит электронный перенос с металлической поверхности на окружающую среду. Второй стадией является катодная реакция, где происходит потребление электронов окислителями на окружающей поверхности металла. Для осуществления этих реакций требуется наличие электролита, который обеспечивает перемещение зарядов.
Коррозия металла представляет серьезную проблему, так как она вызывает значительные экономические и экологические потери. Исследование причин и механизмов электрохимического процесса коррозии является важным для разработки методов защиты металлических конструкций и повышения их стойкости к окислению.
Причины коррозии металла
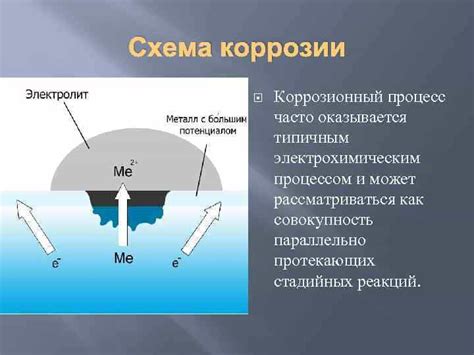
1. Воздействие окружающей среды
Коррозия металла может происходить под влиянием различных факторов окружающей среды, таких как влажность, кислотность или щелочность. Особенно активно происходит процесс коррозии в присутствии агрессивных веществ, таких как соли, воздушные кислоты, хлор, сероводород и другие химические соединения.
2. Электролитические процессы
Одной из основных причин коррозии металла являются электролитические процессы. Металл, находясь в контакте с другим металлом или электролитом, может стать анодом или катодом в электрохимической реакции. Это приводит к возникновению разности потенциалов и потоку электронов, что активирует процесс коррозии.
3. Механическое воздействие
Механические напряжения, вызванные деформацией металлической структуры, могут также способствовать коррозии. Недостаточная прочность материала или наличие дефектов в структуре, например, трещин или микропор, может привести к образованию коррозионных очагов.
4. Гальваническая коррозия
Гальваническая коррозия возникает при контакте двух различных металлов в присутствии электролита. В этом случае металл с более низким электрохимическим потенциалом (анод) подвергается растрескиванию и растворению, в то время как металл с более высоким потенциалом (катод) остается нетронутым.
5. Температура
Высокая температура часто ускоряет процесс коррозии металла. Повышенная тепловая энергия способствует активации электрохимических реакций и увеличивает скорость коррозии. Кроме того, термические циклы нагрева и охлаждения могут вызывать механическое напряжение, способствующее коррозии.
6. Другие факторы
Возможны также другие причины коррозии металла, такие как применение некачественного покрытия или защитных материалов, предварительное механическое повреждение поверхности металла, неправильное применение или обработка материала, а также различные химические реакции, побочные эффекты и т.д.
Электрохимический процесс
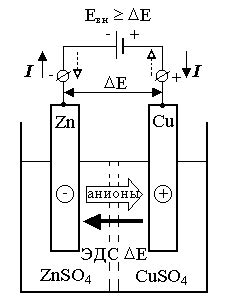
Электрохимический процесс - это процесс превращения химической энергии в электрическую энергию и наоборот. В контексте коррозии металла, электрохимический процесс играет важную роль, так как является основным механизмом разрушения материала под воздействием окружающей среды.
Электрохимическая коррозия металла основана на реакциях окисления и восстановления, которые происходят на поверхности металла. Это электрохимический процесс, в котором происходит передача электронов от анода к катоду через электролит, образованный окружающей средой и поверхностью металла.
В процессе коррозии, на поверхности металла образуется анодные и катодные области. В анодной области происходит окисление металла, в результате которого образуются ионы металла и электроны. Ионы металла растворяются в электролите и переносятся в катодную область. Вместе с ионами металла, электроны также перемещаются в катодную область через внешнюю цепь.
На катоде происходит восстановление металла, то есть восстановление ионов металла до нейтрального состояния. Этот процесс сопровождается отрицательным зарядом, поэтому ионы металла и электроны снова сливаются, образуя металлический металл и способствуя его сохранению.
Таким образом, электрохимический процесс коррозии металла является переносом ионов металла от анода к катоду через электролит, а также окислительно-восстановительными реакциями на поверхности металла. В результате этого процесса происходит разрушение металла и образование коррозионных продуктов, которые могут негативно повлиять на работу и долговечность металлических конструкций и изделий.
Механизмы коррозии металла

Коррозия металла является сложным электрохимическим процессом, который происходит при взаимодействии металла с окружающей средой. Основные механизмы коррозии включают наличие анодов и катодов на поверхности металла, а также протекание электронных и ионных переносов.
При коррозии металла на его поверхности образуются анодные и катодные участки. В качестве анодов выступают области металла, где происходит окисление и потеря электронов. Катодами служат области, где происходит восстановление и приток электронов. Коррозия возникает из-за разности потенциалов между анодными и катодными участками, что приводит к тому, что металл восстанавливается в одних областях и окисляется в других.
Однако механизмы коррозии металла не ограничиваются только наличием анодов и катодов. Протекание электронных и ионных переносов также играют важную роль. Электроны переносятся от анодов к катодам через проводник, тогда как ионы перемещаются через электролит, который может быть вода, раствор или газ. В результате этих переносов происходит окисление и растворение металла в анодной области, а на катодной области металл осаждается и восстанавливается.
Другим фактором, влияющим на механизмы коррозии металла, является концентрация кислорода и водорода в окружающей среде. Кислород ускоряет окислительные реакции, способствуя коррозии, в то время как водород может вызвать коррозию, если он выпадает из раствора. Внутреннее напряжение между анодами и катодами также может повлиять на механизмы коррозии, поскольку оно приводит к распространению коррозии по всей поверхности металла.
Анодная и катодная реакции
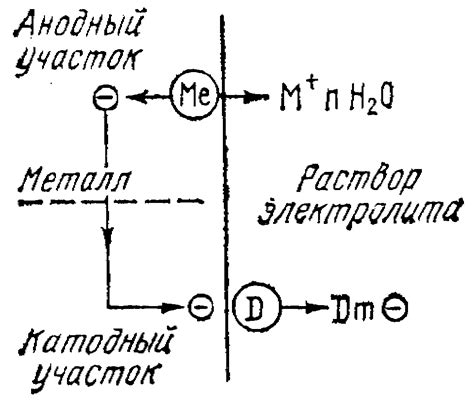
Коррозия металла - это электрохимический процесс, в котором металл подвергается разрушительному воздействию окружающей среды, что приводит к его старению и потере своих функциональных свойств.
Анодная реакция является одной из основных составляющих процесса коррозии металла. При анодной реакции происходит окисление металла, при котором из его структуры выделяются электроны. При этом образуется положительно заряженный ион металла, который переходит в среду.
Катодная реакция, в свою очередь, является парной реакцией анодной реакции. При катодной реакции происходит восстановление металла, причем электроны, выделяемые при анодной реакции, передаются на катод, где восстанавливают металлические ионы до нейтрального состояния.
Взаимодействие анодной и катодной реакций является основой всего процесса коррозии. При наличии электролита и протекании электрического тока происходит перенос ионов металла от анода к катоду. Это приводит к разрушению структуры металла, образованию коррозионных продуктов и появлению коррозионных процессов на его поверхности.
Анодная и катодная реакции определяют степень коррозии и механизм ее развития. Правильное понимание этих процессов позволяет разработать эффективные методы защиты от коррозии и предотвратить нежелательные последствия для металлических конструкций и изделий.
Влияние окружающей среды на коррозию металла
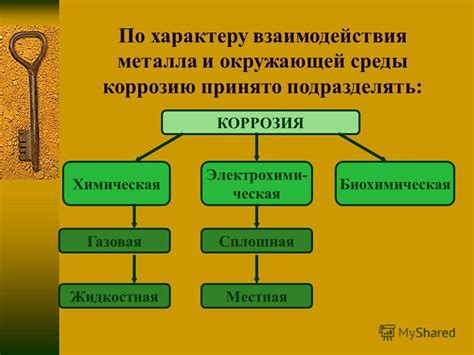
Окружающая среда играет важную роль в процессе коррозии металла. Различные факторы в окружающей среде могут ускорять или замедлять процесс коррозии.
Одним из основных факторов является наличие влаги. Вода является электролитом, которая позволяет проводить электрический ток между анодом и катодом в процессе коррозии. При наличии достаточной влажности, процесс коррозии протекает значительно быстрее.
Кроме того, содержание кислорода в окружающей среде также оказывает существенное влияние на коррозию металла. Кислород реагирует с металлом, образуя оксиды, которые являются основной причиной разрушения металлической структуры.
Наличие агрессивных химических веществ, таких как кислоты или щелочи, также способствует ускорению процесса коррозии. Они могут образовывать особые условия, при которых скорость электрохимической реакции на поверхности металла увеличивается, что приводит к ускоренному разрушению.
Также необходимо учитывать температуру окружающей среды. При повышенной температуре скорость коррозии металла может значительно возрасти из-за активации электрохимических процессов на поверхности металла.
И, наконец, механические факторы окружающей среды, такие как трение или вибрация, также могут оказывать влияние на процесс коррозии. Они могут приводить к механическому повреждению защитных слоев на поверхности металла, что способствует образованию ячеек коррозии и ускоряет процесс разрушения.
Таким образом, окружающая среда имеет значительное влияние на процесс коррозии металла. Знание этих факторов позволяет предпринять необходимые меры для защиты металлических конструкций и предотвращения их разрушения.
Вода и влажность

Вода является одним из основных факторов, способствующих коррозии металла. Влажность окружающей среды и присутствие воды на поверхности металла создают основные условия для развития электрохимических процессов, приводящих к коррозии.
Влажная среда содержит воду, а также растворенные в ней соли и другие загрязнения. Контакт металла с влагой приводит к разрушению защитных оксидных пленок, образованных на поверхности металла, и активации процессов окисления и восстановления.
Различные типы воды могут влиять на скорость развития коррозии. Например, присутствие растворенных газов, таких как кислород или углекислый газ, может ускорять окислительные процессы и способствовать коррозии. Также вода может содержать химические вещества, которые могут образовывать агрессивные растворы, повышающие коррозию металла.
Влажность окружающей среды также оказывает влияние на процессы коррозии. При высокой влажности конденсируется влага на поверхности металла, что может привести к образованию пленки влаги и увеличению времени контакта с водой. Это может способствовать развитию коррозии и приводить к более интенсивному повреждению металлической поверхности.
Основные способы предотвращения коррозии металла

Коррозия металла - это негативный электрохимический процесс, который приводит к разрушению и порче металлических поверхностей. Для предотвращения коррозии необходимо применять различные защитные методы и технологии.
1. Покрытие металла. Один из наиболее распространенных способов защиты от коррозии - это покрытие металлической поверхности специальными защитными покрытиями. Это может быть нанесение краски, эмали, лака или применение специальных антикоррозийных покрытий, таких как цинковое покрытие или порошковая краска. Покрытие создает защитный барьер между металлом и окружающей средой, предотвращая воздействие влаги и агрессивных химических веществ на металл.
2. Использование антикоррозийных добавок. Для улучшения защитных свойств металла можно добавить специальные антикоррозийные вещества в состав материала. Это могут быть антикоррозийные добавки, например, фосфаты или хроматы, которые увеличивают устойчивость металла к коррозии.
3. Метод катодной защиты. Катодная защита - это электрохимический процесс, при котором металл становится катодом и подвергается защитным мерам. Для этого создается специальная система, в которой металл соединяется с анодом из другого материала, более электрохимически активного. Катодная защита позволяет активно предотвращать коррозию, сохраняя целостность металлической поверхности.
4. Регулярное техническое обслуживание. Регулярное техническое обслуживание и уход за металлическими конструкциями и изделиями также является важным фактором для предотвращения коррозии. Это может включать очистку и протирку поверхности, удаление ржавчины и нанесение защитных средств. Регулярная проверка и поддержание состояния металлических поверхностей помогут предотвратить развитие коррозии.
5. Избегание контакта с агрессивными средами. Кроме применения защитных методов, важно избегать контакта металла с агрессивными средами, которые могут способствовать развитию коррозии. Это может включать избегание контакта с соленой водой, кислотными веществами или другими химическими агентами, которые могут повредить металл.
Вопрос-ответ

Что такое коррозия металла?
Коррозия металла является процессом разрушения металла под воздействием окружающей среды, в основе которого лежит электрохимическая реакция.
Какие факторы влияют на коррозию металла?
На коррозию металла влияют различные факторы, включая влажность, температуру, наличие кислорода и растворенных солей в окружающей среде.
Какие причины могут вызывать коррозию металла?
Коррозия металла может быть вызвана различными причинами, такими как химическое взаимодействие металла с веществами в окружающей среде, электролитическое действие и поверхностные дефекты металла.
Какие механизмы лежат в основе электрохимического процесса коррозии?
Основными механизмами электрохимического процесса коррозии являются анодный и катодный процессы. При анодном процессе происходит окисление металла, а при катодном процессе происходит восстановление.
Как можно защитить металл от коррозии?
Существует несколько способов защиты металла от коррозии, таких как использование защитных покрытий, антикоррозионных покрытий, катодной защиты и использование ингибиторов коррозии.
