В химии основные элементы составляют крупную группу металлов. Изучение свойств и химических реакций металлов является важной частью программы по химии в 9 классе. Предмет основ металлов входит в раздел "Неорганическая химия". Понимание основных характеристик металлов, их реакций и применения является ключевым для понимания химических процессов и составляет основу для дальнейшего изучения химии.
В рамках контрольной работы 9-классники должны продемонстрировать свои знания о различных аспектах металлов. Это включает в себя знание свойств различных металлов, их реакций с кислотами, основаниями и солями, а также умение решать задачи, связанные с применением металлов в жизни и промышленности.
Например, вопросы могут быть посвящены химическим реакциям металлов с кислородом, водой или солями. Ученик должен знать, какие продукты образуются при таких реакциях и какие факторы влияют на их скорость и направление. Кроме того, может быть дана задача, связанная с расчетом массы или объема реагентов и продуктов реакций.
Успешное выполнение контрольной работы по химии будет свидетельствовать о том, что ученик освоил основные понятия и законы, касающиеся химических свойств металлов. Это поможет ему лучше понять мир химических реакций и применение металлов в нашей повседневной жизни.
Определение понятий в химии металлов

Металлы - это химические элементы, которые характеризуются хорошей тепло- и электропроводностью, а также металлической блеской.
Металлизация - это процесс покрытия поверхности неметаллического или полужидкого материала слоем металла.
Электронное строение металлов определяется наличием внешней электронной оболочки незанятых электронов. Металлы имеют от одного до трех незанятых электронов в своей внешней электронной оболочке.
Амальгамы - это сплавы металлов с ртутью. Амальгамы обладают низкой температурой плавления и используются в различных областях, таких как стоматология и химическая промышленность.
Окисление - это процесс химической реакции, при которой металл соединяется с кислородом. При окислении металлы образуют оксиды, которые могут иметь различные степени окисления.
Пассивация - это явление, при котором металл приобретает пассивность, то есть оболочку оксида, которая защищает его от дальнейшего окисления и коррозии.
Металлическая химия - это раздел химии, изучающий свойства и реакции металлов, а также способы получения и применения металлических материалов. Металлическая химия важна для развития различных отраслей промышленности, таких как машиностроение, электроника и строительство.
Свойства металлов и их применение

Металлы – это химические элементы, обладающие характерными физическими и химическими свойствами. Они обладают высокой электропроводностью, теплопроводностью и металлическим блеском.
Одно из главных свойств металлов – это их способность образовывать ионные соединения с неметаллами. Это свойство делает металлы важным материалом для производства различных изделий.
Металлы широко используются в промышленности и в нашей повседневной жизни. Например, медь применяется для изготовления электрических проводов и различных электронных устройств.
Железо – это один из самых распространенных металлов. Оно используется для производства строительных конструкций, машин и орудий труда. Железо и его сплавы также применяются для производства автомобилей, железнодорожных путей и многих других предметов.
Алюминий – легкий металл, который широко используется в авиационной и автомобильной промышленности. Он также применяется для производства упаковочного материала, например, алюминиевых банок и фольги.
Свинец применяется для производства аккумуляторов и покрытий металлических изделий. Он также используется в строительстве и в других отраслях промышленности.
Это лишь некоторые примеры использования металлов. Металлы являются неотъемлемой частью нашей жизни и необходимы во многих отраслях промышленности.
Химические реакции металлов
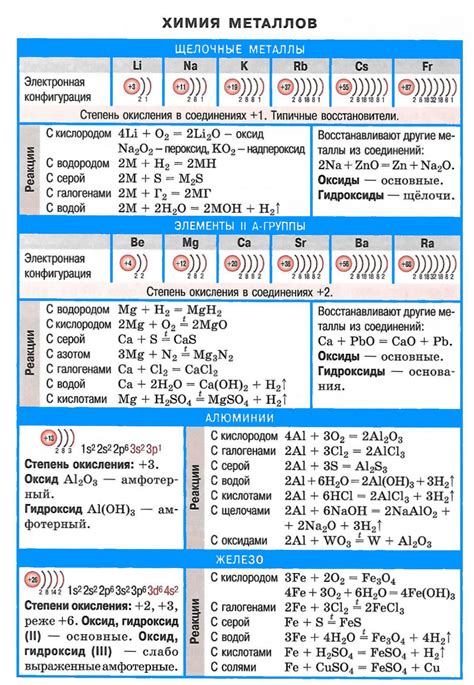
Металлы обладают высокой активностью в химических реакциях из-за своей способности отдавать электроны. Одной из основных химических реакций металлов является реакция с кислородом. В результате этой реакции металлы окисляются, переходя из нейтрального состояния в положительно заряженные ионы.
Примером реакции металла с кислородом может быть горение магния. При нагревании магния в присутствии кислорода происходит его сильное горение, в результате которого образуется оксид магния. Эта реакция сопровождается ярким свечением и высокой температурой.
Еще одной важной реакцией металлов является их реакция с водой. Реакция металлов с водой происходит при выделении водорода и образовании гидроксида металла. Некоторые металлы, такие как натрий и калий, реагируют с водой даже при комнатной температуре, образуя щелочные растворы.
Металлы также могут реагировать с кислотами, образуя соли и выделяя водород. Эта реакция основана на способности металлов отдавать электроны, что позволяет им протекать в окружающую среду. Такие реакции происходят, например, при взаимодействии цинка с соляной кислотой или алюминия с серной кислотой.
Важно отметить, что различные металлы могут иметь разные степени активности и по-разному реагировать с химическими веществами. Некоторые металлы, такие как золото и платина, обладают низкой активностью и практически не реагируют ни с кислородом, ни с водой, ни с кислотами.
В результате разных химических реакций металлов образуются различные соединения, которые имеют разные свойства и применение. Химические реакции металлов широко используются в промышленности, в металлургии, а также имеют важное значение в жизни человека.
Особенности периодической системы химических элементов

Периодическая система химических элементов является одним из главных инструментов химии. Она представляет собой систематическое упорядочение всех известных химических элементов по возрастанию их атомных номеров.
Основной принцип, на котором основана периодическая система, это расположение элементов в порядке возрастания их атомной массы и атомного номера. Каждый новый элемент имеет большую атомную массу, чем предыдущий. Таким образом, периодическая система позволяет систематизировать элементы и расставить их в порядке их свойств и химической активности.
Особенностью периодической системы является ее строение. Она состоит из строк, которые называются периодами, и столбцов, которые называются группами. Всего в периодической системе 7 периодов и 18 групп. Группы имеют общие химические свойства, а периоды отражают изменение строения электронных оболочек элементов.
В периодической системе элементы образуют горизонтальные ряды, называемые периодами, и вертикальные столбцы, называемые группами. Каждая группа имеет свое название и номер, а также характеризуется особыми свойствами. Например, группа 1 - алкалии, которые обладают высокой химической активностью, а группа 18 - инертные газы, которые практически не реагируют с другими элементами.
Помимо этого, периодическая система также показывает связь между свойствами элементов и их расположением. Например, в одной и той же группе элементы имеют похожие свойства, так как они имеют одинаковое количество валентных электронов. Это позволяет делать предположения о химических свойствах еще неизвестных элементов.
Таким образом, периодическая система химических элементов является важным инструментом для понимания свойств и взаимодействия химических элементов. Благодаря систематическому упорядочению и классификации элементов, она позволяет установить закономерности и предсказать свойства еще неизвестных элементов.
Вопрос-ответ

Что такое основы металлов?
Основы металлов - это химические соединения, которые образуют базические оксиды воздействуя на воду. Они являются химически активными веществами и обладают способностью взаимодействовать с кислотами, образуя соли и выделяя воду.
Какие металлы являются основами?
В основном основами являются щелочные и щелочноземельные металлы. Это натрий, калий, литий, цезий, рубидий, магний, кальций, стронций и барий.
