Щелочные металлы представляют собой группу элементов в таблице химических элементов, включающую литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они относятся к активным металлам и обладают рядом уникальных физических свойств.
Первое физическое свойство щелочных металлов - низкая плотность. Они обладают небольшой массой в сочетании с большим объемом. Например, литий имеет плотность всего 0,5 г/см³. Это свойство делает щелочные металлы отличными материалами для использования в легких конструкциях и летательных аппаратах.
Второе физическое свойство - мягкость и пластичность. Щелочные металлы можно легко рассечь ножом или согнуть без значительного усилия. Например, натрий так мягок, что его можно резать ножом. Это свойство обуславливает их широкое применение в производстве легкосплавов и сплавов с другими металлами.
Третье физическое свойство - высокая электропроводность. Щелочные металлы являются отличными проводниками электричества. Они обладают высокой подвижностью электронов, что позволяет им эффективно перемещаться в структуре кристаллической решетки. Это свойство делает их полезными для использования в производстве электроники и аккумуляторов.
Физические свойства щелочных металлов:

1. Мягкость и пластичность. Щелочные металлы являются очень мягкими и пластичными веществами. Они легко поддаются деформации и могут быть вытянуты в тонкую проволоку или раскатаны в тонкую пленку. Благодаря этим свойствам, щелочные металлы широко используются в производстве проводников и покрытий.
2. Низкая плотность. Щелочные металлы обладают низкой плотностью, что означает, что они очень легкие. Например, литий, самый легкий из щелочных металлов, имеет плотность всего около 0,5 г/см³. Это позволяет использовать эти металлы в легких конструкциях и при создании лёгких материалов.
3. Высокая теплопроводность. Щелочные металлы обладают высокой теплопроводностью. Они способны быстро передавать тепло и энергию. Это свойство делает их полезными в различных технических приложениях, таких как теплообменники и системы охлаждения.
4. Низкая температура плавления. Щелочные металлы имеют низкую температуру плавления. Например, натрий плавится при температуре около 98 °C, что делает его достаточно жидким при комнатной температуре. Это позволяет использовать щелочные металлы в процессах с низкими температурами, например, при создании светящихся веществ.
5. Химическая реакционность. Щелочные металлы отличаются высокой химической реакционностью. Они легко взаимодействуют с водой, кислородом и другими реагентами. Это делает их опасными в обращении, но также открывает широкие возможности для использования в химической промышленности.
Электропроводность и легкость сплавления
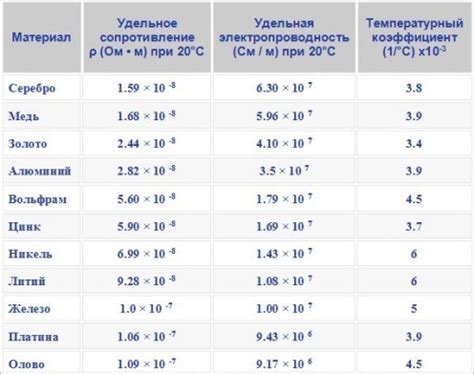
Щелочные металлы, такие как литий, натрий, калий и другие, обладают высокой электропроводностью. Это связано с их структурой и химическими свойствами. Атомы щелочных металлов имеют всего один валентный электрон во внешней электронной оболочке, что делает их атомы очень реактивными и склонными к образованию ионов с положительным зарядом.
Электропроводность щелочных металлов проявляется в том, что они способны эффективно проводить электрический ток. Это свойство является основой для использования этих металлов в различных электрических устройствах, батареях, проводниках и других приложениях. Благодаря высокой электропроводности, щелочные металлы широко используются в производстве аккумуляторов, которые позволяют эффективно хранить источник электрической энергии.
Еще одной важной характеристикой щелочных металлов является их легкость сплавления. Щелочные металлы обладают низкими температурами плавления, что позволяет им быстро и легко переходить из твёрдого состояния в жидкое. Например, литий плавится при температуре всего 180,5 °C, что делает его одним из самых легко плавящихся металлов. Это свойство открывает перед ними широкие возможности в процессе сплавления с другими материалами для создания различных сплавов и соединений с нужными свойствами и характеристиками.
Высокая реактивность и алкалинность
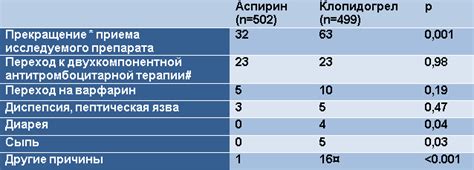
Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, обладают высокой реактивностью и являются одними из самых активных элементов в периодической системе. Это связано с тем, что у них только один электрон в валентной оболочке, что делает их легкими катионами с положительным зарядом.
Их высокая реактивность проявляется в том, что они легко реагируют с кислородом, водой, кислотами и другими веществами. Когда щелочные металлы взаимодействуют с водой, возникает химическая реакция, в результате чего образуется щелочное растворимое гидроксид и выделяется водород.
Алкалинность щелочных металлов заключается в их способности образовывать щелочные растворы, которые обладают высоким уровнем pH. Благодаря этому свойству, щелочные металлы широко применяются в промышленности и научных исследованиях, особенно натрий и калий, которые используются в производстве стекла, щелочных батарей, гидроксидов и других химических соединений.
Также щелочные металлы обладают высокой способностью проводить тепло и электричество, что делает их полезными в производстве электроники и батарей.
Мягкость и низкая плотность

Щелочные металлы обладают особой физической характеристикой - мягкостью - что делает их уникальными среди других металлов. Их мягкость проявляется в том, что они легко портятся и деформируются при небольшом воздействии. Любой, кто когда-либо держал в руках кусок щелочного металла, может подтвердить это.
Важной особенностью щелочных металлов является их низкая плотность. По сравнению с другими металлами, такими как железо или алюминий, щелочные металлы имеют гораздо меньшую плотность. Например, литий, самый легкий из щелочных металлов, имеет плотность всего около 0,53 г/см³, в то время как плотность железа составляет около 7,87 г/см³.
Эта низкая плотность делает щелочные металлы полезными во многих областях, таких как авиационная и космическая промышленность. Благодаря своей низкой плотности, они помогают уменьшить вес и обеспечить легкость конструкций. Кроме того, их мягкость позволяет легко формировать их в различные формы и структуры с минимальным усилием и затратами.
Высокая теплопроводность и низкая температура плавления
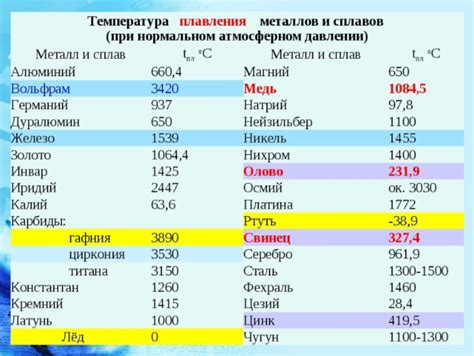
Щелочные металлы, такие как литий (Li), натрий (Na), калий (K) и рубидий (Rb), обладают высокой теплопроводностью и низкой температурой плавления.
Высокая теплопроводность щелочных металлов обусловлена их кристаллической структурой, в которой атомы металла расположены в плотных сложенных пакетах. Это обеспечивает эффективную передачу тепла через металлическую решетку, что делает эти металлы хорошими проводниками тепла.
Низкая температура плавления щелочных металлов объясняется слабостью межатомных связей в их кристаллической структуре. Межатомные связи в щелочных металлах являются относительно слабыми, что позволяет достичь температуры плавления ниже комнатной температуры. Например, натрий плавится при температуре около 97,8°C.
Сочетание высокой теплопроводности и низкой температуры плавления делает щелочные металлы полезными в различных сферах, включая производство батарей, сплавов и пиротехники. Их низкая температура плавления также делает их удобными для использования в жидком состоянии, например, в жидком охлаждающем теплоносителе в некоторых ядерных реакторах.
Свойства щелочных металлов в вакууме

Щелочные металлы (литый натрий, калий, рубидий, цезий и франций) обладают уникальными свойствами, которые проявляются исключительно в вакууме. В отсутствие воздуха и других газов, вакуумное окружение создает особые условия для исследования и экспериментов с щелочными металлами.
Одним из главных физических свойств щелочных металлов в вакууме является их высокая реактивность. В отсутствие газов, которые могут реагировать с металлами, щелочные металлы могут продемонстрировать свою способность активно взаимодействовать с другими элементами и соединениями.
Другим важным свойством щелочных металлов в вакууме является их низкая температура плавления. В пустоте вакуума, где нет внешних факторов, таких как воздух или давление, щелочные металлы могут плавиться при намного более низких температурах, чем в обычных условиях.
Вакуум также позволяет щелочным металлам проявить свою металлическую проводимость электричества и тепла в полной мере. Без присутствия других газов, которые могут повлиять на проводимость, щелочные металлы могут демонстрировать свои уникальные электрические и теплопроводные свойства.
- Вакуумное окружение также позволяет изучать дополнительные свойства щелочных металлов, такие как их магнитные свойства и поведение при высоких давлениях.
- Один из интересных аспектов исследования щелочных металлов в вакууме - возможность создания и изучения новых структур и соединений, которые могут быть стабильными только в отсутствие газового окружения.
- Вакуум позволяет изучать и дополнительные аспекты щелочных металлов, такие как их поверхностные свойства и реакции с другими материалами.
Применение щелочных металлов в различных отраслях

Щелочные металлы - это группа химических элементов, включающих литий, натрий, калий, рубидий, цезий и франций. Их уникальные физические свойства делают их незаменимыми в различных отраслях науки и промышленности.
Во-первых, щелочные металлы широко используются в электроэнергетике. Натрий и калий применяются в составе теплоносителей для ядерных реакторов благодаря своей высокой теплопроводности и низкой радиационной активности. Они также применяются в производстве солнечных батарей для накопления электрической энергии.
Во-вторых, щелочные металлы являются важными компонентами в химической промышленности. Калий используется в производстве удобрений, так как является необходимым элементом для роста растений. Литий используется в производстве литиевых ионных аккумуляторов для мобильных устройств и электромобилей. Натрий и калий также используются в производстве мыла, стекла и многих других химических соединений.
В-третьих, щелочные металлы имеют широкое применение в медицине. Калий играет важную роль в поддержании нормальной функции сердца и нервной системы. Литий используется в лечении психических расстройств, таких как маниакально-депрессивное расстройство.
В-четвертых, щелочные металлы находят применение в производстве стекла и керамики. Натрий и калий добавляются в стекло для повышения его прочности и устойчивости к воздействию тепла. Калий также используется в производстве горных пород и керамических изделий.
В-пятых, щелочные металлы находят применение в различных научных исследованиях. Цезий используется в атомных часах и оптических датчиках. Литий применяется в ядерной физике для создания термоядерного топлива.
Таким образом, щелочные металлы играют важную роль в различных отраслях науки и промышленности, благодаря своим уникальным физическим свойствам и химическим связям.
Вопрос-ответ

Какие физические свойства обладают щелочные металлы?
Щелочные металлы обладают такими физическими свойствами, как низкая плотность, низкая температура плавления и кипения, мягкость и хорошая теплопроводность. Они также хорошо проводят электричество и имеют низкую энергию ионизации.
Почему щелочные металлы обладают низкой плотностью?
Низкая плотность щелочных металлов обусловлена их атомной структурой. Атомы щелочных металлов имеют большой радиус и низкую атомную массу, поэтому их атомы, находящиеся в кристаллической решетке, не сильно взаимодействуют друг с другом. Это делает металлы менее плотными.
Какова химическая активность щелочных металлов?
Щелочные металлы являются одними из самых химически активных металлов. Они легко реагируют с водой, кислородом и другими веществами, образуя гидроксиды, оксиды и соли. Они также обладают высокой энергией ионизации, что делает их реактивными.
В чем заключается мягкость щелочных металлов?
Мягкость щелочных металлов обусловлена их слабыми межатомными связями. Атомы щелочных металлов имеют низкую энергию ионизации, поэтому они легко отдают внешний электрон, образуя положительный ион. Эти положительные ионы слабо связаны друг с другом, что делает металлы мягкими и легко деформируемыми.
Какие у щелочных металлов свойства, связанные с теплопроводностью?
Щелочные металлы обладают хорошей теплопроводностью. Это связано с их структурой кристаллической решетки и наличием свободных электронов. Электроны могут свободно двигаться по решетке и передавать тепло. Благодаря этому, щелочные металлы хорошо проводят тепло.
