Реакции металлов с кислотами являются важной темой в химии. Они позволяют изучать активность металлов и определять их химические свойства. Одной из наиболее интересных реакций является взаимодействие концентрированной азотной кислоты с различными металлами. Эта реакция стала предметом множества исследований, в ходе которых учеными были выявлены некоторые закономерности активности металлов.
Концентрированная азотная кислота является сильной окислительной кислотой, способной взаимодействовать с большим количеством металлов. Однако, не все металлы одинаково активны по отношению к азотной кислоте. Некоторые металлы, такие как калий или натрий, реагируют с кислотой с большим разогреванием, при этом выделяются яркие искры. В то время как другие металлы, вроде железа или меди, реагируют гораздо медленнее и без явных признаков активности.
Исследования показали, что активность металлов в реакции с азотной кислотой зависит от нескольких факторов. Важную роль играют электрохимические свойства металла, такие как потенциал окисления и электроотрицательность. Чем больше потенциал окисления металла, тем активнее он реагирует с кислотой. Также влияет степень окисления, наличие пассивной пленки на поверхности металла, а также состояние агрегатного состояния металла.
Влияние концентрации азотной кислоты на реакцию с металлами

Реакция концентрированной азотной кислоты с металлами является одной из наиболее популярных химических реакций, которая привлекает внимание исследователей со всего мира. Однако, одним из важных факторов, влияющих на эту реакцию, является концентрация азотной кислоты.
Исследования показывают, что при повышении концентрации азотной кислоты реакция с металлами становится более интенсивной. Это объясняется тем, что повышение концентрации приводит к увеличению количества активных ионов в растворе, что обеспечивает больший потенциал для реакций с металлами.
Более концентрированная азотная кислота обладает более высокой кислотностью, что обеспечивает более быстрое протекание реакции. Кроме того, повышенная концентрация азотной кислоты может увеличивать активность металлов, за счет более интенсивного воздействия на их поверхность.
Однако, имеется определенный предел концентрации азотной кислоты, при котором реакция может замедляться или становиться менее интенсивной. Высокая концентрация азотной кислоты может приводить к образованию защитной пленки на поверхности металла, что уменьшает его активность и затрудняет протекание реакции.
Исследования влияния концентрации азотной кислоты на реакцию с металлами имеют большое значение для понимания процессов, происходящих при растворении металлов в кислотных средах. Они позволяют определить оптимальные условия для проведения реакций и эффективного использования азотной кислоты в различных промышленных процессах.
Изучение химической активности металлов в реакции с азотной кислотой
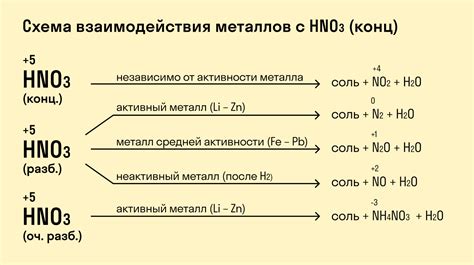
Азотная кислота (HNO3) является одним из наиболее активных окислителей и используется в лаборатории для растворения различных металлов. Изучение реакции азотной кислоты с металлами позволяет определить их химическую активность и создать закономерности, которые могут быть использованы в дальнейших исследованиях и практических применениях.
Реакция металлов с азотной кислотой происходит по следующей схеме: металл реагирует с кислородом, который образуется при разложении азотной кислоты, образуется соответствующий нитрат металла и выделяется диоксид азота и/или окислы азота. Процесс сопровождается выделением тепла и возможным образованием пены или газовых пузырьков.
В ходе экспериментов было установлено, что некоторые металлы проявляют большую активность в реакции с азотной кислотой, чем другие. Например, щелочные металлы, такие как натрий и калий, реагируют с азотной кислотой сильно и быстро, выделяя большое количество газовых пузырьков и часто приводя к непроизводимому взрыву.
С другой стороны, благородные металлы, такие как золото и платина, очень плохо реагируют с азотной кислотой и могут оставаться практически неизменными в целом процессе.
Таким образом, изучение реакции концентрированной азотной кислоты с металлами позволяет установить иерархию их активности и определить, какие металлы легко растворяются в азотной кислоте, а какие остаются устойчивыми. Эти сведения могут быть полезными для разработки новых материалов, а также для понимания химических процессов, происходящих в природе и в промышленности.
Зависимость скорости реакции от природы металла
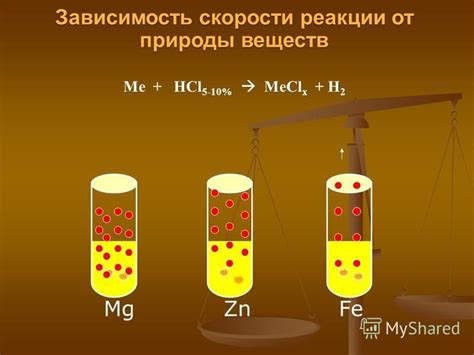
Скорость реакции между концентрированной азотной кислотой и различными металлами может существенно изменяться в зависимости от природы металла. Некоторые металлы активно взаимодействуют с азотной кислотой, проявляя большую скорость реакции, тогда как у других металлов эта скорость намного ниже.
Активность металлов в реакции с азотной кислотой может быть определена на основании продолжительности реакции или осадка, образующегося в результате взаимодействия металла с кислотой. Металлы, такие как натрий, кальций и магний, активно реагируют с азотной кислотой, образуя газообразные продукты и интенсивно пенящийся осадок.
Другие металлы, такие как алюминий и цинк, также реагируют с азотной кислотой, но скорость реакции может быть ниже, так как образующийся на металле оксидная пленка может замедлять процесс взаимодействия. Следующая группа металлов, включающая свинец и медь, обладает низкой активностью в реакции с азотной кислотой, и реакция может происходить очень медленно или вовсе не происходить.
Таким образом, зависимость скорости реакции концентрированной азотной кислоты с металлами напрямую связана с природой металла. Активность металла определяется его свойствами и способностью вступать в химические реакции с кислотами. Изучение этой зависимости позволяет лучше понять химическую активность металлов и их взаимодействие с кислотами.
Факторы, влияющие на эффективность реакции

1. Активность металла: Реакция концентрированной азотной кислоты с металлами зависит от их активности. Чем выше активность металла, тем быстрее и эффективнее протекает реакция. Например, реакция с активными металлами, такими как натрий или калий, протекает очень быстро, а с менее активными металлами, такими как железо или медь, требуется больше времени.
2. Концентрация азотной кислоты: Концентрация азотной кислоты также влияет на эффективность реакции. При повышении концентрации азотной кислоты увеличивается скорость реакции и вероятность успешного взаимодействия с металлом. Однако слишком высокая концентрация может привести к более интенсивной реакции, что может быть опасно и требует особой осторожности.
3. Поверхность металла: Поверхность металла также играет роль в эффективности реакции. Чем больше поверхность металла, тем больше мест для взаимодействия металла с азотной кислотой и тем более эффективной будет реакция. Например, мелко растресканная или порошкообразная форма металла зачастую приводит к более интенсивной реакции, чем массивные куски металла.
4. Температура: Температура также влияет на эффективность реакции. При повышении температуры скорость реакции увеличивается, что может привести к более эффективному протеканию реакции с металлом. Температура может быть контролируемой переменной, позволяющей увеличить или уменьшить скорость реакции в зависимости от требуемых результатов.
5. Взаимодействие с другими соединениями: Взаимодействие азотной кислоты с другими соединениями, такими как соли или органические вещества, также может влиять на эффективность реакции. Наличие растворенных солей или органических веществ, в зависимости от их природы и концентрации, может изменить скорость и интенсивность реакции с металлом.
В целом, эффективность реакции азотной кислоты с металлами зависит от активности металла, концентрации азотной кислоты, поверхности металла, температуры и взаимодействия с другими соединениями. Учет и оптимизация этих факторов позволяют достичь наиболее эффективных результатов в исследовании реакции концентрированной азотной кислоты с металлами.
Исследование влияния температуры на скорость реакции металла с азотной кислотой
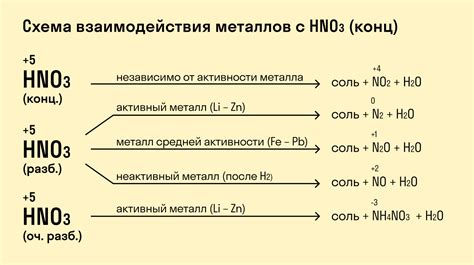
Один из факторов, влияющих на скорость реакции металла с азотной кислотой, является температура. Известно, что при повышении температуры скорость химических реакций увеличивается. Исследование влияния температуры на реакцию между металлом и концентрированной азотной кислотой позволяет установить закономерности активности различных металлов.
При проведении эксперимента были использованы различные металлы, такие как железо, цинк, медь и алюминий. Каждый металл был помещен в азотную кислоту, а затем наблюдалась скорость реакции при разных температурах.
Результаты исследования показали, что при повышении температуры реакция между металлом и азотной кислотой происходит быстрее. Это объясняется тем, что при повышенной температуре молекулы азотной кислоты обладают большей кинетической энергией и могут взаимодействовать с металлом более интенсивно.
Также было установлено, что различные металлы имеют разную активность при реакции с азотной кислотой. Например, железо проявляет высокую активность, быстро вступая в реакцию с кислотой, в то время как алюминий проявляет низкую активность, реагируя медленнее.
Таким образом, исследование влияния температуры на скорость реакции металла с азотной кислотой позволяет установить закономерности активности металлов и понять, как физические условия влияют на химическую реакцию.
Определение оптимальной концентрации азотной кислоты для реакции с металлами
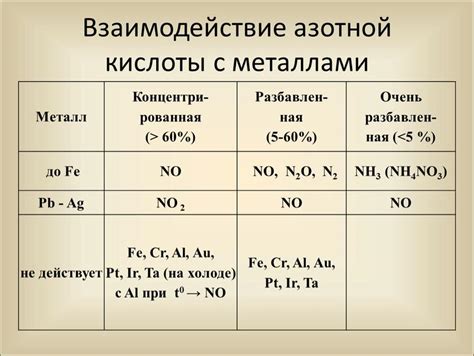
Реакция концентрированной азотной кислоты с металлами является одной из основных реакций в химической лаборатории. Определение оптимальной концентрации азотной кислоты для данной реакции является важной задачей, решение которой позволяет получить максимальное количество продукта при минимальных затратах времени и реагентов.
В химической лаборатории проводятся эксперименты, в которых изучаются различные концентрации азотной кислоты и ее влияние на скорость реакции с металлами. Для этого используются различные металлы, такие как железо, алюминий, медь и др. Эксперименты проводятся при разной концентрации азотной кислоты, начиная от низкой и постепенно повышая ее, чтобы определить оптимальную концентрацию.
Определение оптимальной концентрации азотной кислоты осуществляется путем измерения скорости реакции при разных концентрациях. Обнаруживается, что с увеличением концентрации азотной кислоты реакция с металлами происходит быстрее. Однако, при слишком высокой концентрации, могут происходить побочные реакции, что может быть нежелательно.
В результате проведения экспериментов и анализа данных определяется оптимальная концентрация азотной кислоты для реакции с каждым из металлов. Это позволяет получить наибольшую выходную продукцию при наименьших затратах реагентов и времени. Определение оптимальной концентрации азотной кислоты для реакции с металлами имеет практическое значение и позволяет оптимизировать процессы химического синтеза.
Вопрос-ответ

Какая реакция происходит при взаимодействии азотной кислоты и металлов?
При взаимодействии азотной кислоты с металлами происходит окислительно-восстановительная реакция, в результате которой азотная кислота окисляет металл, а сама превращается в азотные оксиды.
Какие металлы реагируют с азотной кислотой?
Реакция металлов с азотной кислотой зависит от их активности. В целом, реакцию можно наблюдать с металлами активной группы, такими как литий (Li), натрий (Na), калий (K), магний (Mg), кальций (Ca) и др. Металлы низкой активности, такие как железо (Fe), свинец (Pb) и медь (Cu), обычно не реагируют с азотной кислотой.
Почему активность металлов влияет на реакцию с азотной кислотой?
Активность металлов влияет на их способность отдавать электроны. Металлы более активной группы имеют более слабую связь с электронами, поэтому они легче отдают электроны азотной кислоте, окисляясь при этом. Металлы менее активной группы имеют более сильную связь с электронами, поэтому они труднее отдают электроны и не реагируют с азотной кислотой.
