Алюминий - один из самых распространенных металлов в земной коре, а его соединения используются во многих отраслях промышленности. Важным аспектом его химических свойств является его способность к окислению в присутствии кислорода. Сегодня мы поговорим о количестве вещества кислорода, необходимого для окисления 1 моля металла алюминия.
Алюминий является хорошим окислителем и обладает свойством образовывать стабильный оксидный слой на поверхности металла. Этот слой защищает алюминий от дальнейшего окисления и коррозии. Однако, для образования этого слоя необходимо наличие определенного количества кислорода.
Для окисления 1 моля алюминия требуется 3 моля кислорода. Это означает, что каждый атом алюминия вступает в реакцию с 3 молекулами кислорода, образуя 2 молекулы алюминиевого оксида (Al2O3). Уравнение окислительной реакции выглядит следующим образом:
4 Al + 3 O2 → 2 Al2O3
Таким образом, массовая доля кислорода в алюминиевом оксиде составляет примерно 53%. Это перспективное свойство алюминия позволяет ему использоваться в аэрокосмической и строительной промышленности, а также в производстве различных материалов и изделий.
Количество вещества кислорода
Количество вещества кислорода - это физическая величина, которая определяет количество молекул кислорода в данной системе. Она является важным показателем во многих химических реакциях и процессах.
В химии количество вещества измеряется в единицах, называемых молями. Моль - это количество вещества, содержащее столько же частиц, сколько атомов в 12 граммах углерода-12. Таким образом, молярная масса кислорода равна примерно 16 г/моль.
Количество вещества кислорода часто используется для вычисления необходимого количества кислорода для проведения химических реакций. Например, для окисления одного моля металла алюминия (Al) необходимо два моля кислорода (O2). Это связано с тем, что соединение алюминия с кислородом образует оксид алюминия (Al2O3), в котором один атом алюминия соединяется с двумя атомами кислорода.
Количество вещества кислорода также может быть использовано для вычисления массы кислорода в заданном количестве вещества. Для этого необходимо знать молярную массу кислорода и количество вещества кислорода в системе. Далее, используя простое математическое соотношение - количество вещества = масса / молярная масса, можно вычислить массу кислорода.
Для окисления 1 моля металла алюминия требуется определенное количество вещества кислорода
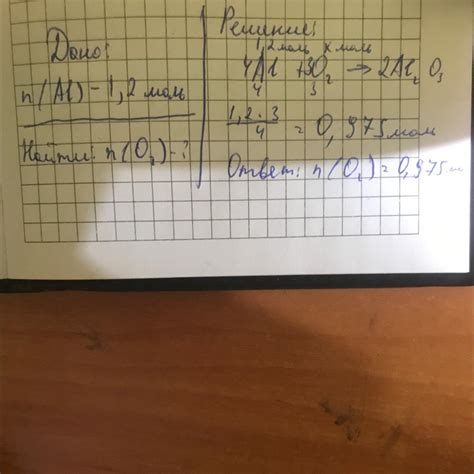
Алюминий – это металл, который хорошо окисляется воздухом. Окисление алюминия происходит в результате соединения металла с кислородом, при этом образуется единственный возможный оксид алюминия – Al2O3. Чтобы этот процесс мог произойти, требуется определенное количество вещества кислорода.
Молярная масса алюминия равна около 27 г/моль, а молярная масса кислорода составляет приблизительно 16 г/моль. Что означает, что для окисления 1 моля алюминия потребуется 1 моль кислорода.
При этом необходимо учитывать, что металл алюминий может иметь различные степени окисления. Например, оксид алюминия Al2O3 соответствует максимальной степени окисления +3, но алюминий также может образовывать соединения с меньшей степенью окисления, например, оксид AlO.
Количество вещества кислорода, необходимого для окисления 1 моля металла алюминия, варьируется в зависимости от конкретного соединения. Для точного расчета необходимо знать состав и степень окисления алюминия в данном соединении, а также учитывать стехиометрическое соотношение между алюминием и кислородом в реакции окисления.
Физические свойства кислорода
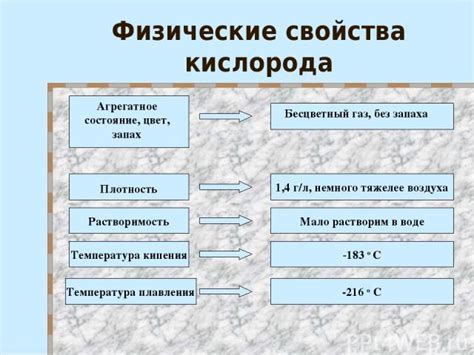
Физические свойства кислорода определяют его способность к существованию в различных физических состояниях и взаимодействию с другими веществами.
Температура и плотность: Кислород – один из немногих газов, который может существовать при комнатной температуре в виде газа. Критическая температура кислорода составляет -118,8 °C, при которой газ превращается в жидкость. Плотность кислорода при нормальных условиях составляет около 1,429 г/л.
Цвет и запах: Кислород является безцветным газом без запаха.
Растворимость: Кислород растворим в воде, при этом растворимость снижается с увеличением температуры.
Плотность: Наибольшая плотность кислород достигает при температуре -183 °C и составляет около 1,4 г/см³. В жидком состоянии кислород является тяжелее воды.
Точка кипения и плавления: Точка кипения кислорода составляет -183 °C, а точка плавления -218,79 °C.
Реактивность: Кислород является очень активным химическим элементом и способен вступать во множество химических реакций. Он является сильным окислителем и поджигает неорганические и органические вещества.
Насыщенность воздуха: В атмосфере находится около 20,95% кислорода, что обеспечивает жизнедеятельность многих организмов на Земле.
Роль кислорода в природе
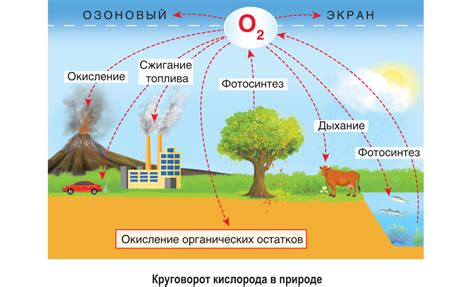
Кислород – один из важнейших элементов, обеспечивающих жизнедеятельность на Земле. Он является необходимым компонентом для дыхания и окисления многих организмов. Благодаря кислороду происходят все процессы сжигания и дыхания, которые обогащают окружающую среду, атмосферу и воду.
В природе кислород широко распространен в атмосфере, составляя около 21% ее общего объема. Он также присутствует в молекулярном виде в воде, находящейся в океанах, реках, озерах и влажности почвы. Кислород связан с другими элементами в органических и неорганических соединениях, образуя оксиды и оксигемоглобин в крови, необходимый для поддержания жизнедеятельности организмов.
Однако кислорода не хватает в тех местах, где происходит интенсивное сжигание органического вещества, например, при пожарах или в промышленных районах. В таких условиях отсутствие кислорода может привести к серьезным последствиям, таким как отравление или задышка.
Кроме того, кислород является важным компонентом в процессе окисления металлов. Например, для окисления 1 моля металла алюминия необходимо 3 моля кислорода. Этот процесс играет важную роль в производстве алюминия, который широко используется в промышленности, строительстве и бытовых целях.
Химические реакции алюминия

Алюминий - это химический элемент с атомным номером 13 и символом Al на периодической системе элементов. Он является активным металлом, который может реагировать с различными веществами, образуя разнообразные химические соединения.
Одной из самых известных реакций алюминия является его взаимодействие с кислородом воздуха. Алюминий окисляется до оксида алюминия (Al2O3) в результате этой реакции. Это образует тонкую защитную пленку на поверхности металла, которая предотвращает дальнейшую реакцию с кислородом. Этот процесс также известен как пассивация алюминия.
Алюминий также может реагировать с кислотами. Например, при взаимодействии алюминия с соляной кислотой (HCl) выделяется водород (H2) и образуется соль алюминия (AlCl3). Такие реакции широко используются в лаборатории и промышленности для производства алюминиевых солей.
Алюминий также может реагировать с щелочами, например, натрием гидроксидом (NaOH), образуя гидроксид алюминия (Al(OH)3). Эта реакция также называется гидролизом алюминия. Гидроксид алюминия может быть использован в процессах обеззараживания воды и как ингредиент в производстве различных химических соединений.
Реакции алюминия с другими элементами и веществами, такими как хлор, фосфор и сера, также часто исследуются и используются в промышленности и научных исследованиях. Таким образом, алюминий является важным химическим элементом, который имеет широкий спектр реакций и применений.
Окисление металла алюминия с кислородом и другими веществами
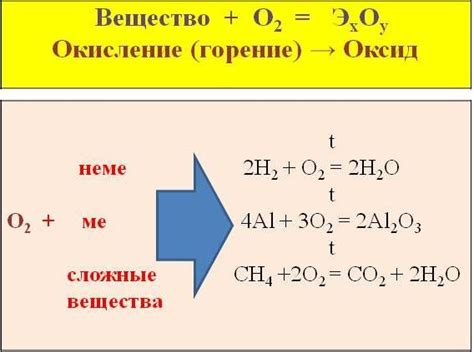
Кислород является одним из наиболее распространенных и активных окислителей, который может реагировать с многими веществами, включая металл алюминий. Алюминий обладает высокой реакционной способностью, что делает его подходящим объектом для исследования окисления с использованием кислорода и других веществ.
Одним из результатов этой реакции является образование оксида алюминия (Al2O3), которое является защитным слоем на поверхности алюминия и предотвращает дальнейшее окисление. Этот слой защищает металл от коррозии и придает ему дополнительную прочность.
Кроме реакции с кислородом, металл алюминий может образовывать соединения с другими веществами, например с хлором, фосфором и серой. Эти соединения имеют важное применение в различных отраслях промышленности, таких как производство алюминиевых сплавов, фармацевтическая и пищевая промышленность.
Окисление металла алюминия с кислородом и другими веществами является важным процессом, который применяется в различных технологических процессах, включая производство алюминиевых конструкций, электролитическое получение алюминия и другие.
- Окисление алюминия с кислородом и другими веществами может приводить к образованию различных соединений;
- Оксид алюминия является защитным слоем, предотвращающим дальнейшее окисление;
- Алюминий может образовывать соединения с хлором, фосфором и серой;
- Процесс окисления алюминия имеет широкие применения в промышленности.
Первоначальное состояние

Первоначальное состояние металла алюминия характеризуется его атомной структурой, свойствами и химической активностью. Непосредственно перед окислением, алюминий находится в металлическом состоянии и обладает свойствами мягкости, легкости и хорошей проводимости электричества. Его атомы составляют регулярную кристаллическую решетку, в которой они связаны слабыми межатомными силами.
К атомам алюминия может быть прикреплено несколько атомов кислорода, образуя специфические соединения, такие как оксиды и гидроксиды. Однако, перед окислением, на поверхности алюминия образуется оксидная пленка из алюминия и кислорода, которая служит защитой от дальнейшей окислительной реакции.
Первоначальное состояние металла алюминия может быть представлено в виде таблицы, где перечислены его основные характеристики:
| Свойство | Значение |
|---|---|
| Масса атома | 26.98 ед. массы |
| Электроотрицательность | 1.61 (по шкале Полинга) |
| Температура плавления | 660.32°C |
| Плотность | 2.70 г/см³ |
Таким образом, в первоначальном состоянии металл алюминия является стабильным, металлическим веществом с определенными химическими свойствами.
Металл алюминия до окисления

Алюминий – это легкий, прочный и хорошо поддающийся обработке металл, который широко применяется в различных областях промышленности. Однако без окисления алюминий не может образовать защитную оксидную пленку на своей поверхности, что делает его более уязвимым к коррозии.
Оксидация алюминия – это процесс, при котором алюминий вступает в реакцию с молекулами кислорода, образуя оксид алюминия. Для этого требуется определенное количество кислорода, которое можно выразить в количестве вещества.
Масса одного моля алюминия составляет около 26,98 грамма. Следовательно, для окисления одного моля алюминия требуется такое же количество кислорода. Между тем, молярная масса кислорода равна примерно 32 граммам. Это означает, что для окисления одного моля алюминия требуется около 32 граммов кислорода.
Если предположить, что имеется определенное количество алюминия, то количество кислорода, необходимое для его окисления, можно рассчитать по формуле Моя Моль разделить молярную массу кислорода разделить на молярную массу алюминия и умножить на количество молей алюминия. Таким образом, можно получить точное количество кислорода, требуемое для окисления заданного количества алюминия.
Процесс окисления алюминия кислородом

Взаимодействие металла алюминия с кислородом является одним из фундаментальных процессов, основой для получения оксида алюминия. Окисление алюминия происходит в присутствии кислорода из воздуха, при этом образуется тонкая пленка оксида на поверхности металла.
Окисление алюминия сопровождается реакцией, в результате которой образуется оксид алюминия (Al2O3). Эта реакция имеет место при нагревании алюминия до высоких температур, обычно выше 600 градусов по Цельсию. При этой температуре, кислород реагирует с поверхностными атомами алюминия, образуя оксидные соединения.
Окисление алюминия кислородом является экзотермическим процессом, то есть при этом выделяется теплота. Это явление происходит за счет образования новых химических связей между атомами алюминия и кислорода.
При окислении алюминия кислородом важную роль играют поверхностные условия и катализаторы. Наличие природного оксида алюминия на поверхности металла повышает скорость окисления за счет катализа. Также, электрохимический потенциал металла алюминия влияет на скорость процесса окисления, что позволяет использовать эту реакцию в промышленности для получения оксида алюминия и его соединений.
Вопрос-ответ

Сколько кислорода необходимо для окисления 1 моля алюминия?
Для окисления 1 моля алюминия, необходимо 3 моля кислорода.
Какое количество кислорода требуется для полного окисления 1 моля алюминия?
Для полного окисления 1 моля алюминия необходимо 3 моля кислорода.
Какая реакция происходит при окислении 1 моля алюминия?
При окислении 1 моля алюминия происходит реакция, в результате которой получается 1 моль оксида алюминия.
Почему для окисления 1 моля алюминия требуется именно 3 моля кислорода?
Для окисления 1 моля алюминия требуется 3 моля кислорода, потому что масса алюминия в 3 раза больше массы кислорода, и для полного окисления алюминия необходимо соответствующее количество кислорода.
