Взаимодействие кислот с металлами и неметаллами является одним из фундаментальных процессов в химии. Оно позволяет не только понять природу различных веществ, но и найти их широкое применение в различных областях науки и техники. Взаимодействие кислот с металлами и неметаллами основано на их структурной и химической схожести, а также на энергетических потенциалах, которые определяют возможность проведения реакции.
Взаимодействие кислот с металлами основывается на способности металлов отдавать электроны. Кислоты, в свою очередь, являются источником протонов. Когда кислота и металл взаимодействуют, протоны кислоты реагируют с электронами металла, образуя водород. При этом металл может раствориться в кислоте, образуя соль и освобождаясь отдельным водородом или взаимодействовать с кислотой, но не растворяться в ней. Взаимодействие кислот с металлами может происходить с выделением тепла и образованием пены или газа.
Взаимодействие кислот с неметаллами также основано на структурной и химической схожести веществ. Однако, в отличие от металлов, неметаллы не способны отдавать электроны. Вместо этого, они образуют связи с протонами кислоты, образуя различные химические соединения. Взаимодействие кислот с неметаллами может быть очень разнообразным и включать образование интермедиатов, получение новых химических соединений и образование солей.
Взаимодействие кислот с металлами и неметаллами является важной составляющей не только в химических реакциях, но и в промышленных процессах, медицине и других областях. Это позволяет синтезировать новые материалы, проводить анализ и исследования различных веществ, а также создавать различные полезные продукты.
Взаимодействие кислот с металлами
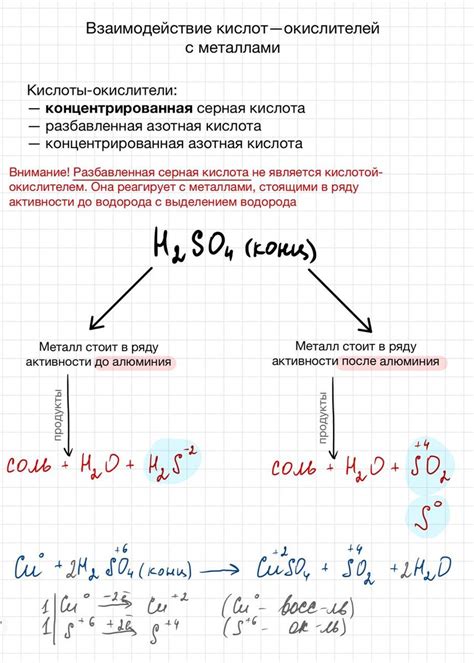
Кислоты представляют собой важный класс химических соединений, обладающих кислотными свойствами. При взаимодействии с металлами, кислоты проявляют разнообразные реакции, которые имеют большое практическое значение.
Одним из наиболее распространенных типов реакций является образование солей. Когда кислота вступает в реакцию с металлом, образуются ионные соединения, называемые солями. Например, хлороводородная кислота (HCl) реагирует с натрием (Na), образуя соль – хлорид натрия (NaCl).
Во время реакции между кислотой и металлом происходит образование водорода (H2). Образование водорода является характерным признаком реакции взаимодействия металла с кислотой. Например, при реакции меди (Cu) с серной кислотой (H2SO4) образуется серный диоксид (SO2), а также водород (H2).
Реакции взаимодействия кислот с металлами играют важную роль в промышленности и в повседневной жизни. Например, продукты реакции металлов с кислотами используются в процессе получения соединений для производства удобрений, лекарств и других химических веществ.
Кроме того, взаимодействие кислот с металлами влияет на процессы коррозии. Коррозия – это разрушение металла под воздействием окружающей среды. Некоторые кислоты, например, серная кислота, способны разрушать металлические поверхности, вызывая коррозию.
Связь между кислотами и металлами

Кислоты - это вещества, способные отдавать ионы водорода при растворении в воде. Они имеют кислотные свойства и могут реагировать с различными веществами, включая металлы.
Взаимодействие кислот с металлами происходит посредством окислительно-восстановительных реакций, в результате которых металл отдает электроны, становясь положительно заряженным ионом. В свою очередь, кислоты принимают эти электроны, превращаясь в отрицательно заряженные ионы.
Связь между кислотами и металлами обусловлена различием в электроотрицательности между ними. Металлы имеют низкую электроотрицательность и легко отдают электроны, что позволяет кислотам принять их и образовать соли. Таким образом, в результате реакции кислоты с металлами образуются соли и выделяется водород газ.
Взаимодействие кислот с металлами имеет широкое практическое применение в различных областях. Например, реакция соляной кислоты с металлическими цинком, железом или алюминием используется для получения водорода в промышленности и в лабораторных условиях. Этот процесс основан на принципе окислительного растворения металlice металла в кислотной среде.
Реакции кислот с металлами
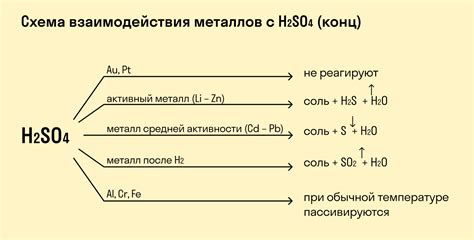
Кислоты – это вещества, которые могут образовывать положительные ионы водорода (H+) в водном растворе. Они имеют кислотные свойства и обладают способностью реагировать с различными веществами. Особый тип реакций, которые кислоты проявляют, – это реакции с металлами.
Когда кислоты реагируют с металлами, образуется соль и высвобождается водород. Реакция происходит по следующему принципу: кислота отдаёт свой протон (водородный ион) металлу, а сама трансформируется в соль. Водород, который высвобождается в результате реакции, может быть собран и использован в разных процессах.
Реакция кислот с металлами может быть разной интенсивности, в зависимости от конкретного сочетания кислоты и металла. Некоторые металлы, такие как железо и цинк, активно реагируют с кислотами, поэтому процесс может протекать быстро и взрывообразно. В то же время, другие металлы, например, золото и платина, практически не образуют реакцию с кислотами.
Реакции кислот с металлами имеют широкое применение в различных областях. Например, они используются в производстве водорода, который является важным ресурсом для производства различных химических веществ. Кроме того, эти реакции имеют применение в гальванических элементах, батареях и других устройствах, которые работают на основе химической энергии.
Взаимодействие кислот с неметаллами

Неметаллы, такие как кислород, сера, фосфор и хлор, также могут реагировать с кислотами, образуя различные соединения и проявляя химические свойства. Такие реакции, как правило, сопровождаются выделением газов или образованием кислых оксидов.
Например, реакция кислорода со соляной кислотой приводит к образованию хлористого водорода и хлоридов металлов:
- HCl + O2 → H2O + Cl2 (соляная кислота + кислород → вода + хлор)
- 2HCl + P4 → H3PO4 + 2HCl (соляная кислота + фосфор → фосфорная кислота + хлорид водорода)
Кроме того, реакция серы с кислотами может привести к образованию сульфатов и газов:
- H2SO4 + S → SO2 + H2O (серная кислота + сера → диоксид серы + вода)
- 3H2SO4 + P → H3PO4 + H2S2O7 (серная кислота + фосфор → фосфорная кислота + пированадат серы)
Таким образом, взаимодействие кислот с неметаллами является важным процессом в химии, приводящим к образованию различных соединений с участием неметаллов и демонстрирующим химические свойства данных элементов.
Связь между кислотами и неметаллами

Связь между кислотами и неметаллами обусловлена реакциями, которые происходят при контакте данных веществ. Неметаллы обладают отрицательными электронными зарядами и образуют ионы или молекулы со связями, основанными на совместном использовании электронов (координационная связь). Кислоты, с другой стороны, содержат положительно заряженные протоны и характеризуются подвижными водородными ионами (H+).
Взаимодействие кислот с неметаллами происходит путем образования реакционной смеси, в которой неметалл принимает электроны от кислоты, формируя ионы соответствующей кислоты и водорода. Например, хлорид водорода (HCl) при контакте с кислородом (O) образует воду (H2O), а хлор (Cl2) выделяется в виде газа:
- 2HCl + O → H2O + Cl2
Типичными примерами реакций между кислотами и неметаллами являются реакции с участием сероводорода (H2S), фтора (F2), хлора (Cl2), брома (Br2) и йода (I2). Например, сероводород реагирует с серной кислотой (H2SO4), образуя сульфиды металлов и воду:
- 3H2S + 2H2SO4 → 3S + 4H2O
Важным аспектом взаимодействия кислот с неметаллами является их применение в различных областях. Например, серная кислота используется в производстве удобрений, лекарств, бумаги и других химических соединений. Фторид водорода (HF) применяется в качестве едкого реагента при гравировке стекла и электронных микросхем. Реакции с неметаллами также играют ключевую роль в аналитической химии, позволяя определить наличие или концентрацию различных веществ.
Реакции кислот с неметаллами

Кислоты могут проявлять химическое взаимодействие с неметаллами, образуя различные соединения. Эти реакции могут протекать с выделением газов, образованием солей или окислением неметалла.
Одной из наиболее распространенных реакций является реакция кислот с кислородом, образующая оксиды неметаллов. Например, хлороводородная кислота реагирует с кислородом, образуя хлористый водород (хлор). Также хлорид ксения реагирует с кислородом, образуя диоксид ксения. В этих реакциях оксиды неметаллов являются кислотными оксидами, так как они реагируют с водой, образуя кислоты.
Кроме того, реакции кислот с неметаллами могут протекать с образованием газов. Например, соляная кислота реагирует с фосфором, образуя фосфорную кислоту и выделяя фосфористый водород. Азотная кислота реагирует с аммиаком, образуя аммонийнитрат и выделяя оксид азота.
В некоторых случаях реакции кислот с неметаллами могут протекать с окислением неметалла. Например, хлорная кислота окисляет сероводород до серы и хлора. А пероксид серы реагирует с нитридом амила, образуя серный диамид и выделяя кислород. В этих реакциях кислоты выступают в роли окислителей, а неметаллы – в роли восстановителей.
Вопрос-ответ

Какие металлы реагируют с кислотами?
С кислотами реагируют многие металлы, включая щелочные металлы, алюминий, цинк, железо, медь и т.д. Реакция зависит от конкретной кислоты и металла, и может варьироваться по интенсивности и скорости.
Какие реакции происходят при взаимодействии металла и кислоты?
При взаимодействии металла и кислоты может происходить разложение кислоты с образованием соли и выделением водорода. Например, при реакции цинка с соляной кислотой образуется соль цинка и газ водород.
Какие неметаллы реагируют с кислотами?
Неметаллы, такие как сера, хлор, бром и йод, могут взаимодействовать с кислотами. Например, реакция серы с кислым оксидом азота приводит к образованию азотистой кислоты.
В каких областях применяются реакции металлов с кислотами?
Реакции металлов с кислотами имеют множество применений. Например, они используются в химической промышленности для получения солей, в производстве водорода, а также в аналитической химии для определения содержания кислот в различных образцах.
