Взаимодействие кислот с активными металлами является одной из основных реакций органической химии. Кислоты обладают способностью отдавать протоны, а активные металлы, такие как натрий, калий, магний и алюминий, обладают способностью образовывать ионные связи. В результате взаимодействия кислоты и активных металлов образуются соли и выделяется водород.
Особенностью взаимодействия кислот с активными металлами является их способность активно протекать при комнатной температуре. Например, реакция серной кислоты с алюминием протекает со значительной интенсивностью и сопровождается выделением водорода. Это объясняется высокой активностью металла, который легко отдает электроны и образует комплексы с кислотой.
Примером взаимодействия кислоты с активным металлом служит реакция хлороводородной кислоты с натрием. При этом образуется хлорид натрия и выделяется водородный газ:
2HCl + 2Na → 2NaCl + H2
Также можно привести пример реакции серной кислоты с магнием, в результате которой образуется сульфат магния и выделяется водород:
H2SO4 + Mg → MgSO4 + H2
Изучение взаимодействия кислот с активными металлами имеет большое значение для понимания основных принципов реакций между веществами и развития новых методов синтеза в органической химии.
Взаимодействие кислот с активными металлами

Кислоты представляют собой химические соединения, которые обладают возможностью отдавать протоны (водородные ионы) в растворе. Активные металлы — это элементы, которые активно реагируют с другими веществами, такими как кислоты. При взаимодействии кислоты с активным металлом, происходит химическая реакция, которая может иметь различные последствия.
Одним из наиболее известных примеров взаимодействия кислоты с активным металлом является реакция соляной кислоты (HCl) с активным металлом цинком (Zn). При этой реакции между кислотой и металлом образуется соль и выделяется водородный газ:
- 2HCl + Zn → ZnCl2 + H2↑
Еще одним примером является взаимодействие серной кислоты (H2SO4) с активным металлом железом (Fe). В результате этой реакции образуется соль и выделяются два газа – диоксид серы (SO2) и водород (H2):
- H2SO4 + Fe → FeSO4 + SO2↑ + H2↑
Взаимодействие кислоты с активными металлами может протекать с выделением тепла и поглощением или выделением энергии. Кроме того, в зависимости от активности металла и кислоты, могут образовываться различные продукты реакции. Эти реакции могут иметь различное применение в химической промышленности и лабораторных исследованиях.
Особенности реакции

Взаимодействие кислот с активными металлами представляет собой химическую реакцию, которая сопровождается выделением водорода и образованием солей металлов. Основным принципом данной реакции является донорно-акцепторное взаимодействие, при котором активный металл выполняет роль акцептора электронов, а кислота – донора электронов.
В процессе взаимодействия кислоты с активными металлами происходит образование ионов металла и ионов водорода. Ионы металла образуют соли, которые растворяются в воде и могут обладать различными свойствами – быть кислыми, щелочными или нейтральными. Водород, выделяющийся в результате реакции, может образовывать газообразные пузырьки или искры.
Скорость реакции кислоты с активными металлами зависит от концентрации кислоты, температуры окружающей среды и активности металла. Чем выше концентрация кислоты и температура, тем быстрее протекает реакция. Активные металлы, такие как натрий, калий, магний, реагируют с кислотами очень интенсивно, в то время как менее активные металлы, например, цинк или свинец, реагируют медленно и нестабильно.
Примером реакции кислоты с активным металлом является реакция соляной кислоты с натрием, в результате образуется хлорид натрия и выделяется водород. Уравнение реакции имеет вид: 2HCl + 2Na → 2NaCl + H2. Эта реакция относится к типу однозамещения, при котором металл замещает водород в кислоте.
Примеры химических реакций
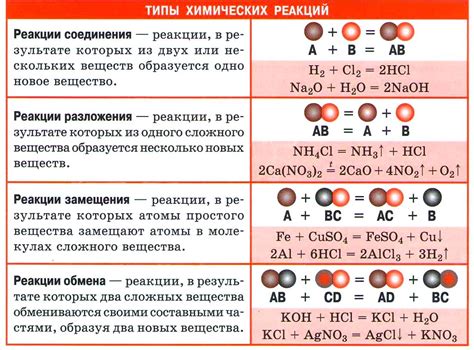
Взаимодействие кислот с активными металлами приводит к образованию солей и выделению водорода. Например, реакция между соляной кислотой (HCl) и металлом цинком (Zn):
- Соляная кислота + цинк: HCl + Zn → ZnCl₂ + H₂.
Соляная кислота реагирует с активным металлом цинком, образуя хлорид цинка и выделяя молекулы водорода.
Еще одним примером реакции между кислотой и активным металлом является реакция между серной кислотой (H₂SO₄) и металлом алюминием (Al):
- Серная кислота + алюминий: H₂SO₄ + 2Al → Al₂(SO₄)₃ + 3H₂.
В этой реакции серная кислота образует сульфат алюминия, а алюминий реагирует с кислотой, выделяя молекулы водорода.
Также, реакция между соляной кислотой и металлом железом (Fe) может выглядеть следующим образом:
- Соляная кислота + железо: 2HCl + Fe → FeCl₂ + H₂.
Здесь соляная кислота образует хлорид железа и выделяет молекулы водорода.
Вопрос-ответ

Каким образом происходит взаимодействие кислот с активными металлами?
Взаимодействие кислот с активными металлами происходит в результате образования солей и выделения водорода. Кислоты отдают протоны (водородные ионы) активным металлам, что приводит к образованию солей. При этом образовавшийся водород выделяется в виде газа.
