Кислоты являются одним из важных классов химических соединений, которые широко используются в различных отраслях промышленности и научных исследованиях. Взаимодействие металлов с кислотами является важной темой в химии и имеет большое практическое значение.
При контакте металла с кислотой происходит реакция, в результате которой образуется водородный газ (H2). Это явление известно как образование H2. Водород обладает рядом уникальных физических и химических свойств, которые делают его полезным и важным во многих отраслях промышленности.
Взаимодействие металлов с кислотами происходит благодаря различиям в ионных свойствах металлов и кислот. Металлы имеют способность отдавать электроны, образуя положительно заряженные ионы (катионы), в то время как кислоты обладают способностью принимать электроны, образуя отрицательно заряженные ионы (анионы).
Металлы и кислоты: процесс образования H2
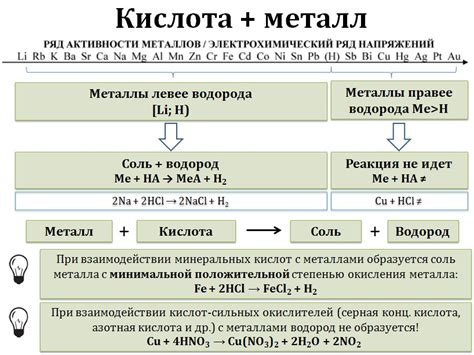
Взаимодействие металлов с кислотами является одной из основных химических реакций. При этом происходит образование молекулы водорода (H2), которая проявляет свои характерные свойства.
Когда металл вступает в реакцию с кислотой, происходит образование соли и молекулы водорода. Водород выделяется в виде газа и может быть обнаружен по его свойствам – легкость, запах и т.д. Возникший водород может быть наблюдаем в виде пузырьков, которые поднимаются из раствора на поверхность, при реакции металла с кислотой.
Этот процесс становится особенно заметным, если ученик наблюдает его с помощью "лампы Гофе". Данное устройство позволяет собирать образующийся газ в стеклянный сосуд и затем его использовать для демонстрации своих основных свойств.
Однако, не все металлы одинаково реагируют с кислотами. Некоторые металлы, такие как железо или цинк, реагируют с кислотами образованием водорода. В то же время, другие металлы, например, медь или серебро, не образуют водород при контакте с кислотами. Это связано с различием в химических свойствах материалов.
В целом, взаимодействие металлов с кислотами и образование водорода - это важный процесс, который находит широкое применение как в образовательных целях, так и в промышленности.
Как металлы взаимодействуют с кислотами?

Взаимодействие металлов с кислотами может происходить по различным механизмам и приводит к образованию водорода (H2) и соли металла. Реакция обычно начинается с образования ионов металла, которые затем реагируют с ионами водорода и анионами кислоты.
Одним из наиболее распространенных типов реакций между металлами и кислотами является "замена водорода". В этом случае ион металла вытесняет ион водорода из кислоты, образуя соль металла и молекулы водорода. Например, при взаимодействии цинка (Zn) с соляной кислотой (HCl) образуется хлорид цинка (ZnCl2) и молекулы водорода.
Взаимодействие металлов с кислотами может происходить также по другим механизмам. Например, некоторые металлы реагируют с кислотами через окислительно-восстановительные реакции, при которых металл окисляется, а ион водорода восстанавливается. Это особенно характерно для сильных окислителей, таких как концентрированная серная кислота.
В результате взаимодействия металлов с кислотами образуется газ водород (H2), который можно обнаружить, например, посредством появления пузырей или использования газообразных пробирок. Кроме того, образование солей металла является еще одним признаком реакции металлов с кислотами.
Каталитическая реакция и образование H2
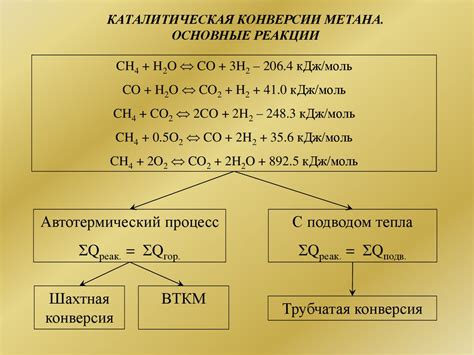
Образование молекулярного водорода (H2) при взаимодействии металлов с кислотами несомненно является каталитической реакцией. Каталитический процесс означает, что металлы не потребляются в реакции, а лишь ускоряют протекание химической реакции. Они действуют как катализаторы, позволяя более эффективно протекать процессу образования водорода.
Основным механизмом каталитической реакции между металлами и кислотами является обмен электронами. Металлы, обладая свободными электронами, могут служить донорами электронов для кислорода в кислоте, что позволяет производить водород. Этот процесс позволяют увеличить скорость реакции, так как электронный обмен становится значительно более эффективным.
Образование H2 при взаимодействии металлов с кислотами может быть проиллюстрировано на примере реакции цинка (Zn) с соляной кислотой (HCl). При данной реакции происходит освобождение молекулярного водорода. Каталитическая роль цинка заключается в том, что он способствует расщеплению молекул HCl на ионы H+ и Cl-. Затем, свободные электроны цинка образуют ковалентные связи с H+ и способствуют образованию молекулярного водорода.
Таким образом, каталитическая реакция между металлами и кислотами играет важную роль в образовании молекулярного водорода. Методы данной реакции находят широкое применение в промышленности и научных исследованиях, благодаря своей эффективности и экономической выгодности.
Свойства и применение H2, полученного из взаимодействия металлов и кислот
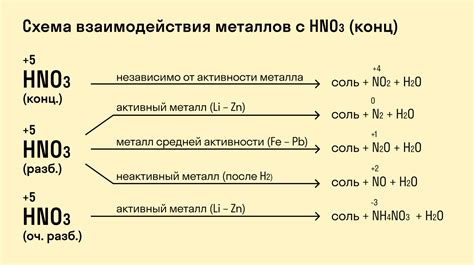
Свойства H2:
- Водород (H2) - легкий, без цвета, безвкусный и газообразный элемент.
- Обладает низкой плотностью и высокой теплопроводностью.
- Состоит из двух атомов, связанных ковалентной связью.
- Является высокоинфламмабельным и может гореть в воздухе, образуя воду.
- H2 обладает высокой энергетической плотностью и используется в качестве топлива водородных элементов.
Применение H2:
- Водород широко используется в промышленности, особенно в процессах синтеза аммиака, метанола и других химических веществ.
- Используется как газовое топливо для ракет и автомобилей с водородными топливными элементами, так как его сгорание не производит углекислый газ.
- Играет важную роль в производстве пищевых продуктов, таких как растительные масла и жиры.
- Широко применяется в процессах нейтрализации, так как взаимодействие H2 с кислотами образует воду.
- Используется в процессах водородации для получения различных химических соединений, таких как жирные кислоты и аминокислоты.
Заключение:
H2, полученный из взаимодействия металлов и кислот, обладает рядом уникальных свойств и имеет широкие области применения. Его низкая плотность и высокая энергетическая плотность делают его привлекательным источником энергии. Кроме того, H2 играет важную роль в производстве множества химических веществ и пищевых продуктов. Взаимодействие H2 с кислотами также является значимым процессом в производстве и в области нейтрализации.
Вопрос-ответ

Какое взаимодействие происходит между металлами и кислотами?
Когда металлы вступают в реакцию с кислотами, происходит образование водорода (H2) и соответствующих солей металлов.
Каков механизм образования водорода при взаимодействии металлов с кислотами?
Механизм образования водорода при реакции металлов с кислотами основан на способности кислоты отдавать протоны (H+) металлу, который тем самым окисляется, а ион водорода (H+) восстанавливается, образуя молекулы водорода (H2).
