В химии имеется ряд различных кислот, которые могут взаимодействовать с металлами. Эта взаимодействие происходит в результате окисления металла и образования солей. Однако, не все металлы обладают одинаковой активностью при контакте с кислотами. Существует так называемый ряд активности металлов, который определяет их способность реагировать с различными кислотами.
На верхней части ряда активности находятся самые активные металлы, такие как алюминий, цинк и железо. Эти металлы могут взаимодействовать даже с очень слабыми кислотами, такими как уксусная кислота. При контакте с кислотой, металл окисляется, а в результате образуется соль и выделяется водород.
В середине ряда активности находятся металлы, такие как медь и серебро. За исключением некоторых кислот, эти металлы не реагируют с большинством кислот. Они могут реагировать только с более сильными кислотами, такими как азотная или серная кислоты.
В нижней части ряда активности находятся самые неподвижные металлы, такие как золото и платина. Они не реагируют с практически любыми кислотами, включая сильные кислоты, такие как хлороводородная или серная кислоты.
Взаимодействие кислот с металлами: ряд активности металлов

Металлы могут вступать в реакцию с кислотами, проявляя различную активность в зависимости от своих химических свойств. Для классификации металлов по степени активности существует ряд активности металлов.
В ряду активности металлов металлы располагаются по убыванию их способности вступать в реакцию с кислотой. На самом активном конце ряда находятся щелочные металлы, такие как натрий и калий. Они обладают высокой активностью и способны быстро реагировать с кислотами, выделяя водородный газ.
Более низкой активностью обладают металлы, которые вступают в реакцию только с определенными кислотами и не активны с другими типами кислот. Примерами таких металлов являются цинк и алюминий.
Наиболее низкую активность проявляют металлы, которые не вступают в реакцию с кислотами при обычных условиях. К таким металлам относятся золото, серебро и платина.
Взаимодействие кислот с металлами носит ионообменный характер. Металлы отдают электроны кислоте, образуя положительно заряженные ионы, а кислота получает электроны, превращаясь в отрицательно заряженный ион. Этот процесс сопровождается выделением водорода и образованием соответствующих солей.
Кислоты и их роль в химических реакциях

Кислоты – это химические соединения, которые обладают кислотными свойствами и способны отдавать протоны или принимать электроны. Они играют важную роль в химических реакциях благодаря своей активности и способности взаимодействовать с различными веществами.
Кислоты могут участвовать в различных реакциях, таких как нейтрализация, окисление-восстановление и гидролиз. Нейтрализация – это химическая реакция, при которой кислота реагирует с основанием и образует соль и воду. В процессе окисления-восстановления кислота может окислять другие вещества и в то же время сама восстанавливаться. Гидролиз – это реакция с разделением воды на ионы.
В химических реакциях кислоты проявляют свою активность, играют роль катализаторов или реагентов. Кислоты могут проводить протонный транспорт и обладают свойствами ацетилирования, аминирования, эфирирования и другими. Они также являются важными компонентами в процессе синтеза органических и неорганических веществ.
Благодаря своей активности кислоты могут взаимодействовать с различными металлами. В результате этого взаимодействия образуются соли, газы и вода. Реакция между кислотами и металлами осуществляется путем передачи электронов. Кислоты отдают протоны, а металлы принимают электроны, что приводит к образованию ионов и выделению газа.
Что такое ряд активности металлов и зачем он нужен

Ряд активности металлов – это упорядоченный список металлов в порядке их активности, то есть способности вступать в химические реакции с кислотами. Он показывает, какие металлы более активны, а какие менее активны.
Ряд активности металлов необходим для определения возможности взаимодействия металла с кислотой. Металлы, находящиеся выше в ряду, считаются более активными и способными замещать металлы, находящиеся ниже в ряду из соединений с кислотами. Это позволяет предсказывать результаты химических реакций и определять, какой металл реагирует с кислотой с образованием соли и выделением водорода.
В ряд активности металлов входят металлы различной активности, начиная с самых активных (например, литий, натрий, калий) и заканчивая наименее активными (например, медь, серебро, золото). Такой ряд активности металлов позволяет предсказывать, будет ли происходить реакция между металлом и кислотой и какого вида будет образовавшаяся в результате реакции соль.
Как работает ряд активности металлов в реакциях с кислотами

Ряд активности металлов представляет собой упорядоченный список металлов в порядке их реакционной активности с кислотами. Чем выше металл в ряду, тем большую активность он проявляет в реакциях с кислотами. Этот ряд позволяет предсказывать, какой металл будет активнее реагировать с данной кислотой.
Металлы, расположенные выше в ряду активности, обладают большим склонностью отдавать электроны и образовывать положительные ионы. Это связано с их более низкими значениями электроотрицательности. Когда металл реагирует с кислотой, он вытесняет из нее водород, образуя соответствующую соль и выделяя газ водород.
На реакции металлов с кислотами влияет их реакционная активность, их плотность, а также концентрация и свойства кислоты. Например, при использовании различных кислот, может происходить различная степень реакции с металлами, и эта степень может изменяться в зависимости от концентрации.
Ряд активности металлов позволяет проводить различные химические эксперименты, определять активность металлов, выбирать подходящие металлы для различных промышленных процессов, а также предсказывать возможность реакции между металлом и кислотой. Этот ряд является важным инструментом в изучении реакций металлов с кислотами и их применении в различных областях науки и техники.
Примеры реакций металлов с кислотами в соответствии с рядом активности
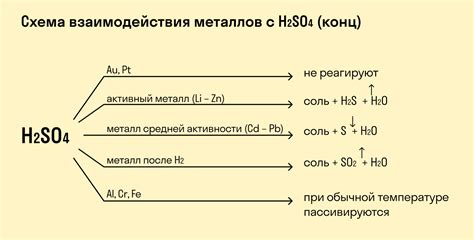
Реакция металлов с кислотами является одним из распространенных видов химических превращений. Она основывается на способности металлов отдавать электроны и образовывать ионы. Основным фактором, влияющим на скорость и степень реакции, является ряд активности металлов – упорядоченный список металлов в порядке возрастания их активности.
Согласно ряду активности, металлы, находящиеся выше в списке, реагируют с кислотами более активно, чем металлы, расположенные ниже. Например, щелочные и щелочноземельные металлы, такие как натрий, калий, магний и кальций, быстро реагируют с различными кислотами, образуя соли и выделяя водородный газ.
Другими примерами реакций металлов с кислотами являются реакции алюминия и цинка с соляной кислотой. При взаимодействии этих металлов с соляной кислотой, образуются соответствующие соли и выделяется водород.
Реакции металлов с кислотами играют важную роль в различных областях, таких как промышленность, наука и повседневная жизнь. Например, реакция цинка с серной кислотой применяется в батарейках, а реакция алюминия с соляной кислотой используется в производстве различных химических соединений и материалов.
Применение знаний о ряде активности металлов в промышленности

Знание ряда активности металлов позволяет применять его в различных областях промышленности. Одной из таких областей является химическая промышленность, где знание ряда активности металлов позволяет определить возможность совместного взаимодействия металла с кислотами. Благодаря этому знанию, можно выбрать подходящий металл для производства химических реактивов, катализаторов и других продуктов.
Производство электроники также основывается на знании о ряде активности металлов. Зная, какие металлы могут быть использованы в контактах и проводах, можно выбрать оптимальные материалы для создания схем электронных устройств. Это важно для обеспечения надежного и безопасного функционирования устройства.
Ряд активности металлов также используется в гальванике и металлообработке. Гальваническое покрытие металлом позволяет улучшить его свойства, например, обеспечить защиту от коррозии или придать декоративный вид. Знание о ряде активности металлов помогает выбрать правильную последовательность покрытия и обеспечивает высокое качество покрытия.
- Химическая промышленность
- Производство электроники
- Гальваника и металлообработка
Вопрос-ответ

Каким образом кислоты взаимодействуют с металлами?
Кислоты могут реагировать с металлами, образуя соли и выделяя водород. В реакции кислоты с металлами происходит передача электронов между ионами, что позволяет кислоте и металлу достичь более устойчивых состояний.
Что такое ряд активности металлов?
Ряд активности металлов - это список металлов, упорядоченных по возрастанию их активности. Чем выше металл на ряду активности, тем более активным он является. Ряд активности металлов позволяет предсказывать, будет ли данное металл реагировать с кислотой и как интенсивно будет протекать эта реакция.
Какие металлы реагируют с кислотами?
Металлы могут быть активными или пассивными. Самые активные металлы, например натрий или калий, реагируют с водой и кислотами. Менее активные металлы, такие как железо или медь, могут реагировать только с некоторыми кислотами в определенных условиях. Пассивные металлы, такие как золото или платина, обычно не реагируют с кислотами.
