Одной из важных характеристик химических реакций металлов является их способность вступать в реакцию с кислородом. Этот процесс называется оксидацией металла и приводит к образованию металлического оксида. Реакция оксидации металлов является основой для получения множества материалов с различными физическими и химическими свойствами.
Оксиды металлов представляют собой химические соединения, состоящие из металла и кислорода. Эти соединения обладают различными свойствами и находят широкое применение в различных областях науки и промышленности. Металлические оксиды могут быть как ионными или ковалентными веществами, что определяет их физические и химические свойства.
Реакция оксидации металлов с кислородом происходит при взаимодействии металла с кислородом воздуха или специальными реагентами. В результате этой реакции на поверхности металла образуется слой оксида, который может быть тонким и непроницаемым для дальнейшей окислительной реакции или же толстым и пористым, что способствует продолжению процесса окисления.
Металлы и их взаимодействие с кислородом
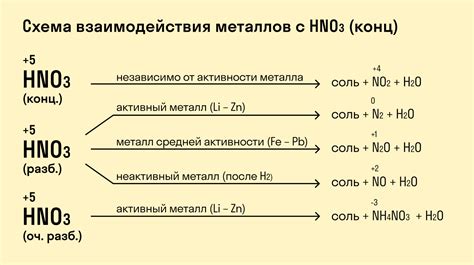
Металлы - это группа химических элементов, обладающих свойством проводить электрический ток и имеющих блеск. Одной из важных характеристик металлов является их способность взаимодействовать с кислородом.
Реакция металлов с кислородом называется окислительно-восстановительной, так как металлы окисляются при контакте с кислородом. В результате этой реакции образуются металлические оксиды, которые обладают своими уникальными свойствами.
Оксиды металлов имеют различные физические и химические свойства. Некоторые из них, например, железный оксид или алюминиевый оксид, обладают красивыми цветами и могут использоваться в производстве красок и косметики.
Существует также набор реакций, которые могут происходить с участием оксидов металлов. Например, оксиды могут реагировать с кислотами, образуя соли и воду. Также они могут быть использованы в процессе производства стекла, керамики и катализаторов.
Взаимодействие металлов с кислородом имеет не только химическую, но и практическую значимость. Знание свойств оксидов металлов позволяет эффективно использовать их в различных областях промышленности и науки.
Оксидация металлов: научное объяснение

Оксидация металлов является процессом, при котором металлические элементы реагируют с кислородом и образуют оксиды. Оксиды металлов имеют различную степень окисления и химические свойства в зависимости от своего состава.
Оксидация металлов осуществляется через взаимодействие металла с кислородом в воздухе или воде. Под воздействием кислорода на поверхности металла образуется пленка оксида, которая защищает его от дальнейшей окисления. Эта пленка обычно препятствует проникновению кислорода внутрь металла и помогает сохранить его структуру и свойства.
Однако, некоторые металлы могут продолжать реагировать с кислородом при повышенной температуре или в интенсивной окружающей среде. Например, железо реагирует с кислородом при высоких температурах, образуя железную ржавчину или окись железа.
Оксиды металлов широко используются в промышленности и научных исследованиях, так как они обладают разнообразными свойствами и могут быть использованы в различных процессах, таких как катализ и производство керамики. Некоторые оксиды металлов, такие как оксид цинка и оксид титана, обладают полезными свойствами, такими как проводимость или устойчивость к высоким температурам, и используются в электронике и космической промышленности.
Процесс оксидации металлов: типичные реакции

Оксидация металлов представляет собой химическую реакцию, при которой металлический элемент соединяется с кислородом. Такие реакции являются типичными и характерными для многих металлов.
Одним из наиболее известных примеров реакции оксидации металлов является процесс образования ржавчины на поверхности железа. При взаимодействии с кислородом воздуха, железо окисляется, образуя оксид железа (III). Этот оксид имеет красную окраску, что и придает ржавчине такой характерный цвет.
Другой пример реакции оксидации металлов – образование опасного вещества – оксида нитрогена (IV). При взаимодействии металлического азида с кислородом, металл окисляется, образуя оксид нитрогена (IV), который является сильным окислителем.
Некоторые металлы окисляются очень быстро и реакция с кислородом происходит взрывоопасно. Например, калий, который находится в непосредственной близости к кислороду, может образовать яркую вспышку и сильный шум при попадании воздуха.
Также стоит отметить, что оксидация металлов может протекать не только в воздухе при комнатной температуре, но и при высоких температурах, водородной или кислотной среде. В результате таких реакций образуется широкий спектр металлических оксидов с различными свойствами и структурами.
Коррозия металлических оксидов: последствия и причины

Металлы, будучи подвержены воздействию кислорода, образуют металлические оксиды. К сожалению, эти оксиды могут подвергаться коррозии, что может привести к серьезным последствиям. Коррозия металлических оксидов происходит из-за реакции окисления, при которой электроны отделяются от металла и переходят на кислород. Это может происходить под воздействием воды, влаги или других агрессивных веществ.
Одной из причин коррозии металлических оксидов является наличие влаги или воды, так как они обеспечивают среду для реакции окисления. Вода служит электролитом, а окисление и восстановление происходят на поверхности металлического оксида. Кроме того, коррозию могут вызывать и другие вещества, например, кислоты или щелочи, которые усиливают процесс окисления металла.
Последствия коррозии металлических оксидов могут быть разнообразными и вполне серьезными. Одним из наиболее очевидных последствий является образование ржавчины на поверхности металла. Ржавчина может привести к разрушению металлической конструкции или повреждению изделия. Кроме того, коррозия может вызывать потерю металла, что снижает его прочность и стабильность. Это может быть особенно опасно в случае конструкций или механизмов, которые работают под нагрузкой.
Для предотвращения коррозии металлических оксидов необходимо принимать меры по защите металла от воздействия окрислителя. Одним из способов является нанесение защитных покрытий на поверхность металла, которые могут предотвратить доступ кислорода и воды. Также важно избегать контакта металла с агрессивными средами, такими как кислоты или щелочи. Регулярное обслуживание и очистка металлических конструкций также помогут предотвратить коррозию и сохранить их долгий срок службы.
Влияние оксидации на свойства металлов
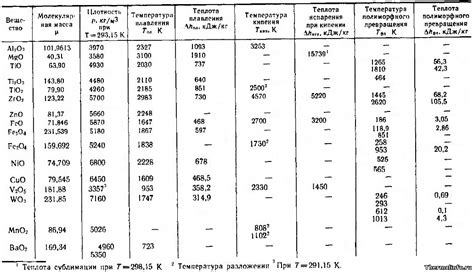
Металлы подвержены оксидации, процессу взаимодействия металлических веществ с кислородом. Оксидация может привести к изменению свойств металлов, включая их химическую активность, физическую мощность и термическую стойкость.
Одним из результатов оксидации металлов является образование оксидов. Оксиды металлов могут иметь различные физические и химические свойства, которые зависят от специфической структуры, состава и способа синтеза.
Некоторые металлические оксиды проявляют полупроводниковые свойства, что делает их важными материалами для электроники, в частности в производстве транзисторов, светодиодов и солнечных батарей. Другие оксиды имеют магнитные свойства и находят применение в производстве магнитных материалов.
- Оксидация металлов может привести к их коррозии, что может ухудшить их механические свойства и снизить их долговечность. Это особенно актуально для металлов, используемых в строительстве, автомобильной промышленности и производстве бытовых приборов.
- Оксидация металлов может также повысить их плавность и улучшить способность к обработке, обеспечивая более высокое качество и точность изготовления металлических изделий.
Оксидация металлов может влиять на их химическую реактивность и способность взаимодействовать с другими веществами. Например, оксидированные металлы могут проявлять более интенсивную реакцию с кислородом и образовывать с трудом растворимые соединения, что может быть использовано в процессах очистки воды и воздуха.
Предотвращение оксидации металлических оксидов

Оксидация металлических оксидов может привести к их разрушению и потере свойств. Важно предотвратить этот процесс, чтобы сохранить целостность и функциональность материалов.
Одним из способов предотвращения оксидации является нанесение защитного покрытия на поверхность металлического оксида. Это может быть покрытие из полимеров, эмали или металлических слоев. Защитное покрытие создает барьер между металлическим оксидом и внешней средой, предотвращая доступ кислорода и других окислительных веществ.
Другим методом предотвращения оксидации является изменение условий окружающей среды. Например, можно снизить концентрацию кислорода в окружающей атмосфере или увеличить содержание инертных газов, таких как азот или аргон. Это позволяет уменьшить окислительные свойства окружающей среды и предотвращает процессы окисления металлического оксида.
Также важным методом предотвращения оксидации является правильное хранение и эксплуатация металлических оксидов. Они должны быть защищены от воздействия влаги, кислот и других окислительных сред. При необходимости, металлический оксид может быть хранен в инертной атмосфере или упакован в специальные контейнеры, обеспечивающие его сохранность.
И наконец, важно регулярно проводить осмотр и обслуживание металлических оксидов, чтобы своевременно обнаружить и устранить признаки оксидации. Это позволит сохранить эстетический вид, физические и химические свойства материала, а также продлить его срок службы.
Применение металлических оксидов в технологиях и промышленности
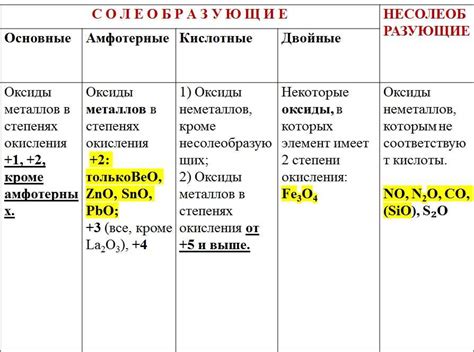
1. Катализаторы. Металлические оксиды широко применяются в качестве катализаторов в различных химических процессах. Например, оксиды цинка и оксиды железа используются в производстве синтетических волокон, пластмасс и лаков. Оксид церия применяется в катализе восстановления, а оксиды вольфрама и молибдена используются в процессах гидрогенирования и окисления.
2. Электроды для аккумуляторов. Многие металлические оксиды, такие как оксид никеля и оксид кобальта, используются для создания электродов в аккумуляторах. Они обладают высокой электропроводимостью и способностью к химической стабильности, что делает их эффективными материалами для хранения и высвобождения электрической энергии.
3. Керамика и стекло. Металлические оксиды, такие как оксид алюминия, оксид кремния и оксид титана, используются в производстве керамических и стеклянных изделий. Они придают им прочность, термостабильность и оптические свойства. Например, оксид титана используется для создания пигментов, которые придают красоту и яркость керамическим и стеклянным изделиям.
4. Конденсаторы. Некоторые металлические оксиды, включая оксид алюминия и оксид цинка, используются в производстве конденсаторов. Они служат диэлектрическими материалами, способными хранить и высвобождать электрическую энергию. Благодаря своей высокой электроизоляционной способности и стабильности, металлические оксиды играют важную роль в современной электронике и информационных технологиях.
5. Покрытия. Металлические оксиды могут быть использованы в качестве покрытия для улучшения химической стойкости и долговечности материалов. Например, оксид алюминия может быть нанесен на поверхность металла для защиты его от окисления и коррозии. Оксид цинка используется в качестве антикоррозионного покрытия для поверхности стали, чтобы предотвратить ее ржавление.
В заключение, металлические оксиды играют важную роль в различных технологиях и промышленности. Они применяются в качестве катализаторов, электродов для аккумуляторов, материалов для керамики и стекла, диэлектриков для конденсаторов, а также покрытий, обеспечивающих защиту материалов от окисления и коррозии.
Вопрос-ответ

Какие металлы реагируют с кислородом?
С кислородом реагируют различные металлы, включая щелочные металлы (натрий, калий), щелочноземельные металлы (магний, кальций), переходные металлы (железо, медь), а также некоторые благородные металлы (золото, платина).
Какова реакция металлов с кислородом?
Реакция металлов с кислородом называется окислением. В результате этой реакции металлы образуют металлические оксиды. Например, магний реагирует с кислородом, образуя оксид магния (MgO). Железо реагирует с кислородом, образуя оксид железа (Fe2O3).
