Металлы являются одними из наиболее распространенных и важных элементов химического периодического закона. Они обладают высокой электропроводностью, теплопроводностью и механической прочностью, а также широко используются в различных отраслях промышленности. Кислород, в свою очередь, является необходимым элементом для поддержания жизни на Земле и играет ключевую роль во многих химических процессах.
Однако, не все металлы взаимодействуют с кислородом одинаковым образом. Наибольшую склонность к реакциям с кислородом проявляют активные металлы, такие как алюминий, калий, магний и натрий. При взаимодействии с кислородом они образуют оксиды, которые могут быть как прочными и стойкими соединениями, так и нестабильными и легко разрушаемыми веществами.
Однако, есть один металл, который не вступает в реакцию с кислородом - это золото. Золото является одним из самых инертных металлов и долгое время считалось символом богатства и роскоши. Благодаря своей инертности, золото не окисляется на воздухе и не подвержено коррозии, что делает его идеальным материалом для изготовления ювелирных изделий и электронных компонентов.
Реакции кислорода с металлами
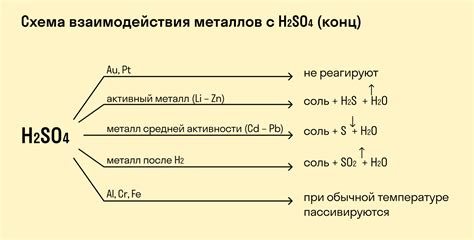
Кислород проявляет широкую реакционную способность с металлами. Одной из наиболее известных реакций является горение, или окисление, металлов в присутствии кислорода. При этом происходит выделение тепла и образование оксидов металлов.
Также кислород может реагировать с металлами, образуя перекиси. Например, реакция активных щелочных металлов с кислородом приводит к образованию перекисей, которые обладают высокой реакционной способностью. Перекиси металлов могут использоваться в различных областях, включая медицину и промышленность.
Некоторые металлы способны образовывать с кислородом стабильные оксиды. Например, алюминий образует защитную пленку оксида, которая предотвращает дальнейшую реакцию металла с кислородом. Этот феномен называется пассивацией. Пассивированные металлы обладают повышенной стойкостью к окислению и используются в различных промышленных процессах и конструкциях.
Интересным примером реакции кислорода с металлами является образование окалинного образования на поверхности железа при его окислении воздухом. Окалина представляет собой сложное соединение оксида железа с различными примесями. Она образует тонкую пленку на поверхности металла, которая может иметь защитное или порчащее действие в зависимости от условий эксплуатации.
В целом, взаимодействие кислорода с металлами является важным процессом и находит широкое применение в различных областях науки и промышленности. Изучение этих реакций помогает лучше понять поведение и свойства металлов и применять их на практике более эффективно.
Кислород и составление химических соединений
Кислород - один из наиболее активных химических элементов, способный образовывать широкий спектр соединений с другими элементами. Он имеет электроотрицательность и сильно стремится принять электроны от других элементов, что позволяет ему образовывать стабильные химические связи.
При взаимодействии с большинством металлов кислород образует оксиды, которые могут иметь различные степени окисления. Эти оксиды играют важную роль в общей химии и имеют различные свойства и применения.
Кислород также может образовывать озоны, перекиси и другие соединения с металлами, которые имеют особые свойства и могут использоваться в различных областях науки и технологий.
Процесс образования химических соединений между кислородом и металлами может быть описан с использованием химических уравнений, которые показывают, какие реакции происходят между исходными веществами и какие продукты образуются.
Некоторые металлы, такие как золото и платина, обладают высокой устойчивостью к взаимодействию с кислородом и не образуют стабильных соединений с ним. Однако большинство других металлов, таких как железо, алюминий, медь и цинк, образуют различные оксиды и другие соединения с кислородом при наличии подходящих условий.
- Одним из примеров реакции кислорода с металлом является образование оксида железа Fe2O3, который является основным компонентом ржавчины.
- Еще одним примером является образование оксида алюминия Al2O3, который обладает высокой термической стабильностью и используется в производстве керамики и рефракторов.
Факторы, влияющие на взаимодействие кислорода и металлов
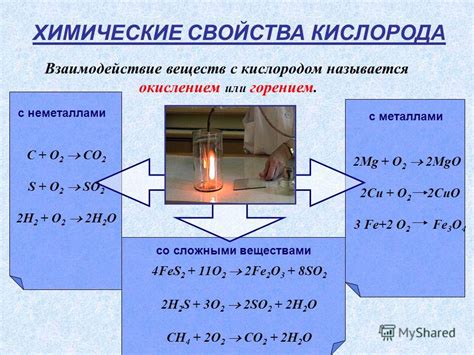
Взаимодействие кислорода с металлами является сложным процессом, который может быть оказан влияние различными факторами.
Во-первых, характер и структура металла играют важную роль в этом процессе. Кристаллическая решетка металла, его поверхностные свойства и межатомные взаимодействия могут влиять на скорость и интенсивность окисления.
Во-вторых, температура окружающей среды имеет значительное значение. При повышенной температуре обратная реакция, т.е. восстановление оксида металла, может протекать более интенсивно. Однако низкие температуры также могут способствовать ускорению окисления, например, за счет растворения кислорода в металлической матрице.
Окружающая среда также влияет на процесс окисления металлов. Наличие влаги или коррозионно-активных веществ, таких как кислоты или соли, может значительно ускорить процесс окисления. Это связано с образованием электролитических пар, которые способствуют растворению металла и проведению электронного тока.
Наконец, сами металлы имеют разную реакционную способность. Некоторые металлы более склонны к окислению, такие как железо и алюминий, в то время как другие металлы могут образовывать защитные пленки оксидов, такие как алюминий и цинк, которые помогают предотвратить дальнейшую окисляющую реакцию.
Итак, факторы, влияющие на взаимодействие кислорода и металлов, включают структуру и характер металла, температуру окружающей среды, окружающую среду и реакционную способность металла. Понимание этих факторов позволяет контролировать процесс окисления металлов и предотвращать разрушение металлических конструкций или изделий.
Альтернативные взаимодействия металлов с элементами окружающей среды

Кроме взаимодействия металлов с кислородом, существуют и другие альтернативные взаимодействия, которые могут привести к различным химическим реакциям и образованию соединений.
Одним из таких взаимодействий является реакция металлов с водой. Некоторые металлы, такие как натрий и калий, являются очень активными и реагируют с водой с образованием соответствующих гидроксидов и выделением водорода. Это реакция электролитического окисления металла водой.
Другой тип взаимодействия металлов с элементами окружающей среды - это реакция с кислотами. Многие металлы могут реагировать с кислотами, образуя соли и высвобождая водород. Например, цинк реагирует с соляной кислотой, образуя хлорид цинка и выделяя водород. Это реакция обмена.
Интересным типом взаимодействия является реакция металлов с аммиаком. Некоторые металлы, такие как медь и серебро, могут образовывать аммониакаты - сложные соединения с аммиаком. Это реакция координационной химии, где металлы формируют комплексы с аммиаком.
Также стоит упомянуть о взаимодействии металлов с солями. Некоторые металлы могут образовывать сложные соединения с солями, такие как карбонаты или фосфаты. Например, кальций может образовывать карбонат кальция, который является основным компонентом мрамора. Это реакция нейтрализации.
Вопрос-ответ

Как кислород взаимодействует с металлами?
Когда кислород взаимодействует с металлом, происходит окисление металла. Это реакция окисления, которая приводит к образованию оксида металла.
Какие металлы взаимодействуют с кислородом?
Практически все металлы могут взаимодействовать с кислородом. Однако, активные металлы, такие как натрий, калий и цинк, сильнее реагируют с кислородом и могут гореть на воздухе.
Что происходит при взаимодействии кислорода с алюминием?
При взаимодействии кислорода с алюминием образуется оксид алюминия (Al2O3). Этот оксид образует защитную пленку на поверхности алюминия, которая предотвращает дальнейшее окисление металла.
Может ли взаимодействие кислорода с металлами привести к коррозии?
Да, взаимодействие кислорода с некоторыми металлами, такими как железо, может привести к коррозии. Когда железо окисляется, образуется ржавчина, которая разрушает металл.
