Катионы металлов и анионы кислотных остатков являются основными составляющими химических соединений и играют важную роль во многих процессах, происходящих как в природе, так и в промышленности. Катионы металлов обладают положительным зарядом и являются основными ионами металлов, в то время как анионы кислотных остатков имеют отрицательный заряд и являются производными от кислотных молекул.
Свойства катионов металлов определяются их атомным радиусом, зарядом ядра и электронной конфигурацией. Катионы могут образовывать сложные соединения с анионами кислотных остатков, включая соли и кислоты. Взаимодействие между катионами и анионами обычно происходит на основе электростатических сил притяжения, где заряды противоположного знака привлекаются друг к другу.
Катионы металлов и анионы кислотных остатков могут также образовывать комплексы, где катион координируется с атомами кислотного остатка. Такие комплексы имеют важное значение в координационной химии и могут обладать разнообразными свойствами, включая антиоксидантные, каталитические и биологические.
Катион металла и анион кислотного остатка: основные свойства и взаимодействия

Катион металла - это положительно заряженная частица, которая образуется при потере одного или нескольких электронов. Катионы металлов имеют своеобразные свойства, такие как металлический блеск, проводимость электричества и тепла, а также способность образовывать ионы в растворах и вступать в химические реакции.
Анион кислотного остатка - это отрицательно заряженная частица, которая образуется при приобретении одного или нескольких электронов. Анионы кислотных остатков имеют свои собственные характеристики, такие как способность образовывать кислоты, реагировать с основаниями и другими химическими соединениями, а также участвовать в образовании солей.
Взаимодействия между катионами металлов и анионами кислотных остатков играют важную роль во многих химических процессах. Катионы и анионы могут притягиваться друг к другу благодаря электростатическим силам, образуя ионные связи. Такие ионные соединения часто обладают высокой стабильностью и являются основой для многих минералов и солей.
Более сложные взаимодействия катионов металлов и анионов кислотных остатков происходят в растворах и в реакционных средах. Некоторые катионы и анионы могут образовывать комплексы, когда катион образует координационные связи с анионом через общие электроны. Такие комплексы имеют важное значение в координационной химии и могут обладать различными свойствами, такими как расцветка, магнитные свойства и катализаторы химических реакций.
Свойства катионов металла
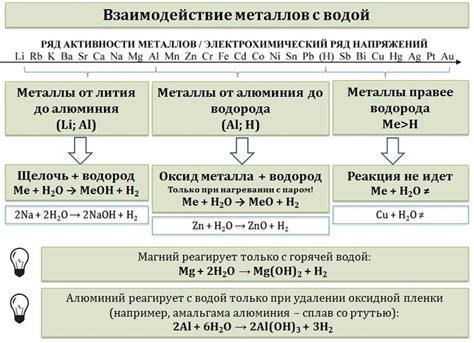
Катионы металла представляют собой положительно заряженные ионы, которые обладают рядом характерных свойств. Одно из главных свойств катионов металла - их способность образовывать растворы, в которых они подвижны и могут претерпевать различные химические реакции.
Катионы металла также имеют определенную массу и заряд, которые влияют на их поведение в химических реакциях. Например, чем больше заряд катиона, тем более сильно он притягивается к отрицательно заряженным частицам, таким как анионы кислотного остатка.
Еще одним важным свойством катионов металла является их способность образовывать координационные соединения с молекулами, содержащими анионы кислотного остатка. В этом случае катионы металла окружаются молекулами растворителя или другими лигандами, которые стабилизируют координационное соединение и увеличивают его устойчивость.
Кроме того, катионы металла могут образовывать соединения с анионами кислотного остатка, которые характеризуются различной степенью силы связи между ионами. Некоторые катионы металла образуют сильные связи с анионами и обладают высокой устойчивостью, в то время как другие металлы могут образовывать более слабые связи и иметь меньшую устойчивость в соединениях с анионами.
Свойства анионов кислотного остатка

Анионы кислотного остатка обладают рядом свойств, которые определяют их важную роль в химических реакциях и взаимодействиях с другими веществами.
Во-первых, анионы кислотного остатка могут быть одновременно электронно-донорными и электроотрицательными, что позволяет им активно участвовать в реакциях с катионами металлов. Этот электронно-акцепторный характер позволяет анионам кислотного остатка образовывать ионы солей и металлоорганических соединений.
Во-вторых, анионы кислотного остатка могут образовывать силные связи с положительно заряженными атомами или молекулами. Это свойство определяет их способность к образованию сильных ковалентных или ионных связей и катализировать различные химические реакции.
Другим важным свойством анионов кислотного остатка является их способность к образованию сложных соединений с металлами. Это свойство позволяет использовать анионы кислотного остатка в процессе синтеза новых материалов с определенными физическими и химическими свойствами.
В заключение, анионы кислотного остатка активно взаимодействуют с другими веществами и стимулируют различные химические реакции благодаря своим электронным и структурным свойствам.
Взаимодействие катионов металла и анионов кислотного остатка

Взаимодействие катионов металла и анионов кислотного остатка представляет собой важную химическую реакцию, которая обусловливает множество физических и химических свойств металлических соединений. Катионы металла и анионы кислотного остатка вступают в электростатическое взаимодействие, которое определяет степень и характер реакции.
Катионы металла обладают положительным зарядом и имеют способность притягивать анионы кислотного остатка. Это взаимодействие основано на электростатических силовых полях, которые возникают между заряженными частицами. Часто катионы металла и анионы кислотного остатка образуют ионные связи, при которых положительно заряженный катион притягивает отрицательно заряженный анион.
Взаимодействие катионов металла и анионов кислотного остатка имеет важные последствия для свойств соединений. Например, оно определяет растворимость соединений в различных растворителях. Если взаимодействие между катионом металла и анионом кислотного остатка сильное, то соединение будет хорошо растворяться в воде или других поларных растворителях. Если же взаимодействие слабое, то соединение будет слабо растворяться или вообще оставаться нерастворимым.
Взаимодействие катионов металла и анионов кислотного остатка также влияет на химические реакции соединений. Оно может способствовать образованию новых соединений, растворению или осаждению веществ. Кроме того, взаимодействие катионов и анионов определяет физические свойства соединений, такие как температура плавления и кипения, проводимость электрического тока и другие характеристики.
Роль катионов металла и анионов кислотного остатка в химических реакциях
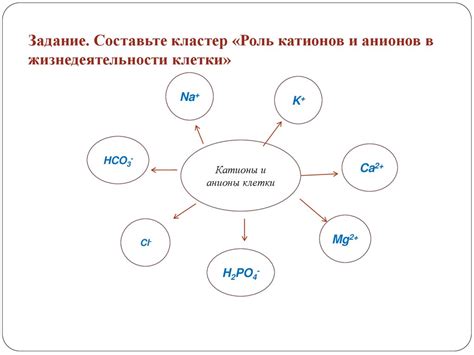
Катион металла и анион кислотного остатка играют важную роль в химических реакциях, так как влияют на их характер и процесс протекания. Катионы металла и анионы кислотного остатка являются основными участниками химических реакций, так как обладают электрическим зарядом и могут образовывать химические связи с другими частицами.
Катионы металла играют важную роль в катализе химических реакций. Они могут образовывать соединения с различными молекулами, за счет чего ускоряется процесс протекания реакции. Кроме того, катионы металла могут использоваться в качестве катализаторов для получения конкретных продуктов в химических преобразованиях.
Анионы кислотного остатка также играют важную роль в химических реакциях. Они могут вступать в реакции с различными катионами и образовывать новые соединения. Кроме того, анионы кислотного остатка могут служить как активаторы или ингибиторы химических реакций, влияя на скорость и направление процесса.
Взаимодействие катионов металла и анионов кислотного остатка происходит во многих химических реакциях. Они могут образовывать ионы с противоположным зарядом и образовывать ионные связи. Такие связи обеспечивают стабильность и прочность химических соединений. Кроме того, взаимодействие катионов металла и анионов кислотного остатка может приводить к образованию комплексных соединений с определенными свойствами и специфичностью.
Влияние катионов металла и анионов кислотного остатка на свойства соединений

Катионы металла и анионы кислотного остатка являются основными компонентами множества химических соединений. Их взаимодействия существенно влияют на свойства этих соединений.
Катионы металла, такие как Na+, Mg2+, Fe3+ и др., обладают различной валентностью и способностью образовывать комплексные соединения. Они могут вступать в контакт с анионами кислотного остатка и образовывать соли или координационные соединения. При этом важную роль играют заряд катиона, его радиус и способность координационной связи.
Анионы кислотного остатка, например SO42-, NO3-, Cl- и др., являются основными компонентами кислот и имеют выраженную электроотрицательность. Они способны образовывать с катионами металла ионообменные соединения или образовывать ковалентные связи. Это влияет на степень растворимости, термическую стабильность и другие свойства соединений.
Совместное присутствие катионов металла и анионов кислотного остатка может влиять на локальную среду в окружении ионов, приводя к изменению электрических и магнитных свойств, а также к химическим и физическим реакциям. Это, в свою очередь, может влиять на каталитическую активность, стабильность и другие важные свойства соединений.
Вопрос-ответ

Что такое катион металла?
Катион металла - это положительно заряженный ион металла, который образуется в результате потери одного или нескольких электронов металлом. Катионы металла играют важную роль во многих химических реакциях и имеют различные свойства и взаимодействия с анионами.
Какие свойства имеют катионы металла?
Катионы металла имеют несколько ключевых свойств. Во-первых, они обладают положительным зарядом и являются электрофильными, что означает, что они притягивают отрицательно заряженные частицы или анионы. Во-вторых, катионы металла обычно обладают каталитической активностью и способны ускорять химические реакции. Кроме того, катионы металла могут образовывать комплексные соединения с анионами или нейтральными молекулами, что может влиять на их свойства и реактивность.
