Калий - химический элемент с порядковым номером 19 в периодической таблице. Этот элемент является недовольным металлом, обладающим низкой плотностью и невысокой температурой плавления. В своем естественном состоянии калий представлен в виде твердого вещества, имеющего серебристо-белый цвет и мягкую текстуру.
Однако при нагревании калий быстро тает и превращается в жидкость, сохраняя свою химическую структуру. Это особенное свойство делает калий уникальным среди других металлов, так как большинство металлов имеют твердую форму в типичных условиях комнатной температуры и не плавятся до достижения высоких температур.
Стоит отметить, что жидкий калий обладает рядом интересных свойств и широко применяется в различных областях, таких как химическая промышленность, электроника и наука.
Вместе с тем, стоит помнить, что жидкий калий очень реактивен и подвержен окислению, поэтому требует особой осторожности в обращении. В контакте с воздухом калий образует оксиды, которые быстро разрушают его структуру. Поэтому в промышленности калий хранят и перевозят в вакуумированных ампулах или заливают под слоем легкой не реактивной жидкости, такой как скипидар.
Калий: история и свойства
Калий – химический элемент, открытый в 1807 году совместно немецкими учеными Хамфри Дэви и Генри Оссиллоу Томсоном. Имя калий получил по арабскому слову "кали", что означает "пастушеская соли".
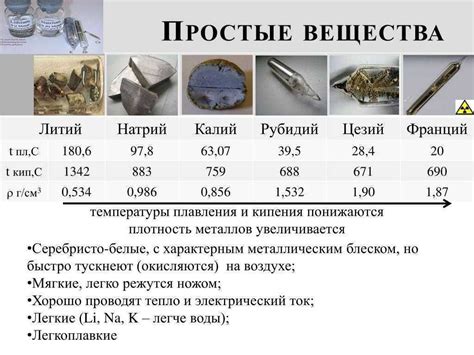
Калий относится к щелочным металлам, а его атомный номер равен 19. Он занимает четвёртое место среди элементов по распространенности в земной коре. Калий имеет серебристо-белый цвет и мягкую текстуру. Его плотность составляет около 0,86 г/см³. Калий обладает низкой плавкостью и кипением: соответственно 63,4 °C и 759 °C.
Одно из главных свойств калия – возможность взаимодействовать с водой, что является редкостью для металлов. При контакте с водой, калий реагирует с выделением водорода и образованием щелочной среды. Эта способность делает калий полезным в различных промышленных процессах и химических реакциях.
Калий является необходимым элементом для живых организмов. Он участвует в поддержании стабильного внутреннего баланса растворов в тканях и клетках. Кроме того, калий играет важную роль в проведении нервных импульсов и сокращении мышц.
Калий широко используется в различных отраслях промышленности, включая производство стекла, удобрений, жидкостей для теплоносителей и металлургических процессов. Он также находит применение в медицине для лечения некоторых болезней связанных с нарушением работы сердца и почек.
Калий в истории науки

Калий, химический элемент с атомным номером 19, был открыт в 1807 году английским химиком Хэмфри Дэви во время его исследования щелочных металлов. Дэви получил калий, разлагая его оксид калия с помощью электролиза. Это открытие сыграло важную роль в развитии химической науки и способствовало пониманию природы элементов и химических реакций.
Впоследствии ученые смогли изучить свойства и характеристики калия более подробно. Калий является мягким металлом серебристого цвета, который легко реагирует с водой, образуя щелочь и выделяя водород. Он также обладает высокой химической реактивностью и часто используется в различных химических процессах и промышленности.
Калий является неотъемлемым элементом живых организмов, играет важную роль в поддержании баланса воды и электролитов, нервной и мышечной функции, а также в работе сердечно-сосудистой системы. Калий присутствует во многих продуктах питания, таких как бананы, картофель, орехи и гречка. Его недостаток или избыток в организме может вызывать различные заболевания и патологические состояния.
Сегодня в научных исследованиях продолжают изучать свойства калия и его влияние на различные процессы. Благодаря развитию современных методов и технологий, ученые смогли расширить наши знания о калии и его роли в природе и жизни человека.
Физические свойства калия

Калий – алкалийный металл с атомным номером 19 в периодической таблице элементов. Он обладает мягкостью и низкой твердостью, поэтому его можно легко растирать пальцами. Калий обладает серебристо-белым блеском и мягким металлическим оттенком.
Температура плавления калия составляет около 63 градусов Цельсия, что делает его жидким при комнатной температуре. Это необычное свойство отличает калий от большинства других металлов, которые обычно являются твердыми при комнатной температуре.
Калий имеет низкую плотность – около 0,86 г/см³, что делает его легким металлом. Это позволяет ему плавать на поверхности воды. При контакте с водой калий реагирует с образованием гидроксида калия и выделяет гидроген. Данное свойство калия используется в химической и фармацевтической промышленности.
Калий обладает высокой электропроводностью. Он является хорошим проводником электричества и тепла, что делает его важным материалом в различных электрических приборах. Калий также является важным питательным элементом для растений и животных, необходимым для нормального функционирования их организмов.
Натрий и калий: сходства и различия

Натрий и калий являются элементами химической таблицы, относятся к группе щелочных металлов и обладают сходством в ряде характеристик.
Одним из основных сходств между натрием и калием является их металлическая природа. Оба элемента имеют ярко-серебристый цвет и относительно низкую плотность.
Еще одним общим свойством натрия и калия является их способность реагировать с водой. При контакте с водой образуется щелочь и выделяется водород.
Однако, несмотря на сходство, натрий и калий также имеют и некоторые различия. Одно из основных различий заключается в их активности. Калий является более активным элементом по сравнению с натрием. Он имеет большую склонность к реакциям и может вызывать возгорание при контакте с воздухом или водой.
Кроме того, натрий и калий также различаются по своим физическим свойствам. Натрий, например, имеет более низкую температуру плавления и кипения по сравнению с калием.
Таким образом, натрий и калий являются сходными по ряду характеристик, но имеют и ряд различий, которые делают их уникальными элементами в химической таблице.
Калий и натрий: химическое строение

Калий и натрий - два химических элемента, относящихся к группе щелочных металлов. Оба элемента имеют похожую химическую структуру и свойства, связанные с их электронными конфигурациями.
Калий и натрий обладают одной валентностью и образуют положительно заряженные йоны, K+ и Na+. Это позволяет им активно взаимодействовать с отрицательно заряженными ионами, образуя соли и окислы. Калий и натрий активно участвуют в обмене веществ в живых организмах.
Калий и натрий также обладают сходными физическими свойствами. Они являются мягкими металлами, обладают низкой плотностью и низкой температурой плавления. Калий и натрий относятся к активным металлам, способным реагировать с кислородом и водой.
Однако, несмотря на их схожесть, калий и натрий имеют и отличия в своей химической структуре. Натрий имеет один электрон во внешней электронной оболочке, а калий - два. Это отличие в электронной оболочке определяет различия в их реактивности и химических свойствах.
Таким образом, химическое строение калия и натрия, их валентность и электронная конфигурация определяют их сходство и различия в реактивности и свойствах, делая их важными элементами в химической и биологической науке.
Физические и химические свойства
Калий - химический элемент, обозначаемый символом K и имеющий атомный номер 19. В природе калий находится в виде минералов, таких как сильвинит и карналлит. Имеет серебристо-белый цвет и мягко-серую фракцию наружности.
Одним из наиболее удивительных свойств калия является его реакция с водой. Когда кусок калия помещается в воду, он начинает интенсивно реагировать, выбрасывая пузыри водорода и оставляя за собой след. Этот процесс также сопровождается выделением тепла, из-за чего вода может начать кипеть.
Калий является хорошим проводником электричества и тепла, и обладает низкой плотностью. Он имеет низкую температуру плавления - 63,25 °C (145,85 °F) и высокую температуру кипения - 759 °C (1398 °F), что делает его жидким металлом при комнатной температуре. Однако при хранении или принятии квадратной формы, калий переходит в твердое состояние.
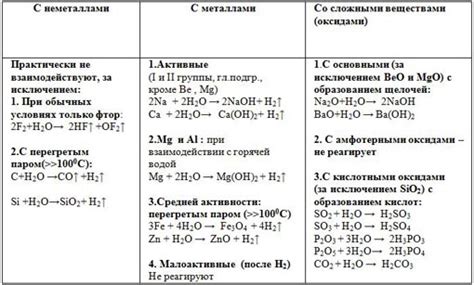
Калий реагирует с большинством неметаллов, таких как кислород, сера и фосфор, а также с многими органическими соединениями. Этот элемент также используется в различных промышленных процессах, таких как производство удобрений, стекла и синтез ракетного топлива.
Применение калия

Калий является одним из самых важных элементов, используемых в сельском хозяйстве. Он является неотъемлемой частью многих удобрений, таких как калийные соли. Калий вносит значительный вклад в повышение урожайности и качества сельскохозяйственных культур.
Калийная удобрения применяются для улучшения земли, повышения его плодородия и обеспечения растений необходимыми питательными веществами. Они также способствуют увеличению устойчивости растений к стрессовым условиям, таким как засуха или засоление почвы.
Калий применяется также в производстве стекла и мыла. Он является важным компонентом в производстве стекла, так как повышает его прочность и устойчивость к высоким температурам. Калий также используется в производстве мыла, так как поддерживает его моющие свойства и делает кожу более мягкой и гладкой.
Калий играет важную роль в работе нервной системы человека. Он помогает поддерживать электролитный баланс, регулирует давление крови и участвует в передаче нервных импульсов. Поэтому калий является необходимым элементом питания для поддержания здоровья человека.
В целом, калий является важным элементом в различных областях промышленности и сельском хозяйстве. Его применение способствует повышению урожайности сельскохозяйственных культур, улучшению качества стекла и мыла, а также поддержанию здоровья человека.
Калий в сельском хозяйстве

Калий — один из главных элементов питания растений и одна из основных питательных веществ в сельском хозяйстве. Он влияет на множество процессов в растениях и является неотъемлемой частью различных физиологических функций растений.
Калий играет важную роль в механизмах роста, фотосинтеза и обмена веществ растений. Он способствует усвоению растениями азота и фосфора, а также регулирует водный баланс растений. Благодаря наличию калия в почве, растения могут лучше переносить стрессы, такие как засуха или заморозки.
Калий также влияет на качество и урожайность сельскохозяйственных культур. Недостаток этого элемента может привести к низкому урожаю и ухудшению качества продукции. Поэтому важно обеспечить растения достаточным количеством калия, добавляя его в почву с помощью специальных удобрений или при помощи органического вещества, такого как компост или навоз.
Для определения содержания калия в почве и дозировки удобрений проводят анализ почвы и определяют ее плодородность. Использование правильных доз удобрений с калием позволяет улучшить урожайность и качество продукции, а также снизить воздействие вредителей.
Таким образом, калий является важным элементом в сельском хозяйстве, играющим ключевую роль в росте и развитии растений, а также в формировании качественного урожая.
Калий в медицине

Калий является одним из важнейших минералов для правильного функционирования нашего организма. Он играет ключевую роль в поддержании электролитного баланса, участвует в контроле сердечного ритма, регулирует функцию мышц и нервной системы.
В медицине калий используется для лечения различных состояний и заболеваний. Он применяется в качестве лекарственного средства для компенсации дефицита калия в организме. Такая нехватка может возникать, например, при заболеваниях почек, болезнях желудочно-кишечного тракта, потере больших количеств жидкости при повышенном потоотделении.
Калий также участвует в процессе постановки диагноза некоторых заболеваний и становится неотъемлемой частью медицинских исследований. Он используется для проведения биохимических анализов, в том числе анализов крови и мочи.
Однако следует помнить, что самолечение калием может быть опасным. Применение препаратов калия должно осуществляться под наблюдением врача, который учтет все индивидуальные особенности организма и состояние здоровья пациента. Перед началом применения калия в любой форме следует проконсультироваться с врачом и соблюдать его рекомендации.
Вопрос-ответ

Каковы основные свойства калия?
Калий - химический элемент, относящийся к группе щелочных металлов. Он обладает низкой плотностью, мягкостью, серебристым блеском и реагирует с водой, образуя щелочь. Также калий обладает хорошей проводимостью тепла и электричества.
Почему калий реагирует с водой?
Калий реагирует с водой из-за своей химической активности. При контакте с водой он образует щелочь и выделяет водород. Эта реакция является экзотермической, то есть сопровождается выделением тепла.
Как используется калий в промышленности?
Калий находит широкое применение в промышленности. Он используется в производстве удобрений, стекла, мыла, батарей, а также в некоторых химических реакциях. Калийные соединения играют важную роль в живой природе, так как являются необходимыми макроэлементами для растений и животных.
