Щелочноземельные металлы – это группа химических элементов, которые находятся во второй группе периодической таблицы Менделеева. К ним относятся бериллий, магний, кальций, стронций, барий и радий. Щелочные земли, по которым получили свое название эти металлы, встречаются в земной коре и являются важными для различных процессов в живых организмах.
В химии щелочноземельные металлы особо интересны тем, что они представляют последний элемент каждого периода в периодической таблице. Бериллий является заключительным элементом первого периода, магний – второго, кальций – третьего, стронций – четвертого, барий – пятого, а радий – шестого. Каждый из них обладает своей уникальной химической структурой и характеристиками.
Щелочноземельные металлы хорошо известны своей реакционной способностью и способностью образовывать соединения с другими элементами. Они обладают двумя валентными электронами в своей внешней электронной оболочке, что делает их очень активными при реакциях с другими элементами. Эти металлы широко используются в различных отраслях промышленности, включая производство сплавов, керамики, сельское хозяйство и медицину.
Щелочноземельные металлы
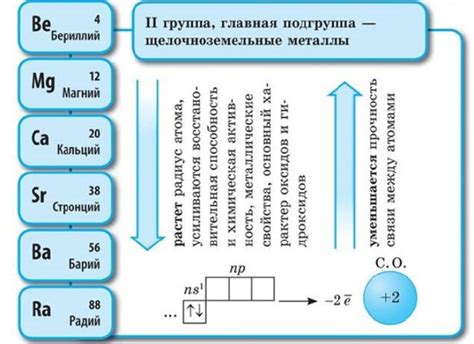
Щелочноземельные металлы — это элементы второй группы периодической таблицы, расположенные между щелочными металлами и переходными металлами. Они включают бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Щелочноземельные металлы обладают общими химическими свойствами. Они имеют два внешних электрона в своей валентной оболочке и образуют двойные положительные ионы. Эти металлы являются хорошими проводниками электричества и тепла, обладают металлическим блеском и обычно реактивны в контакте с водой и кислородом.
Бериллий является легким и прочным металлом с высокой температурой плавления. Он широко используется в промышленности, особенно в производстве сплавов и легких конструкций. Магний также имеет низкую плотность и используется в производстве сплавов, в том числе в авиационной и автомобильной промышленности.
Кальций, стронций и барий широко распространены в природе в виде соединений. Они играют важную роль в органическом и неорганическом мире. Например, кальций необходим для строения костей и зубов, стронций используется в различных технологических процессах, а барий используется в производстве стекла и радиологии.
Радий — самый тяжелый из щелочноземельных металлов и является радиоактивным. Из-за своей высокой радиоактивности и опасности он имеет ограниченное применение в научных и медицинских исследованиях.
Заключительные элементы
Щелочноземельные металлы представлены в таблице химических элементов сразу после элементов щелочных металлов. Эти металлы включают в себя бериллий, магний, кальций, стронций, барий и радий. Все они являются мягкими и легкоплавкими металлами, обладающими высокой электропроводностью и реакционноспособностью.
Бериллий - самый легкий из щелочноземельных металлов. Он является очень прочным и легким, обладает высокой теплопроводностью и применяется в производстве легких и прочных материалов, включая сплавы для авиационной и космической промышленности.
Магний - элемент, характеризующийся низкой плотностью и хорошей прочностью. Он широко используется в автомобильной и аэрокосмической промышленности, а также в производстве сплавов и легких конструкций.
Кальций - универсальный элемент, обладающий высокой реакционной способностью. Используется в многих отраслях промышленности, включая строительство, медицину и пищевую промышленность.
Стронций - элемент, имеющий много применений, включая использование в огнетушителях, фармацевтической и пиротехнической промышленности.
Барий - металл, входящий в состав специализированных стекол и используемый при производстве радиолюминесцентных красителей.
Радий - элемент, имеющий высокую радиоактивность. Используется в медицине для лечения определенных видов рака.
Каждого периода
В таблице периодов элементов Менделеева существует особая группа металлов, называемая щелочноземельными металлами. Каждый период этой группы заканчивается уникальным элементом, который обладает своими химическими и физическими свойствами.
В первом периоде щелочноземельные металлы представлены элементом бериллием. Этот металл обладает высокой твердостью, является легким и прочным, непричастен к коррозии. Бериллий широко используется в аэрокосмической промышленности, в производстве рентгеновских трубок и в других технических целях.
Во втором периоде щелочноземельные металлы заканчиваются элементом магнием. Этот металл обладает низкой плотностью, высокой прочностью и хорошей термической проводимостью. Магний широко применяется в авиационной и автомобильной промышленности, в производстве сплавов и ферросплавов, и находит применение в производстве магниевых труб и конструкций.
В третьем периоде щелочноземельными металлами являются элементы стронций и кальций. Стронций обладает ярким красным свечением при горении, и его соединения используются в производстве радиолюминесцентных красок и пирофорных веществ. Кальций является необходимым элементом для живых организмов, и широко применяется в качестве пищевой добавки и в производстве строительных материалов.
Техническое применение

Щелочноземельные металлы находят широкое применение в технической сфере благодаря своим уникальным физическим и химическим свойствам.
Кальций используется в металлической промышленности для производства арматурных сталей, а также в производстве алюминия и некоторых других металлов. Он служит основным компонентом различных сплавов, которые применяются в прокатном производстве. Кальций также используется для отделки и покрытия металлических поверхностей.
Стронций используется в производстве пиротехнических составов, так как способен придавать яркие красные и фиолетовые оттенки пламени. Он также применяется в производстве красок, стекла и светоизлучающих диодов. Кроме того, стронций используется в ядерной энергетике для производства стронций-90, который применяется в источниках радиации для лечения рака.
Барий широко применяется в рентгенологии, где его соединения используются для создания контрастных веществ. Он также добавляется в стекло и керамику для получения высокой плотности и яркого блеска. Барий-сульфат применяется в желудочно-кишечной рентгенографии, а барий-титанат используется в производстве конденсаторов.
Радий используется в промышленности для создания световыводящих материалов, таких как радий-цинковые сульфидные фотокатоды. Он также используется в научных исследованиях и в медицине для лечения определенных форм рака.
Химические свойства

Бериллий образует стабильные соединения со многими элементами, особенно с кислородом. Бериллий окисляется на воздухе лишь при повышенной температуре, но его соединения с кислородом очень реакционны. К примеру, бериллий оксид и бериллиевая соль, обладающие щелочными свойствами, растворяются в воде с образованием щелочной среды. Бериллий способен образовывать стабильные комплексные соединения с органическими и неорганическими веществами.
Магний реактивен при нагревании воздуха и взаимодействии с водой, но его поверхность быстро покрывается оксидной пленкой, которая препятствует дальнейшей реакции. Магний соединяется с большинством неметаллов, образуя стабильные соединения с большим количеством элементов. Легкость формирования и регулярность структуры способствуют широкому применению магния в различных сферах промышленности и научных исследований.
Кальций активен в отношении воды и окисляется на воздухе, образуя оксид. Кальций реагирует с многими неорганическими и органическими соединениями и может служить ионом для образования многих неорганических солей. Кальций играет важную роль в строении костей и зубов у животных и людей и является неотъемлемым элементом для многочисленных биологических процессов в организмах живых существ.
Стронций не образует соединений с кислородом, но может реагировать с водой и некоторыми кислотами. Стронций широко используется в пиротехнической и фармацевтической промышленности, а также как компонент для производства стекла и магнитных материалов.
Барий реагирует со многими веществами, включая воду, кислород и некоторые кислоты. Барий имеет высокую плотность и используется в производстве легированных сталей, а также в некоторых радиологических исследованиях.
Физические свойства

Щелочноземельные металлы обладают рядом характерных физических свойств.
Первым из них является невысокая плотность. Бериллий, магний, кальций и другие элементы этой группы имеют относительно низкую плотность, что делает их легкими и малоупругими материалами.
Второе свойство - мягкость. Щелочноземельные металлы достаточно мягкие и податливые, что позволяет легко изменять их форму и использовать в различных технических процессах.
Третье свойство - хорошая теплопроводность. Щелочноземельные металлы хорошо проводят тепло, что делает их полезными материалами в производстве теплообменников и других устройств, где важна эффективная передача тепла.
Кроме того, важными физическими свойствами щелочноземельных металлов являются их точка плавления и кипения, которые позволяют использовать их в различных процессах плавления и отжига металлов и сплавов.
Производство и добыча

Производство и добыча щелочноземельных металлов является важной отраслью промышленности, в которой задействованы различные технологии и методы. Главные источники добычи щелочноземельных металлов - это рудники и карьеры, где производится извлечение руды из земли.
Для добычи и выплавки щелочноземельных металлов применяются различные процессы, включая помол руды, флотацию, гравитационные и магнитные методы обогащения. Щелочноземельные металлы эффективно сгущаются в перекиси бария или фториде натрия, что позволяет осуществить их высокоочистку и получение металлов высокой чистоты.
Значительная часть производства щелочноземельных металлов приходится на Китай, который является одним из крупнейших производителей и экспортеров этих металлов. Китай также осуществляет добычу редких земель и других редких металлов, которые часто сопровождают эксплуатацию щелочноземельных металлов.
Производство и добыча щелочноземельных металлов требуют строгого соблюдения экологических норм и правил, так как неконтролируемая выработка и отходы могут негативно повлиять на окружающую среду. Компании, занимающиеся производством и добычей, должны уделять особое внимание экологическим мерам и постоянно совершенствовать технологии для снижения вредного воздействия.
История открытия

Щелочноземельные металлы - группа элементов, расположенных во второй группе периодической системы Д.И. Менделеева. Их открытие было важным шагом в развитии химии и произошло благодаря работе нескольких ученых.
Магний был открыт в 1755 году шведским химиком Андреасом Марграфом. Он обнаружил, что остаток после выгорания магнезита содержит новый элемент, который назвал магнием.
Английский химик Сэр Дэви Джон стал первым, кто получил кальций в чистом виде в 1808 году. Он электролизировал расплавленный хлорид кальция, и на аноде образовался металлический кальций.
Стронций был получен в 1808 году французским химиком Адольфом Вильгельмом Голстедом. Он изолировал стронций путем электролиза сульфата стронция.
Металл барий впервые получил в 1808 году химик из Англии Сэр Хамфри Дэви, производя электролиз кислоты бария.
Радий был открыт в 1898 году французским физиком и химиком Пьером и Мари Кюри. Они обработали минерал питца (фторид бария) и обнаружили новый элемент, который назвали радием в связи с его радиоактивными свойствами.
Значение для человека
Щелочноземельные металлы играют важную роль в жизни человека и имеют широкое применение в различных отраслях.
Первоначально, эти металлы используются в медицине. Некоторые из них, такие как магний и кальций, необходимы для нормального функционирования организма. Они участвуют в процессах обмена веществ, поддерживая здоровые кости и зубы, нервную систему и сердечно-сосудистую систему, а также обеспечивая нормальную работу мышц.
Калий также имеет медицинское значение, поскольку он регулирует водно-солевой баланс в организме и поддерживает нормальное функционирование сердца. Он используется в лечении некоторых сердечно-сосудистых заболеваний и заболеваний почек.
Щелочноземельные металлы также находят применение в производстве специальных сплавов, которые используются в авиационной и космической промышленности, а также в электротехнике. Магний, кальций и барий широко используются в литейном производстве и машиностроении. Бериллий, который относится к щелочноземельным металлам, имеет высокую прочность и малый вес, и поэтому применяется в производстве легких и прочных сплавов.
Щелочноземельные металлы также используются в производстве стекла, осветительных приборов и пиротехники. Барий используется в производстве рентгеновского оборудования, а стронций - в производстве огнетушителей.
Таким образом, щелочноземельные металлы имеют значительное значение для человека, они влияют на наше здоровье, обеспечивают работу многих отраслей промышленности и содействуют нашему комфортному существованию.
Вопрос-ответ

Какие элементы относятся к группе щелочноземельных металлов?
К группе щелочноземельных металлов относятся следующие элементы: Бериллий (Be), Магний (Mg), Кальций (Ca), Стронций (Sr), Барий (Ba) и Радий (Ra).
Чем характеризуются щелочноземельные металлы?
Щелочноземельные металлы характеризуются высокой химической реактивностью, низкой плотностью, низкой температурой плавления и высокой проводимостью электричества.
Какие свойства у щелочноземельных металлов обусловлены их электронной структурой?
Свойства щелочноземельных металлов, такие как высокая активность и низкая электроотрицательность, обусловлены наличием двух валентных электронов в s-подуровне внешней электронной оболочки каждого атома.
Какую роль играют щелочноземельные металлы в природе?
Щелочноземельные металлы играют важную роль в природе, так как они являются необходимыми макроэлементами для растений и животных. Они также используются в различных промышленных процессах, включая производство стекла, сплавов и легких металлов.
