Активные металлы - это группа элементов, которые обладают высокой реактивностью и способностью активно взаимодействовать с другими веществами. Они часто используются в различных химических реакциях и промышленных процессах.
Среди основных представителей активных металлов можно выделить натрий, калий, литий, магний, цезий и кальций. Эти элементы встречаются в природе в виде соединений и широко используются в различных сферах деятельности человека, таких как металлургия, электроэнергетика, фармацевтическая и пищевая промышленность.
Основными свойствами активных металлов являются низкая плотность, низкая температура плавления и кипения, а также способность образовывать ионы с положительным зарядом. Они хорошо проводят тепло и электричество, а также обладают высокой реакционностью с водой, кислотами и воздухом.
Например, натрий является одним из самых распространенных и доступных активных металлов, который широко используется в производстве стекла, щелочей и металлических сплавов. Калий применяется в производстве удобрений и взрывчатых веществ, а литий используется в производстве акумуляторов и лекарств.
Определение активных металлов и изучение их свойств имеет важное значение в научных и технических исследованиях. Благодаря их химическим и физическим свойствам, активные металлы являются незаменимыми компонентами во многих производственных процессах и находят широкое применение в различных отраслях промышленности.
Активные металлы: общие сведения
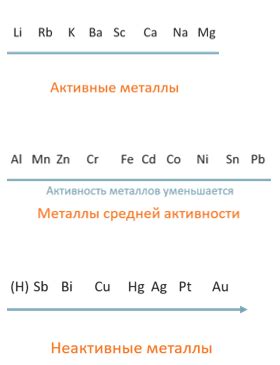
Активные металлы - это химические элементы, которые обладают высокой реакционной способностью. Они легко вступают в химические реакции с другими веществами, особенно с кислородом и водой. Активные металлы находятся в левой части периодической системы элементов и включают представителей таких групп, как щелочные металлы (например, литий, натрий, калий), щелочноземельные металлы (например, магний, кальций, барий) и некоторые элементы из группы цинка.
Основная характеристика активных металлов - их способность активно реагировать с кислородом, образуя оксиды. Например, литий с горящим пламенем горит в воздухе, образуя оксид лития. В реакции с водой активные металлы образуют щелочные растворы, которые являются сильными основаниями. Например, натрий реагирует с водой, образуя щелочь натрия и выделяя водород. Эти свойства активных металлов делают их полезными в различных областях, таких как производство щелочных батарей и используются для удаления из воды вредных примесей и очистки воды.
Важно отметить, что активные металлы имеют высокую аффинность к кислороду и поэтому их наличие в природе преимущественно в соединениях, а не в свободном состоянии. Они также имеют низкую плотность, что делает их легкими и легко подвижными. Некоторые активные металлы, такие как магний и алюминий, также обладают хорошей коррозионной стойкостью и используются в строительстве и авиационной промышленности.
В таблице ниже представлены некоторые основные свойства активных металлов:
| Группа | Представители | Общие свойства |
|---|---|---|
| Щелочные металлы | Литий, натрий, калий | Низкая плотность, низкая температура плавления, реакция с водой |
| Щелочноземельные металлы | Магний, кальций, барий | Хорошая коррозионная стойкость, высокая реакционная способность |
| Цинк | Цинк | Химически активен, используется во многих индустриальных процессах |
В заключение, активные металлы представляют собой группу химических элементов, которые легко реагируют с другими веществами. Их свойства делают их полезными в различных областях, от производства батарей до очистки воды. Активные металлы имеют высокую реакционную способность и химическую активность, что делает их одними из важных веществ в химической промышленности.
Определение активных металлов

Активные металлы - это группа химических элементов, которые проявляют высокую активность при взаимодействии с другими веществами. Такие металлы легко окисляются, что означает, что они тенденциозно отдают свои электроны и образуют положительные ионы, называемые катионами.
Основные представители активных металлов включают литий (Li), натрий (Na), калий (K), цезий (Cs) и рубидий (Rb). Эти элементы принадлежат к первой группе периодической таблицы и имеют одну электрон во внешней электронной оболочке. Вследствие этого, они готовы легко отдавать этот электрон, чтобы образовать положительный ион с одним зарядом.
Активные металлы обладают свойствами, которые делают их полезными в различных сферах. Они хорошо проводят тепло и электричество, поэтому используются в производстве электроники и проводимости. Они также обладают низкой плотностью и хорошей пластичностью, что делает их применимыми в металлургии и строительстве.
Однако активные металлы также имеют свойства, которые делают их опасными или трудно обрабатываемыми в некоторых случаях. Например, они реагируют с водой, образуя горючие газы, поэтому осторожность необходима при их хранении и использовании. Кроме того, они склонны к коррозии воздухом и другими химическими веществами, поэтому требуют дополнительных методов защиты и консервации.
Свойства активных металлов

Активные металлы – это элементы, обладающие высокой химической активностью. Они легко взаимодействуют с другими веществами, особенно с кислородом и водой. Самыми известными активными металлами являются литий (Li), натрий (Na), калий (K) и магний (Mg).
Одно из основных свойств активных металлов – их способность реагировать с водой. При контакте с водой активные металлы мгновенно выделяют водород, образуя гидроксиды. Например, реакция лития с водой протекает с такой силой, что может вызвать искры или даже возгорание.
Активные металлы обладают также высокой электропроводностью. Они являются хорошими проводниками электрического тока и широко применяются в электронике и электротехнике. Литий и натрий, например, используются в производстве аккумуляторов для мобильных устройств и электромобилей.
Еще одним важным свойством активных металлов является способность образовывать соли с кислотами. Подобные реакции широко используются в химической промышленности. Например, калийное удобрение – соль калия (KCl) – производится из калийной руды, содержащей калийные соединения.
Общей чертой активных металлов является их низкая плотность. Литий и натрий входят в число самых легких металлов, что делает их удобными для использования в легкой промышленности и авиации. Кроме того, активные металлы обладают высокой теплопроводностью, что также находит применение в различных отраслях промышленности, например, в производстве радиаторов и теплообменников.
Представители активных металлов

Активные металлы являются важной группой элементов, которые проявляют высокую химическую активность и реактивность. Эти металлы способны активно взаимодействовать с другими элементами и веществами. Они обладают свойствами, такими как высокая электропроводность, тугоплавкость и способность образовывать ионы положительного заряда.
Один из наиболее известных представителей активных металлов - это литий. Литий является самым легким из металлов и обладает высокой электропроводностью. Он также является наиболее реактивным из всех металлов, способным реагировать даже с водой. Литий широко используется в производстве литиевых аккумуляторов, а также в фармацевтической и сельскохозяйственной промышленности.
Еще одним представителем активных металлов является натрий. Натрий также обладает высокой реактивностью и способностью реагировать с водой. Он широко используется в пищевой промышленности, в производстве стекла и мыла. Натрий также играет важную роль в регулировании водного баланса в организмах животных и растений.
Калий является еще одним из представителей активных металлов. Этот металл также реактивен и способен взаимодействовать с водой. Калий играет важную роль в регулировании клеточного равновесия и функционировании нервной системы в организмах животных и растений. Он также используется в производстве удобрений и стальных сплавов.
Таким образом, представители активных металлов, такие как литий, натрий и калий, обладают высокой химической активностью и имеют широкие применения в различных областях науки и промышленности.
Натрий

Натрий — химический элемент с атомным номером 11 и символом Na в периодической системе. Он относится к группе щелочных металлов и имеет серебристо-белый цвет. Натрий является одним из основных представителей активных металлов.
У натрия высокая химическая реакционность. Он реагирует с водой с образованием щелочи и выделением водорода. Натрий также активно реагирует с кислородом, образуя оксид натрия. Это свойство делает его нестабильным в открытом воздухе и требует хранения в специальных условиях.
Натрий широко используется в промышленности, особенно в производстве щелочей, стекла и металлов. Он также используется в биологии и медицине в качестве важного элемента в организме. Натрий необходим для многих жизненно важных функций, включая регулирование водного баланса, передачу нервных импульсов и сокращение мышц.
Натрий имеет многочисленные применения в повседневной жизни. Его соединения используются в производстве пищевых добавок, моющих средств, косметики и бытовой химии. Натриевые ионные батареи также используются в устройствах с высоким энергопотреблением, таких как ноутбуки и мобильные телефоны.
Калий

Калий является одним из наиболее известных и широко распространенных активных металлов. Он относится к первой группе периодической таблицы и имеет атомный номер 19. Калий является третьим элементом алкалиевой группы и химически очень активным металлом, который реагирует с водой, кислородом и многими другими соединениями.
Основные свойства калия включают низкую плотность, мягкость, серый цвет и хорошую теплопроводность. Калий также обладает низкой температурой плавления и кипения, что делает его хорошим материалом для различных промышленных и научных приложений.
Калий широко используется в различных отраслях, включая производство удобрений, стекла, мыла, жиров и многих других продуктов. Он также используется в химической промышленности для получения различных соединений калия.
Примеры применения калия:
- В производстве удобрений для повышения плодородия почвы.
- В производстве стекла для придания ему особых свойств.
- В производстве мыла для его моющих свойств.
- В производстве жиров для консервации пищевых продуктов.
В заключение, калий является одним из наиболее важных и полезных активных металлов, который находит свое применение в различных отраслях промышленности и имеет множество полезных свойств и приложений.
Рубидий

Рубидий - активный алкалийный металл, химический элемент периодической системы с атомным номером 37 и символом Rb. Он находится в первой группе элементов, вместе с литием, натрием, калием и цезием. Рубидий - один из самых редких элементов на Земле, его содержание в земной коре составляет всего около 0,006%.
Рубидий встречается природным образом в минералах, таких как лепидолит и полевые шпаты. Он является мягким, серебристо-белым металлом, который быстро реагирует с водой и влажным воздухом, образуя гидроксид рубидия и оксид рубидия соответственно.
Рубидий обладает несколькими интересными свойствами. Во-первых, он является очень реактивным и может реагировать с различными веществами, включая воду, кислород и некоторые органические соединения. Во-вторых, рубидий имеет наибольшую ионизационную энергию среди всех алкалийных металлов, что делает его полезным во многих технических и научных приложениях.
Использование рубидия включает создание специальных стекол, лазеров, фоточувствительных устройств и ядерных реакторов. Также рубидий используется в медицине для лечения некоторых заболеваний, таких как диабет и гипертония.
Несмотря на свою редкость, рубидий имеет некоторые практический применения и значительный научный интерес. Его свойства и потенциал для использования в различных областях делают его одним из активных металлов, заслуживающим внимания и изучения.
Цезий

Цезий – это мягкий, серебристо-белый металл, который характеризуется высокой реактивностью и химической активностью. Он является одним из самых активных металлов и хорошо растворим в воде и других растворителях.
Цезий обладает низкой плотностью и низкой температурой плавления, что делает его применимым в различных технологиях, включая производство электронных компонентов и вакуумных устройств. Он также используется в радиационных источниках и коммуникационных системах.
Помимо своих промышленных применений, цезий может использоваться в медицинских исследованиях и диагностике, так как он обладает радиоактивными свойствами. Однако из-за своей высокой реактивности и токсичности цезий требует особой осторожности при его обработке.
Цезий является редким элементом и встречается в природе в виде минералов, таких как полевые шпаты и лепидолит. Основные производители цезия включают Россию и Китай.
Вопрос-ответ

Как определить активные металлы?
Определение активных металлов осуществляется на основе их способности вступать в реакцию с кислородом или водой. Активные металлы легко окисляются, образуя гидроксиды или оксиды. Также они обладают способностью образовывать ионные соединения с отрицательными анионами.
Какие основные представители активных металлов?
Основными представителями активных металлов являются литий, натрий, калий, рубидий, цезий, магний, кальций, барий и стронций. Они находятся в первых трех группах периодической таблицы.
Какие свойства характерны для активных металлов?
У активных металлов есть несколько характерных свойств. Они обладают металлическим блеском, хорошо проводят тепло и электричество, обладают низкой плотностью и низкой температурой плавления. Они также реагируют с воздухом, водой и кислотами.
Как ведут себя активные металлы в реакциях с водой и кислотами?
Активные металлы реагируют с водой, образуя гидроксиды и высвобождая водород. С растворенными кислотами они образуют соли и высвобождают водород. Например, при реакции натрия с водой образуется гидроксид натрия и высвобождается водородный газ.
Что представляют собой гидроксиды и оксиды активных металлов?
Гидроксиды активных металлов представляют собой соединения металла с гидроксильной группой (OH-). Они обычно являются кристаллическими веществами, растворяются в воде и обладают щелочными свойствами. Оксиды активных металлов представляют собой соединения металла с кислородом. Они обычно являются твердыми веществами и обладают основными свойствами.
