Серная кислота (H2SO4) является одной из наиболее распространенных и использованных кислот в химической промышленности. Она обладает мощными окислительными свойствами и широко применяется в различных отраслях, включая производство удобрений, промышленности кожи и текстиля, а также в процессе очистки воды. Взаимодействие серной кислоты с металлами часто сопровождается химической реакцией, которая может приводить к образованию соответствующих солей и выделению водорода.
Список металлов, способных к химической реакции с серной кислотой, включает ряд элементов из различных групп периодической системы. Сюда входят титан, железо, медь, алюминий, цинк, никель, марганец и др. Однако, не все металлы способны реагировать с серной кислотой одинаково интенсивно. Некоторые металлы, такие как золото и платина, обладают высокой устойчивостью и не реагируют с серной кислотой без присутствия других окислителей или катализаторов.
Реакция металлов с серной кислотой может происходить двумя основными способами: с образованием соли и водорода. При этом, серная кислота действует как окислитель, перенося электроны на металл, а металл отдает электроны, становясь положительно заряженным и образуя соответствующую соль. Образование водорода происходит при разложении молекулы серной кислоты на ионы водорода и сульфатные ионы.
Реакция металлов с серной кислотой

Серная кислота (H2SO4) является одним из самых распространенных и важных химических соединений. Она обладает сильными окислительными свойствами и является хорошим реагентом для окисления различных веществ. Взаимодействие металлов с серной кислотой протекает по реакции:
Металл + Серная кислота → Сернокислотный раствор + Выделение водорода
Реакция металлов с серной кислотой может протекать с различной интенсивностью в зависимости от их активности. Наиболее активные металлы проявляют сильное окислительное действие на кислоту и могут даже вызвать ее воспламенение.
К ним относятся, например, активные щелочные металлы, такие как натрий (Na) и калий (K). При контакте с серной кислотой они сильно нагреваются, выделяются характерные пламенные газы и искры, а в результате реакции образуются сернокислотные растворы с высокой концентрацией.
Более пассивные металлы, как цинк (Zn) и железо (Fe), тоже могут реагировать с серной кислотой, но реакция протекает уже медленнее и менее интенсивно. В данном случае образуются разбавленные сернокислотные растворы и выделяются газы.
Однако, некоторые металлы, например, серебро (Ag) и золото (Au), с серной кислотой не реагируют, так как они являются термодинамически стабильными и имеют низкую активность. Это свойство позволяет использовать серную кислоту для очистки и хранения этих драгоценных металлов.
Таким образом, реакция металлов с серной кислотой зависит от их активности и может протекать с различной интенсивностью. При взаимодействии образуются сернокислотные растворы и выделяется водород, что делает эту реакцию важной с точки зрения промышленных и лабораторных процессов.
Список металлов, испытывающих химическую реакцию
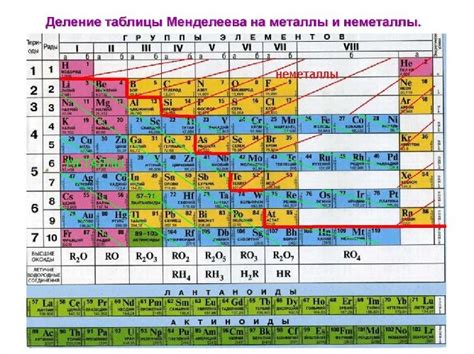
Металлы могут вступать в химическую реакцию с различными веществами, включая кислоты. Одной из наиболее распространенных реакций металлов является их взаимодействие с серной кислотой. Серная кислота – это сильная кислота, состоящая из сероводорода и кислорода. При контакте с некоторыми металлами происходит окислительно-восстановительная реакция, в результате которой металл образует соль серной кислоты и выделяется сероводород.
Среди металлов, способных к химической реакции с серной кислотой, можно выделить следующие:
- Цинк – цинк вступает в реакцию с серной кислотой, образуя соль цинка и выделяя сероводород;
- Железо – железо также реагирует с серной кислотой, образуя соль железа и выделяя сероводород;
- Алюминий – алюминий окисляется серной кислотой, образуя соль алюминия и выделяя сероводород;
- Медь – медь реагирует с серной кислотой, образуя соль меди и выделяя сероводород;
- Свинец – свинец также реагирует с серной кислотой, образуя соль свинца и выделяя сероводород.
Это лишь некоторые примеры металлов, которые могут вступать в химическую реакцию с серной кислотой. Важно помнить, что химическая реакция зависит от условий, в которых она происходит, а также от концентрации и температуры реагирующих веществ.
Механизм реакции металлов с серной кислотой
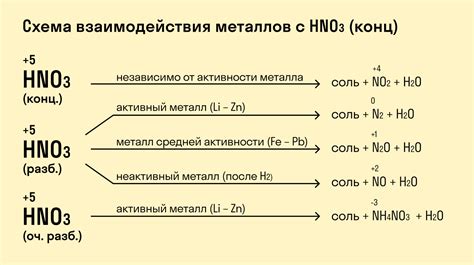
Реакция металлов с серной кислотой происходит по следующему механизму:
- Диссоциация кислоты: Серная кислота (H2SO4) диссоциирует на ионы водорода (H+) и сульфатные ионы (SO42-). Это происходит благодаря воде, которая является растворителем кислоты.
- Окисление металла: Металл реагирует с ионами водорода, окисляясь и образуя положительные ионы металла (M+). Это происходит из-за разницы в электрохимическом потенциале металла и ионов водорода.
- Образование сульфата металла: Положительные ионы металла соединяются с отрицательными сульфатными ионами, образуя сульфат металла (M2SO4).
Таким образом, реакция металлов с серной кислотой приводит к образованию сульфата металла и водорода. Механизм этой реакции зависит от электрохимических свойств металла и его способности окисляться.
Некоторые металлы, такие как цинк и железо, обладают достаточно высокой активностью и легко реагируют с серной кислотой. Другие металлы, такие как свинец и медь, менее активны и реакция с ними происходит медленнее.
Реакция металлов с серной кислотой может использоваться для получения соответствующих сульфатов металлов, которые в дальнейшем могут быть использованы в различных отраслях промышленности.
Важность реакции металлов с серной кислотой в промышленности
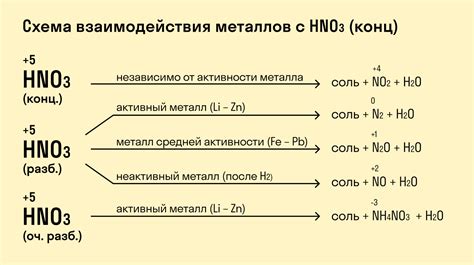
Реакция металлов с серной кислотой играет важную роль в промышленности, так как образующиеся в результате продукты реакции имеют широкий спектр применения. Эта химическая реакция является одной из основных для получения серной кислоты и ее соединений.
Первое, что делают в промышленности, это выбирают подходящие металлы для реакции с серной кислотой. К таким металлам относятся цинк, железо, алюминий и некоторые другие. В процессе реакции, серная кислота взаимодействует с металлом, образуя сульфатные соли и выделяяся молекулярный водород. Это содержание серной кислоты преследуют зачастую целенаправленно и достигают высокой концентрации, расширяя возможности применения в различных областях промышленности.
Серная кислота находит применение в производстве удобрений, в качестве катализатора во многих химических процессах, а также используется при очистке металлических поверхностей и водопроводных труб от ржавчины и накипи. Она также активно используется в батареях, аккумуляторах и других электрохимических устройствах.
Важность реакции металлов с серной кислотой в промышленности заключается не только в получении серной кислоты, но также в широком спектре применения образующихся продуктов реакции. Они находят применение в различных отраслях и процессах, что делает данную реакцию неотъемлемой частью промышленности.
Вопрос-ответ

Какие металлы могут реагировать с серной кислотой?
С серной кислотой реагируют различные металлы, включая цинк, железо, свинец, медь, алюминий, никель, кадмий, кобальт. Это обусловлено их активностью в химических реакциях.
Какие металлы не реагируют с серной кислотой?
Некоторые металлы, такие как золото, платина, серебро, не реагируют с серной кислотой. Это связано с их низкой активностью.
Как происходит реакция металлов с серной кислотой?
Реакция металлов с серной кислотой происходит с выделением газа — сернистого ангидрида (SO2) и образованием соответствующих сульфатов. При этом металлы окисляются, а серная кислота восстанавливается.
